国家药监局继续推进体外诊断试剂应急审批工作
- 2020-02-21 17:38
- 作者:胡芳
- 来源:中国食品药品网
中国食品药品网讯(记者胡芳) 疫情发生后,国家药监局迅速启动医疗器械应急审批程序,按照“统一指挥、早期介入、随到随审、科学审批”的原则和确保产品安全、有效、质量可控的要求,全力加快审评审批速度。目前为止,已批准7家企业7个新冠病毒核酸检测产品(共9个注册证)。
近日,记者从国家药监局获悉,第一批应急审批医疗器械陆续获批后,国家药监局继续推动第二批医疗器械应急审批工作,应急审批的产品包括抗体类检测试剂、核酸荧光PCR检测试剂,以及其他方法学产品。
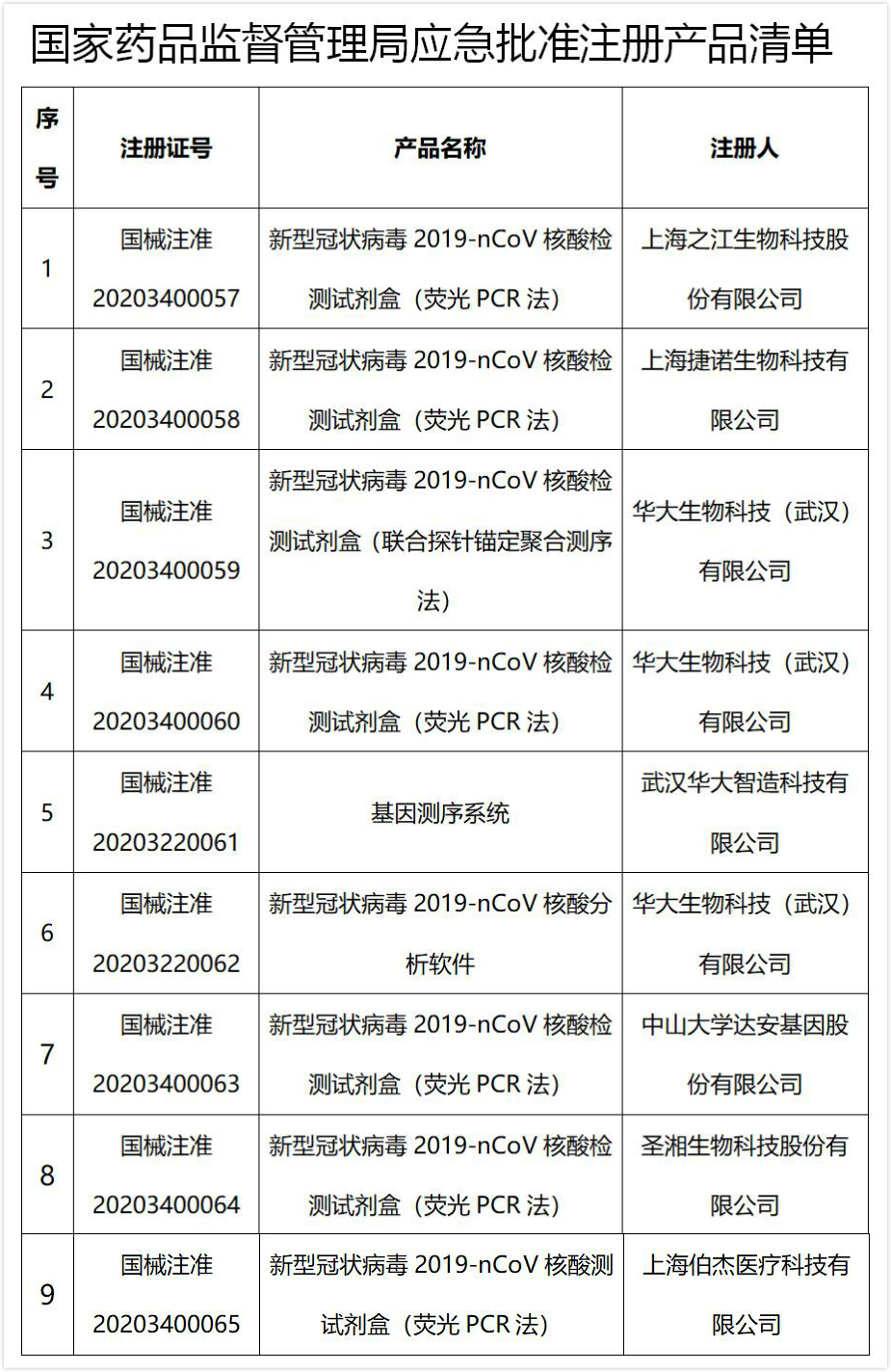
图为国家药品监督管理局应急批准注册产品清单。
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:张可欣)
分享至
×
右键点击另存二维码!
网民评论
欢迎
登录
-
为你推荐
-

-












