每周医药看点(3.23-4.5)
- 2022-04-06 15:34
- 作者:刘思慧
- 来源:中国食品药品网
中国食品药品网讯 国务院办公厅印发《“十四五”中医药发展规划》;《国家药品不良反应监测年度报告(2021年)》发布 ……3月23日—4月5日,医药行业的这些事情值得关注。
行业政策动态
1.国务院办公厅印发《“十四五”中医药发展规划》。《规划》明确了“十四五”期间中医药发展的指导思想、基本原则、发展目标、主要任务和重点措施,提出到2025年,中医药健康服务能力明显增强,中医药高质量发展政策和体系进一步完善,中医药振兴发展取得积极成效,在健康中国建设中的独特优势得到充分发挥。
2.国家药监局综合司就《药品上市许可持有人检查要点(征求意见稿)》公开征求意见。该征求意见稿适用于对委托生产药品的境内持有人的监督检查,对于境内自行生产药品的持有人也可参照开展监督检查。
3.国家药品不良反应监测中心发布《国家药品不良反应监测年度报告(2021年)》。《报告》显示,2021年国家药品不良反应监测报告数量和质量双提升,全国药品不良反应监测网络收到《药品不良反应/事件报告表》196.2万份,每百万人口平均报告数增加到1392份,全国98.0%的县级地区报告了药品不良反应/事件,药品上市许可持有人报告数量及其占比提升,国家基本药物监测总体情况基本保持平稳。
4.国家药监局药审中心(CDE)公示第五十七批化学仿制药参比制剂目录,涉及甲磺酸达拉非尼胶囊等药品。公示期限为2022年3月25日—4月8日。
5.CDE发布《胰岛素类产品生物类似药药学研究与评价技术指导原则》,以规范和指导胰岛素类产品生物类似药的研发、生产和注册,进一步明确技术评价标准。
6.国家卫生健康委办公厅、国家中医药管理局办公室联合发布《关于调整抗新型冠状病毒药物PF-07321332/利托那韦片(Paxlovid)适应症等内容的通知》。其中,适应症调整内容为发病5天以内的轻型和普通型且伴有进展为重症高风险因素的成人。
产品研发/上市信息
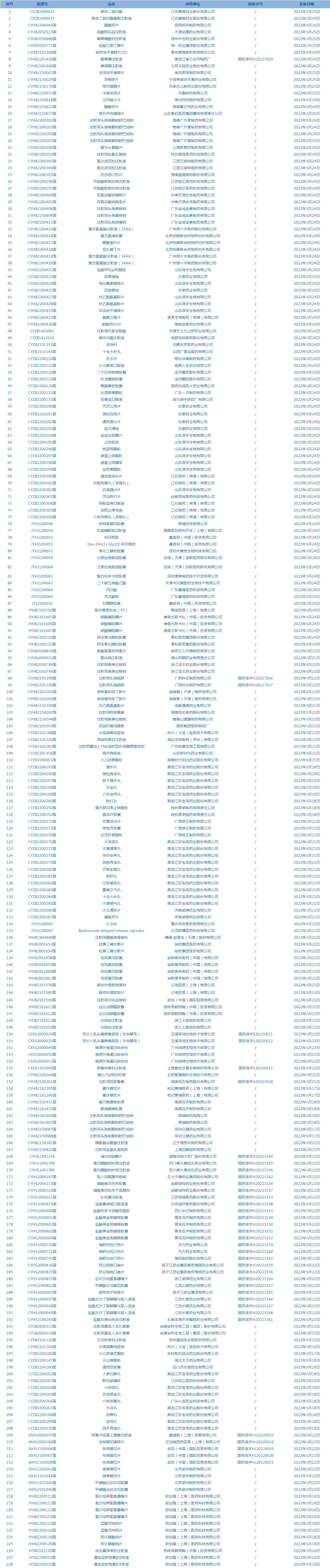
1.国家药监局发布3期药品批准证明文件待领信息,共包括228个受理号,涉及江苏康缘药业股份有限公司等企业。(截至4月5日)
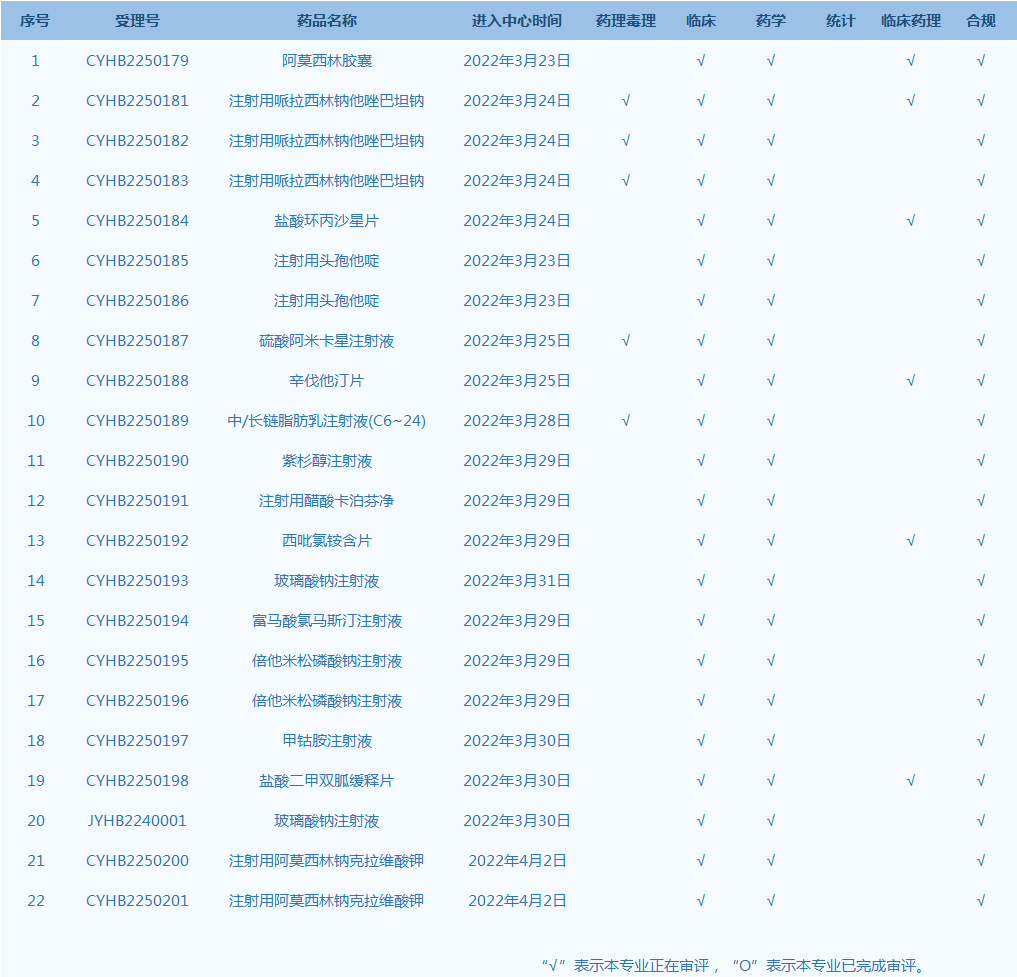
2.CDE网站公示22个仿制药一致性评价任务,涉及阿莫西林胶囊等药品。(截至4月5日)
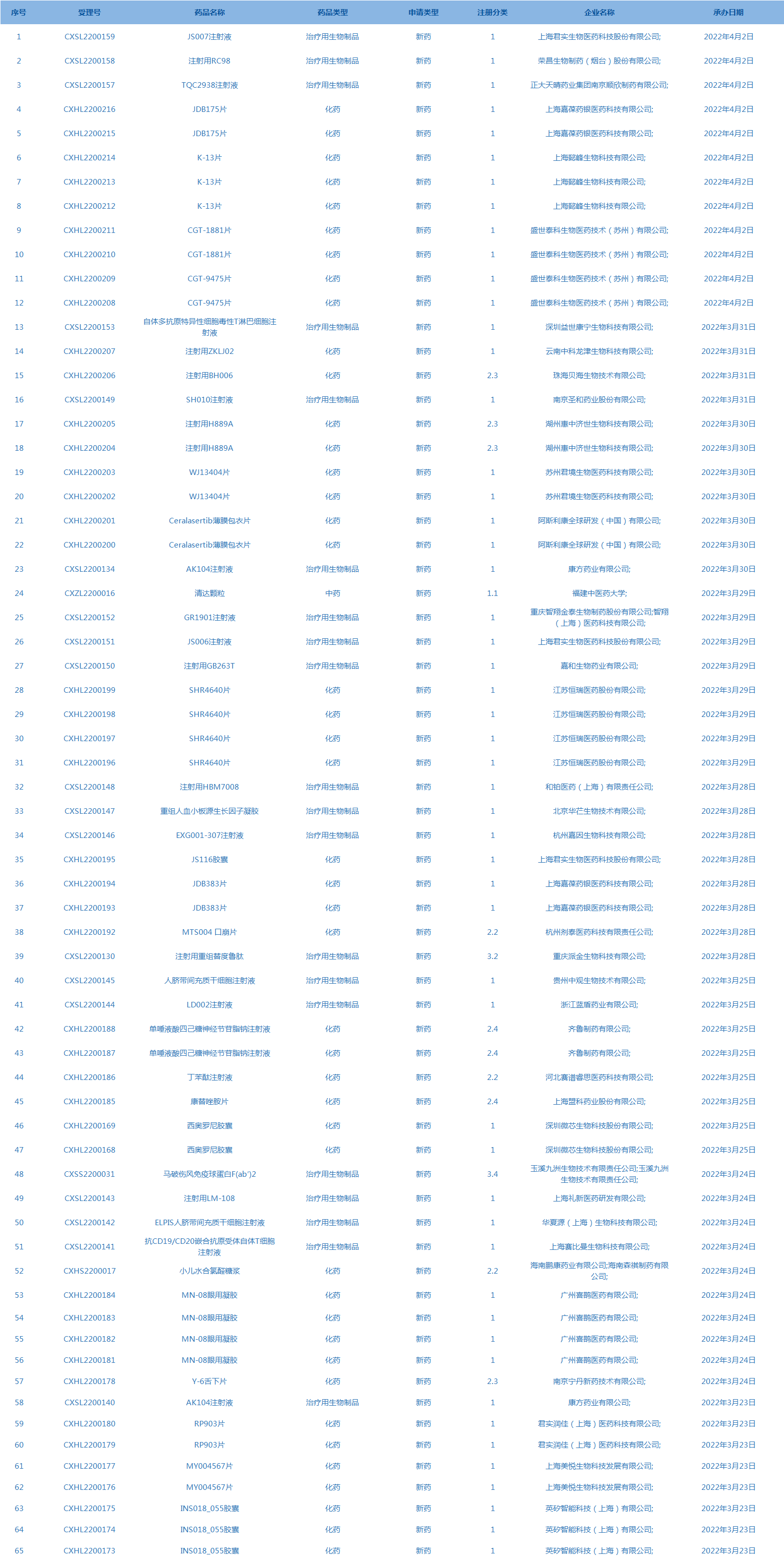
3.CDE承办受理65个新药上市申请,包括JS007注射液等药品。(截至4月5日)
4.CDE网站信息显示,DS-8201a被列入拟突破性治疗品种。(截至4月5日)

医药企业观察
1.华海药业发布公告称,其向美国FDA申报的左乙拉西坦注射液、非布司他片的新药简略申请已获得批准。
2.博瑞生物发布公告称,其产品恩替卡韦片通过了世界卫生组织的预认证(PQ)审核。
3.百凯医药宣布其靶向TROP-2的创新抗体偶联药物BIO-106的1期临床试验申请获得美国FDA批准。同日,百凯医药在美国正式启动该临床研究。
4.国药控股与腾盛博药共同宣布,国药控股与腾盛博药旗下控股公司腾盛华创医药技术(北京)有限公司达成战略合作,双方将携手推进新冠单克隆中和抗体安巴韦单抗/罗米司韦单抗联合疗法在中国的商业化进程,包括药品储备、渠道分销、医院准入及其他创新业务合作。
5.华润医药子公司华润生物医药宣布与优锐生物就精准靶向和整体免疫激活项目PTIA1在全球范围内的产品合作开发达成独家合作,并签署了合作协议。根据协议条款,华润生物医药与优锐生物将共同开发PTIA1,优锐生物负责临床前开发和新药临床试验申请(IND),华润生物医药负责临床试验、上市申请及商业化等工作。
6.劲方医药与SELLAS生命科学集团宣布达成独家授权协议,后者将作为独家合作伙伴获得劲方医药新一代高选择性CDK9小分子抑制剂GFH009注射剂在大中华区之外的全球开发和商业化权益。SELLAS公司将支付劲方医药1000万美元首付款及技术转让费,以及基于不超过3个适应症开发、累计达4800万美元的开发里程碑付款等。
7.礼来公司和信达生物宣布将深化战略合作,礼来授予信达生物在中国大陆地区进口、销售、推广和分销雷莫西尤单抗和RET抑制剂塞普替尼获批后独家商业化权利,授予信达生物享有BTK抑制剂pirtobrutinib未来在中国大陆地区商业化权利的优先谈判权。
8.博奥信生物宣布与Pyxis Oncology签订授权协议。根据协议,Pyxis Oncology将获得博奥信生物创新抗体BSI-060T除大中华区外的全球开发和商业化独家许可,博奥信生物将获得1000万美元的首付款,还将有资格收到总额达2.225亿美元的里程碑付款,以及销售额中两位数比例的特许权使用费。
9.舶望制药宣布完成超4亿元A轮融资,本轮融资由正心谷资本领投,CPE源峰、道远资本、三一创新投资等多家机构共同投资。本轮融资将主要用于推进心血管疾病和罕见病管线的新药临床试验申请,以及推进多个临床前候选药物分子的发现,这些药物将被开发治疗乙肝、自身免疫系统疾病、神经系统疾病等。
10.丹诺医药宣布完成2.64亿元人民币D轮融资。本轮融资由燕创资本和高特佳投资共同领投,星河资本、贝森资本、国联新创等跟投,获得资金将用于推进其主要产品的后期临床试验。
药品集中采购
1.山东省公共资源交易中心发布《关于公布山东省第二批(鲁晋联盟)药品集中带量采购部分中选结果的通知》。烟酰胺、倍他司汀、二羟丙茶碱三个备受关注的大产品正式公布中选价格和供货区域。
2.浙江省医保局发布《关于开展医保药品支付标准试点工作的通知》,根据药品类别,按照国家确定的规则,以通用名(含剂型)确定20个试点药品医保支付标准,全省统一执行。试点从2022年4月1日起正式实施。试点期间,如国家医保局出台关于支付标准正式文件,按正式文件精神做调整。适用的机构范围包括所有定点医疗机构和定点零售药店。
3.广东省药品交易中心发布《关于查看广东联盟双氯芬酸等药品集中带量采购(第二批)报名产品相关信息的通知》。此次涉及的品种包括血液制品、基础输液以及其他部分非独家品种,共2637个品规、208家企业符合申报要求。
4.内蒙古自治区医药采购中心发布《关于公示“八省二区”省际联盟第三批药品集中带量采购拟中选结果的通知》。此次集采涉及心脑血管疾病、呼吸系统疾病及抗生素等临床用量较大的常见病、慢病治疗药品。最终,25家企业的17个品种23个品规拟中选,平均降价54.76%,二羟丙茶碱注射剂流标。【中国食品药品网综合整理/刘思慧】
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐