抗肿瘤药物临床试验剂量选择模式转变
- 2023-12-19 09:14
- 作者:艾昆纬
- 来源:中国医药报
抗肿瘤药物研发的剂量选择模式正在经历不同以往的根本性转变。
传统剂量选择模式的目标是设定最大耐受剂量,这往往会造成额外的毒性,给受试者增加不必要的负担。同时,分子靶向疗法、免疫疗法、细胞疗法的剂量和治疗方案常常在进行临床试验前未经充分描述,从而导致整个药物研发过程的进一步低效。
为解决这一难题,美国食品药品管理局(FDA)的肿瘤卓越中心设立了Optimus项目,并于2023年1月发布了新的指南草案《治疗肿瘤疾病的人用处方药物和生物制品的剂量优化》。该项目旨在推动药物研发从以药物为中心转变为以患者为中心,更好地指导剂量选择,并最大限度地改善患者结局。
传统的剂量模式
癌症是一种毁灭性的疾病,已经折磨人类千年之久,可是直到上个世纪,人类才研发出比较有效的治疗方法来抗击癌症。20世纪40年代,氮芥问世,标志着人类为抗癌付出的努力迎来了希望曙光,开启了为期50多年的由化疗药物推动的抗癌药物研发模式。这种策略的基础是,癌细胞在分裂和生长时缺乏调控,这意味着有细胞毒性的化学疗法可以引发癌细胞损伤和杀死癌细胞。然而,这一治疗方法会导致健康细胞同样受到伤害,引起毒性反应。
为了平衡疗效和安全性,医生通常会按期开展化疗,并设置间断期。这些间断不仅可以帮助患者缓解即时的副作用,也可以让临床医生进一步控制和避免在治疗结束后化疗仍可能产生的长期毒性。
安全性指标是肿瘤学试验的支柱,推动了研究者对最大耐受剂量的探寻。但是究竟由哪些因素构成了“剂量限制性毒性”?关于这个问题众说纷纭,只能交由临床医生决定如何更好地权衡疗效与风险。一些治疗原则表明,疗效与药物功效和副作用均有关联,这使得医生难以作出决定。
抗癌药物获批后进行“剂量优化”时,往往要依靠后续临床试验和观察数据来改善治疗方案。例如,2018年公开的一项研究成果显示,转移性乳腺癌及卵巢癌患者的生存率降低可能与化疗药物剂量的调整有关,强调对于临床试验方案之外的剂量调整需要审慎思考。在多种靶向药获批后进行的上市后临床试验中,也进行过此类观察。
剂量模式的转变
如今,科学家对癌症的理解已经深入了许多。过去,人们仅仅依靠有毒的化疗药物,并认为随着剂量增加,疗效也会增加,直到达到最大的毒性;现在,以特定的细胞途径为靶标的新药不断被研发问世。研究发现,对于这些新疗法来说,剂量与疗效的关系与以前不尽相同。
例如,某个PI3K抑制剂药物基于单臂试验结果获批上市,用于治疗滤泡型淋巴瘤和慢性淋巴细胞白血病。在临床试验中,药物剂量被设定为最大耐受剂量或者接近最大耐受剂量。然而,研究者在该药物上市后随访研究中发现了过量毒性,并对总生存率产生了令人担忧的影响,最终该药物的前述适应证被撤销。
近期,在一篇由FDA专家发表的文章中指出:“通过随机‘剂量探寻’试验来查明总体反应率与不良事件之间的关联,就有可能避免选择毒性过大的剂量以及由其导致的令人担忧的疗效和总体生存率。”同时,FDA建议,申办者在启动临床试验之前,需要先在随机试验中分析剂量反应关系并进行安全性评估。
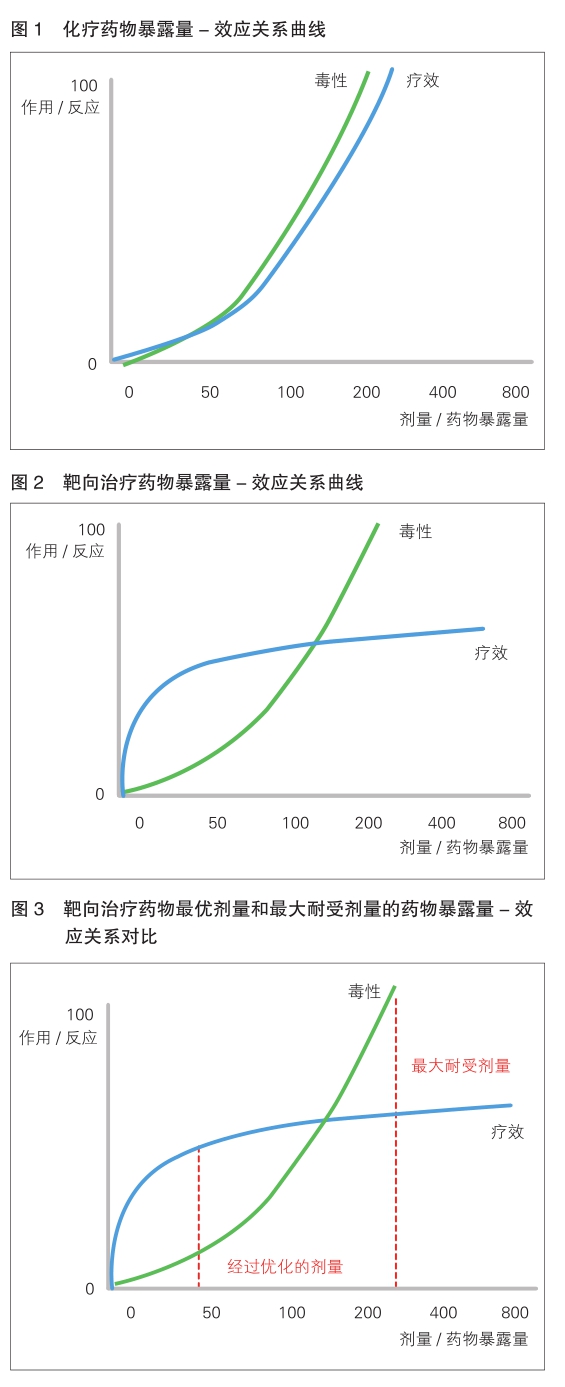
多年以来,传统的有细胞毒性的化疗一直坚持 “越多越好”的理念(详见图1)。可随着时代的改变和多种新型疗法的出现,检测结果显示,最优剂量可能远低于最大耐受剂量,即具有相当的疗效但毒性显著降低。
如今,激酶抑制剂、单克隆抗体、抗体药物偶联物以及其它类型的疗法呈现出不一样的疗效与毒性关系曲线,与传统的曲线差异巨大(详见图2)。
随着毒性的增加,通常会出现一个“疗效平台”,最优剂量可能远低于最大耐受剂量(详见图3)。这些不同于以往的暴露-反应曲线特征是很多新型疗法的剂量选择标准需要改变的根本原因之一,有细胞毒性的化疗药物也是如此。
在早期试验中纳入更多数据
剂量对于药物疗效至关重要,FDA要求申办方提供详细的数据以便进行最优的选择。为了满足这些标准,申办方必须根据血清样本来识别药代动力学的暴露量,并通过剂量调整或者根据治疗引起的不良反应等,来关注耐受性方面的潜在风险。
此外,早期临床试验可能需要更多类型的数据,比如以下几个方面的数据。
根据患者报告结局(PRO)得到的数据 在卫生健康评估中,患者反馈日益成为一种极具价值的资产,FDA已支持把患者报告结局用于药品的上市审批。患者权益倡导者表示,中断给药或减少剂量会对患者生理健康造成负面影响,因为这会加重患者对于治疗是否有效的焦虑,因此他们认为需要采用更可耐受的、更有益于健康的剂量。
在早期临床试验中,“剂量优化”是一个极具价值的步骤。提前把“患者报告结局”数据纳入临床试验设计中,有利于找到更有效的剂量,在改善患者治疗结果的同时又不会增加患者负担。
其实,FDA在《治疗肿瘤疾病的人用处方药物和生物制品的剂量优化》中已经写明:“患者报告结局可以系统、定量地评估可能的不良症状以及药物对身体机能的影响。应考虑把患者报告结局纳入进来,以完善早期‘剂量探寻’试验中的耐受性评估。”
采用多个数据集进行建模和模拟 为了增加在试验中成功找到最优剂量的机会,可以采用多个数据集进行建模和模拟,它们可以提供关键的见解,精准定位理想剂量。该做法的目标是尽可能提高总体反应率等疗效指标,并评估“靶标抑制”和“受体占位”等来自PD生物标志物的辅助证据。如果有投资早期研发资源的可能,可以在“剂量扩展”之前采用“剂量优化”,这可以帮助申办方尽早找到理想剂量,再根据其特有的作用机理扩展到不同的适应证。
与监管方进行早期沟通 为了确保药物研发成功,申办方必须与FDA和其他监管方进行有效沟通,详细说明“剂量优化”设计,包括其关键终点。可以将“临床前数据”作为依据,证明药物适用于特定人群的适应证。申办方还必须解释说明这些“临床前数据”。通过主动把“早期优化”纳入其策略中,申办方可以与监管机构持续对话,更快地达成共同期望的结果。
“剂量优化”以实现更好的临床结果
过去,癌症治疗的目标是尽可能减少三级和四级毒性。现在则需要更精确的方法——能同时兼顾患者体验和毒性水平。
采用精巧的ePRO(电子“患者报告结局”)评估工具可以帮助研究者实现这一点,它有助于微调剂量,同时也保证患者维持尽可能高的生活质量。
早期肿瘤学临床试验中推动“剂量优化”的基本因素之一是患者数量的增加。目前来看,申办方很可能需要花更长的时间来招募这些患者。因此,申办方必须准备好承担额外的时间成本,或者想办法让更多患者参加这些早期试验。
这也意味着申办方需记住以下要素。
以患者为中心 为患者提供更便利的试验选择,这对于招募患者有一定作用,减轻参加者负担则是其中的重要组成部分。如将需要患者长途跋涉来采集的用药后PK样品,改为让他们轻松在家检测,招募效果将大不相同。
增加入选患者的多样性 申办方可以通过尽早增加投资,扩大各类患者群体,来获得有价值的安全性信息,这些安全性信息对于药物将来的研发和注册极具价值。
及早考虑复杂性 治疗方案的另一难点在于,多种剂量强度需要在不同剂量级别的患者群中实现。部分“剂量优化”患者群会涉及到多种不同的疗法,包括研究性产品和其它组合疗法。所以,申办方必须向患者科普他们所需的知识,让患者安心,这样患者才能正确、按时进行联合治疗。即使是一粒药丸服用时间错误,都可能影响后果评估,干扰安全性信息的检测。因此,有效的宣教辅助体系有利于顺利开展工作。
综上,随着抗肿瘤药物应该“更精确”的研发观点的诞生,研究者明显需要更稳健可靠、更有理有据的剂量选择方法推动抗肿瘤药物发展和进步,申办方、患者和研究团队等各方也都需要理解这种新模式的意义。 (艾昆纬供稿)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:陆悦)
分享至
右键点击另存二维码!
-
为你推荐