图说政策:《医疗器械不良事件监测和再评价监督管理办法》(七)
作者: 国家药品监督管理局
来源: 国家药品监督管理局
2018-11-09
《医疗器械不良事件监测和再评价管理办法》自2019年1月1日起施行,全文共80条,包括总则、职责与义务、报告与评价、重点监测、风险控制、再评价、监督管理、法律责任、附则九部分内容。下面我们将分八篇逐步进行解读。
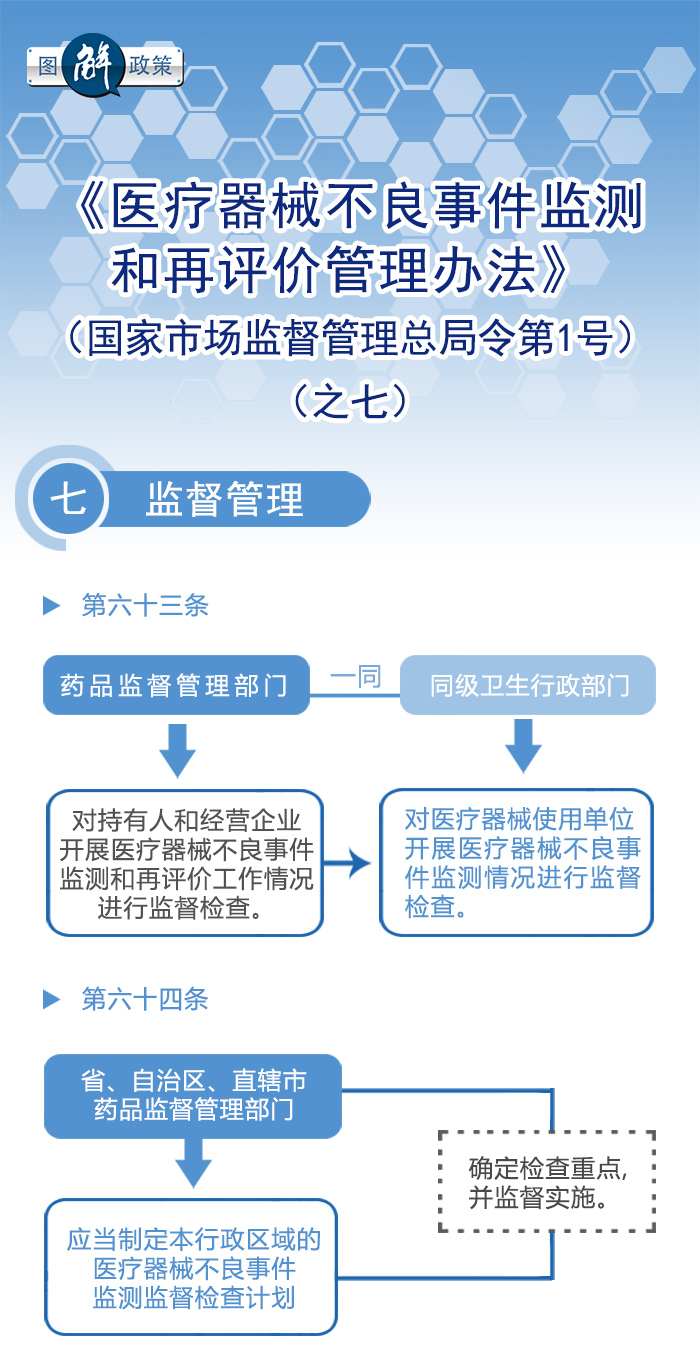
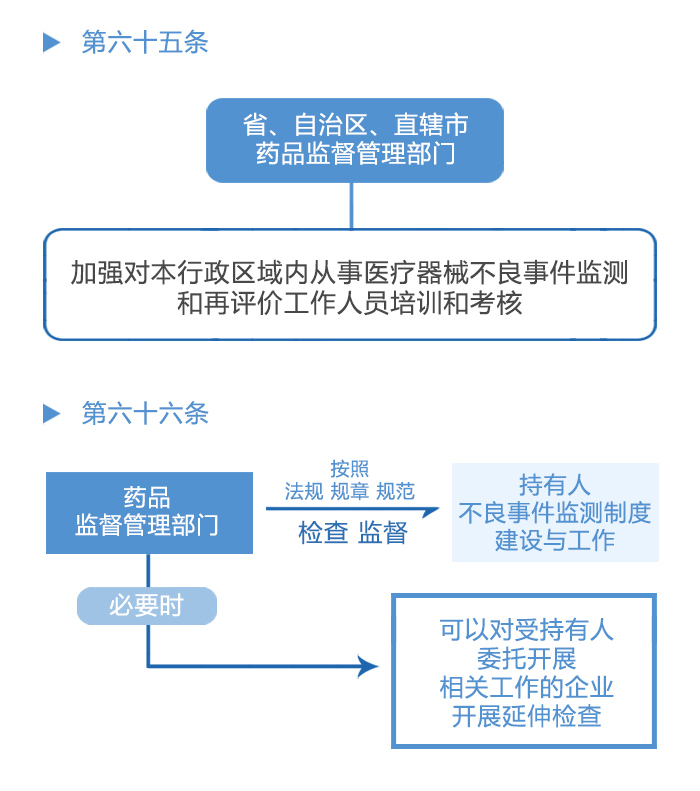
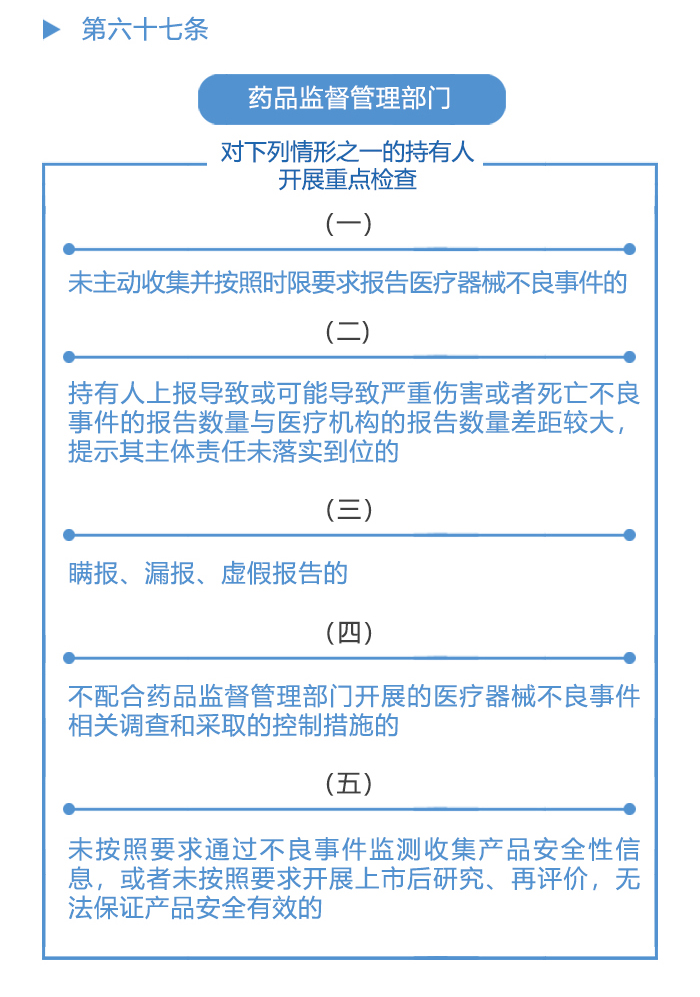


《医疗器械不良事件监测和再评价管理办法》自2019年1月1日起施行,全文共80条,包括总则、职责与义务、报告与评价、重点监测、风险控制、再评价、监督管理、法律责任、附则九部分内容。下面我们将分八篇逐步进行解读。




