23家企业生产的25批(台)医疗器械不合格 欧姆龙电子血压计再上榜
中国食品药品网讯(记者 李硕) 5月5日,国家药监局发布《关于发布国家医疗器械监督抽检结果的通告》。通告显示,国家药监局对电子血压计、一次性使用医用口罩、医用X射线防护用具(防护衣、裙、围脖等)、人体血液及血液成分袋式塑料容器(血袋)等7个品种共151批(台)的产品进行质量监督抽检,欧姆龙(大连)有限公司等23家企业生产的25批(台)产品不符合标准规定。
被抽检项目为标识标签、说明书等项目不符合标准规定的医疗器械产品,涉及7家企业的2个品种7批(台)。
7批(台)抽检(标识标签说明书等项目)不合格产品名单
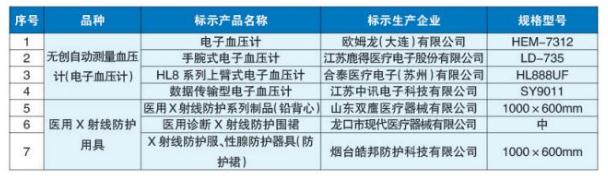
一是无创自动测量血压计(电子血压计)4家企业4台产品不符合标准规定。其中,作为知名跨国企业,标示为欧姆龙(大连)有限公司生产的1台电子血压计(型号HEM-7312,批号201801L,出厂编号20180103173LG)标识不合格,这是继今年2月份抽检被发现其生产的1台电子血压计(型号HEM-8611,批号201804L,出厂编号20180407322LF)存在“泄气”和“标识不合格”问题以来,该公司第二次被列入国家药监局医疗器械抽检不合格名单。另外,标示为江苏鹿得医疗电子股份有限公司生产的1台手腕式电子血压计、合泰医疗电子(苏州)有限公司生产的1台HL8系列上臂式电子血压计、江苏中讯电子科技有限公司生产的1台数据传输型电子血压计,标识要求也不符合标准规定。
二是医用X射线防护用具(防护衣、裙、围脖等)3家企业3批次产品标记不符合标准规定。它们是标示为山东双鹰医疗器械有限公司生产的1批次医用X射线防护系列制品(铅背心)、龙口市现代医疗器械有限公司生产的1批次医用诊断X射线防护围裙、烟台皓邦防护科技有限公司生产的1批次X射线防护服、性腺防护器具(防护裙)。
被抽检项目不符合标准规定的医疗器械产品,涉及17家企业的6个品种19批(台)。
19批(台)抽检不符合标准规定产品名单
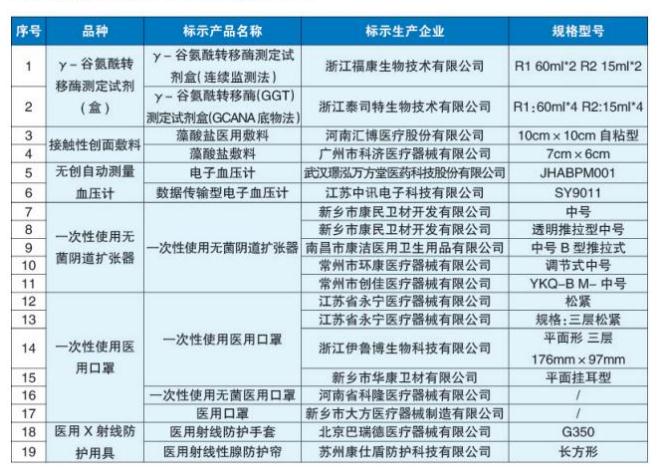
一是γ-谷氨酰基转移酶测定试剂(盒)2家企业2批次产品。涉及标示为浙江福康生物技术有限公司生产的1批次γ-谷氨酰转移酶测定试剂盒(连续监测法)、浙江泰司特生物技术有限公司生产的1批次γ-谷氨酰转移酶(GGT)测定试剂盒(GCANA底物法),线性不符合标准规定。
二是接触性创面敷料2家企业2批次产品酸碱度试验不符合标准规定,涉及标示为河南汇博医疗股份有限公司生产的1批次藻酸盐医用敷料、广州市科济医疗器械有限公司生产的1批次藻酸盐敷料。
三是无创自动测量血压计(电子血压计)2家企业2台产品。标示为武汉璟泓万方堂医药科技股份有限公司生产的1台电子血压计,最大袖带压、可重复性、压力传感器准确性不符合标准规定;标示为江苏中讯电子科技有限公司生产的1台数据传输型电子血压计,指示灯的颜色不符合标准规定。
四是一次性使用无菌阴道扩张器4家企业5批次产品。标示为新乡市康民卫材开发有限公司生产的2批次、南昌市康洁医用卫生用品有限公司生产的1批次一次性使用无菌阴道扩张器,环氧乙烷残留量不符合标准规定;标示为常州市环康医疗器械有限公司生产的1批次一次性使用无菌阴道扩张器,抗变形能力不符合标准规定;标示为常州市创佳医疗器械有限公司生产的1批次一次性使用无菌阴道扩张器,结构强度不符合标准规定。
五是一次性使用医用口罩5家企业6批次产品。标示为江苏省永宁医疗器械有限公司生产的2批次一次性使用医用口罩,口罩带、细菌过滤效率(BFE)不符合标准规定;标示为浙江伊鲁博生物科技有限公司生产的1批次一次性使用医用口罩、新乡市华康卫材有限公司生产的1批次一次性使用医用口罩、河南省科隆医疗器械有限公司生产的1批次一次性使用无菌医用口罩,细菌过滤效率(BFE)不符合标准规定;标示为新乡市大方医疗器械制造有限公司生产的1批次医用口罩,微生物指标不符合标准规定。
六是医用X射线防护用具(防护衣、裙、围脖等)2家企业2批次产品。标示为北京巴瑞德医疗器械有限公司生产的1批次医用射线防护手套,材料不符合标准规定;标示为苏州康仕盾防护科技有限公司生产的1批次医用射线性腺防护帘,设计不符合标准规定。
《中国医药报》社版权所有,未经许可不得转载使用。

















