强生或为这款药付出80亿美元赔偿代价,国内电商平台还在卖!
- 2019-10-16 16:39
- 作者:蒋红瑜
- 来源:中国食品药品网
中国食品药品网讯(记者蒋红瑜) 近日,美国费城一个陪审团裁决,强生必须向一名男子支付80亿美元的惩罚性损害赔偿金。这位名叫尼古拉斯·默里(Nicholas Murray)的男子因使用强生旗下杨森制药的抗精神病药物利培酮(Risperdal)导致乳腺增生,此前已获68万美元补偿性赔偿。
这是宾西法尼亚州审理的数千起利培酮相关案件中判给惩罚性赔偿的第一起案件。陪审团在裁决中指出,强生未能警告使用利培酮可能引发男性乳腺增生的风险。强生对此判决表示不服,称这“与最初的补偿性赔偿金严重不符,公司相信这一裁决将被推翻”。该公司补充称,此案中的陪审团未被允许听取有关利培酮的好处的证据。
记者查询到国内药企也有生产利培酮。在PC端京东电商平台上搜索利培酮片,结果显示有多家药企品牌的利培酮片在售卖,如西安杨森制药有限公司(强生的制药子公司)的维思通利培酮片、浙江华海药业股份有限公司的索乐利培酮片等。
利培酮可否在电商平台售卖?
新修订《药品管理法》第六十一条规定,药品上市许可持有人、药品经营企业通过网络销售药品,应当遵守本法药品经营的有关规定。具体管理办法由国务院药品监督管理部门会同国务院卫生健康主管部门等部门制定。
疫苗、血液制品、麻醉药品、精神药品、医疗用毒性药品、放射性药品、药品类易制毒化学品等国家实行特殊管理的药品不得在网络上销售。
记者查阅得知,利培酮为处方药,用于治疗急性和慢性精神分裂症。特别是对阳性及阴性症状及其伴发的情感症状(如焦虑、抑郁等)有较好的疗效。也可减轻与精神分裂症有关的情感症状。对于急性期治疗有效的患者,在维持期治疗中,该药可继续发挥其临床疗效。
10月14日,记者在移动端京东平台上搜索利培酮,结果显示,“抱歉!暂无相关商品。”但是在PC端登录京东,却发现有西安杨森制药有限公司的维思通利培酮片、浙江华海药业股份有限公司的索乐利培酮片等多款品牌在售。以西安杨森制药有限公司的维思通利培酮片为例,药品页面详情显示,“该药品必须凭处方预约!加入药品清单立即预约,上传处方或问诊获取电子处方一健购药”。记者依据网站的指导,点击“加入药品清单”键,该页面显示,2~6天可以发货,之后填写了购买人和用药人信息,且并未上传处方电子照片,最后进入预约程序。在“药品清单键”下方,有温馨提示,“本品为处方药,请凭处方购买;jkcsjd.com只对处方药品作信息展示,不提供交易·药品监管部门提示:如发现本网站有任何直接或变相销售处方药行为,请保留证据,拨打12331举报。
之后,记者在健客、爱康多等电商平台同样看到有多个品牌的利培酮在售卖。
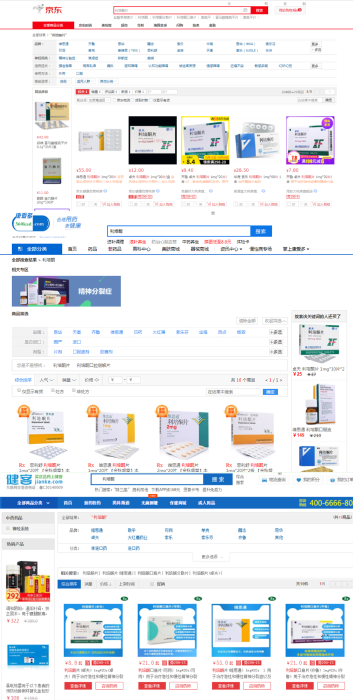
图为京东、健客、爱康多等电商平台截图。
10月15日,记者接到京东客服的电话,表示需要记者上传正规的处方电子照片,才可以发货。记者询问何谓“正规”?对方表示,正规处方指的是有医院的抬头、有医生的签名、开处方的时间是否在有效期之内,之后通过审核确认之后,就可以发货了。
江苏省南通市市场监管局副调研员缪宝迎认为,按照新修订的《药品管理法》,除实行特殊管理的药品不得通过网络销售外,其它类别药品(包括处方药)是允许进行网络销售的。但必须是在今年12月1日新修订《药品管理法》实施之后,且目前还没有制定与新法配套的实施细则。
近年来,强生产品安全性广受关注。今年9月,英国药监机构MHRA发布消息显示,强生特定批次的安视优日抛隐形眼镜可能含有颗粒物擦伤眼角膜,或给眼球造成伤害,强生也正在召回相关产品。8月,强生(中国)有限公司在一则声明中表示已经收到美国司法部的传票。此声明源于美国司法部正在对强生公司是否故意隐瞒婴儿爽身粉里含有潜在致癌物质(石棉)的事实展开的刑事调查。
国家对利培酮的不良反应早有警示
记者查询国家药品监督管理局药品评价中心(国家药品不良反应监测中心)官网发现,输入“利培酮”检索结果显示,有27篇文章。其中药品警戒快讯有12篇,最早的是2008年第8期(总第57期),最新的是2018年第5期(总第181期)。
药品警戒快讯2018年第5期(总第181期)显示,加拿大卫生部决定对所有已上市的非典型抗精神病药的DRESS(潜在的嗜酸性粒细胞增多症及全身症状的药物反应)风险开展评估。DRESS描述了一组罕见但严重危及生命的潜在副作用,包括发热、严重皮疹、面部肿胀或全身大面积的皮肤脱落等。这些反应通常在开始服用药物后2周到2个月发生。
该项安全性评估也包括43例境外DRESS报告,其中只有11例报告的临床表现符合DRESS的定义。这11例报告中,包括2例利培酮报告。加拿大卫生部对已有的信息进行了评估,评估结论认为包括氯氮平、喹硫平、利培酮、阿立哌唑、帕利哌酮及鲁拉西酮在内的其他6种非典型抗精神病药与DRESS之间可能存在关联。加拿大卫生部将与生产企业共同合作对这6种非典型抗精神病药的药品安全性信息进行更新以提示DRESS风险。
药品警戒快讯2015年第3期(总第143期)显示,2015年2月19日,加拿大卫生部与杨森公司(Janssen Inc.)共同发布信息,要求限制利培酮的部分适应症,并修订了药品说明书。
此外,检索结果显示,美国、法国、澳大利亚和欧盟等国家和地区的药品监管部门都曾发表过利培酮的相关风险警示。
2010年4月,欧洲药品管理局药物警戒工作组(PhVWP)对抗精神病药品引起静脉血栓栓塞的风险进行了评估。PhVWP认为不能排除抗精神病药和静脉血栓栓塞之间的关联性,但也无法区分各种药物所出现的不同程度的风险。根据评估结果,PhVWP建议药品信息中应包括对抗精神病药引起静脉血栓栓塞(包括肺栓塞和深层静脉栓塞)的病例表述,并说明在治疗之前和期间应注意识别静脉血栓栓塞发生的风险因素,并采取适当的预防措施。PhVWP的建议适用的药物包括利培酮。
同时,在2015年3月30日,国家药品不良反应监测中心发布的《药品不良反应信息通报(第68期)关注非典型抗精神病药的严重不良反应》显示,目前我国上市的非典型抗精神病药包括:氯氮平、利培酮等。非典型抗精神病药的不良反应主要表现为中枢神经系统反应,如头晕、嗜睡、失眠、癫痫、锥体外系反应、激越、狂躁、谵妄等。此外还有一些严重不良反应,如粒细胞缺乏症、糖脂代谢异常。为充分了解此类药品的安全性,指导临床合理用药,降低用药风险,特发布本期药品不良反应信息通报。
该通报建议,药品生产企业对于非典型抗精神病药潜在的严重风险应予以高度重视,采取积极、有效的风险控制措施,保障患者的用药安全。应加强药品不良反应监测及分析评价工作,对于说明书中风险提示不足的,应及时修订和完善,并应采取有效途径,加大与医务人员和患者的沟通与交流,及时传递最新药品安全信息。
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:郭厚杰)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐
-

-

互联网新闻信息服务许可证10120170033
网络出版服务许可证(京)字082号
©京公网安备 11010802023089号 京ICP备17013160号-1
《中国医药报》社有限公司 中国食品药品网版权所有










