2023年度医疗器械注册工作报告数据透视
- 2024-03-12 16:20
- 作者:
- 来源:中国食品药品网

近日,国家药监局发布《2023年度医疗器械注册工作报告》(以下简称《报告》),本文将结合2021、2022年的报告,梳理近三年我国的医疗器械注册情况。
第三类医疗器械受理、批准数量逐年增长
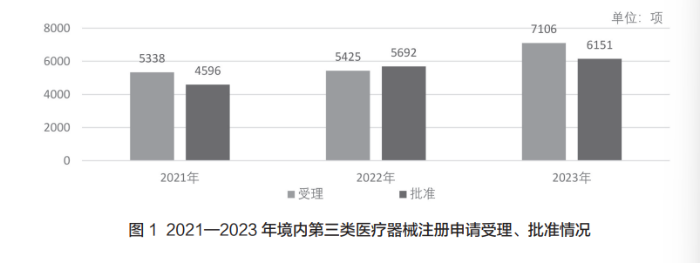
如图1所示,2021—2023年我国境内第三类医疗器械注册申请受理和批准数量均逐年增长。2023年,国家药监局共受理境内第三类医疗器械注册申请7106项,同比增长31.0%,增长幅度较大。其中,医疗器械注册申请5432项,体外诊断试剂注册申请1674项。共批准境内第三类医疗器械注册申请6151项,同比增长8.1%,其中,医疗器械4667项,体外诊断试剂1484项。
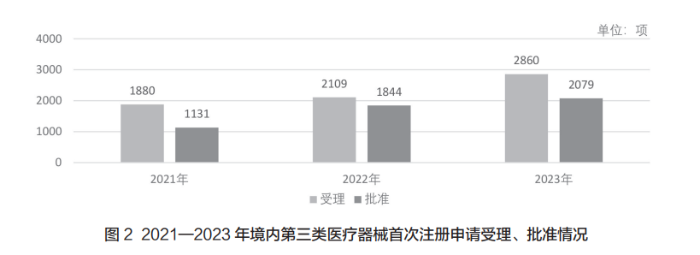
如图2所示,2021—2023年我国境内第三类医疗器械首次注册申请受理和批准数量同样均实现逐年增长。2023年,国家药监局共受理境内第三类医疗器械首次注册申请2860项,同比增长35.6%,增长幅度较大。共批准境内第三类医疗器械首次注册申请2079项,同比增长12.7%。
第二类医疗器械批准数量增长 第一类医疗器械备案数量减少
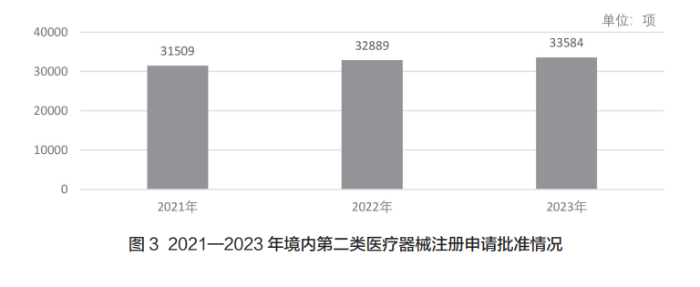
如图3所示,2021—2023年我国境内第二类医疗器械注册申请批准数量逐年增长。2023年,各省级药品监管部门共批准境内第二类医疗器械注册申请33584项,同比增长2.1%。
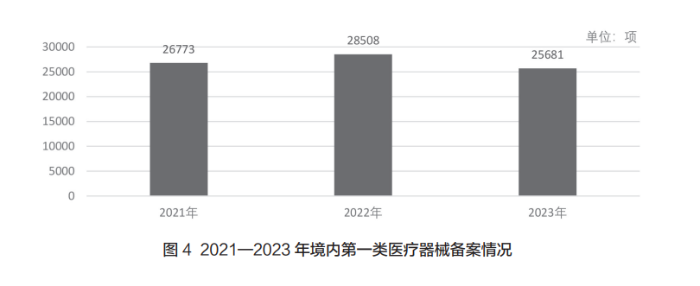
近年来,国家药监局持续规范第一类医疗器械备案工作,加强监督指导。2021—2023年我国境内第一类医疗器械备案情况如图4所示,2022年较2021年有所增长。2023年全国设区的市级药品监管部门共办理境内第一类医疗器械备案25681项,同比减少9.9%,数量有所下降。
进口医疗器械批准数量逐年减少
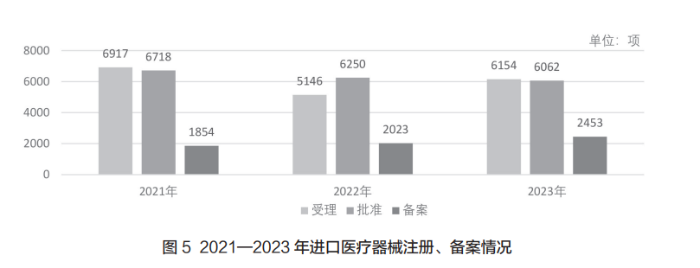
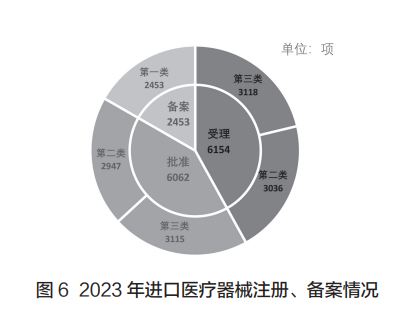
如图5、6所示,2021—2023年进口医疗器械注册申请受理数量在2022年出现明显下降,2023年国家药监局共受理进口医疗器械注册申请6154项,同比增长19.6%,数量有所回升,包括第三类进口医疗器械注册受理3118项和第二类进口医疗器械注册受理3036项。
2021—2023年进口医疗器械注册申请批准数量逐年减少,2023年国家药监局共批准进口医疗器械注册申请6062项,同比减少3.0%,包括第三类进口医疗器械注册申请3115项和第二类进口医疗器械注册申请2947项。
2021—2023年进口医疗器械备案数量逐年增长,2023年国家药监局共办理第一类进口医疗器械备案数量2453项,同比增长21.2%。
保障疫情防控工作
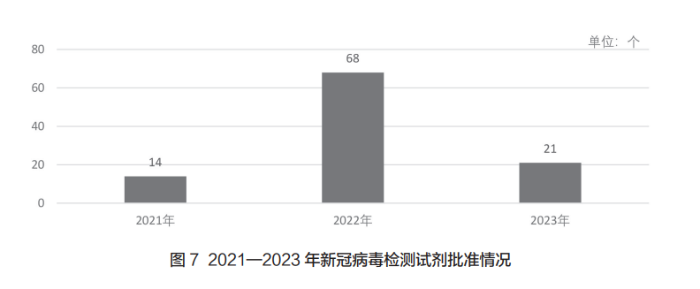
如图7所示,2021—2023年国家药监局均将疫情防控作为重要政治任务,审批多个产品保障人民群众生命健康。其中,2022年共68个新冠病毒检测试剂获批,为三年来最多。2023年,新冠疫情进入常态化防控阶段,国家药监局共批准新冠病毒检测试剂21个,并应急批准3个国产体外膜肺氧合系统(ECMO)上市,助力疫情防控“保健康、防重症”目标落实。
创新医疗器械逐年增长
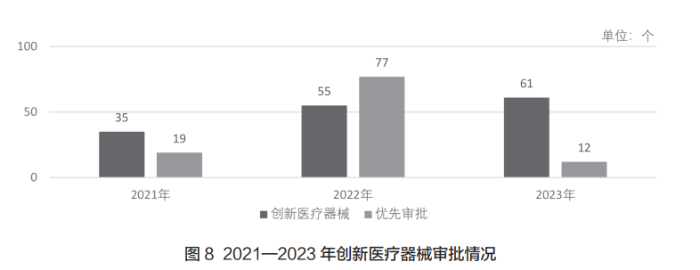
如图8所示,2021—2023年获批创新医疗器械数量逐年增长。2023年,国家药监局共批准创新医疗器械61个,同比增长10.9%,并优先审批医疗器械12个。
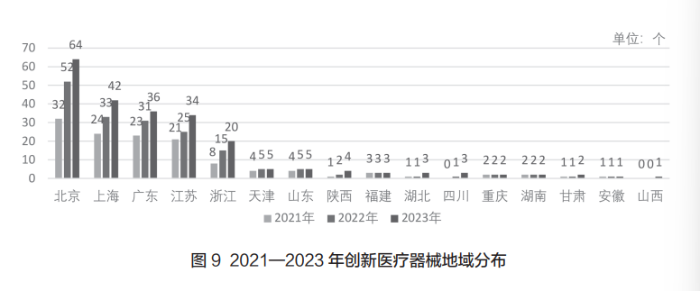
如图9所示,截至2023年底,我国共有250个创新医疗器械获批上市,其中,境内创新医疗器械涉及16个省的167家企业。2023年,北京市共有64个创新医疗器械获批上市,连续三年排名第一;上海市、广东省、江苏省和浙江省排名依次紧随其后,获批上市的创新医疗器械数量均超过10个;2023年8月28日,山西锦波生物医药股份有限公司的注射用重组Ⅲ型人源化胶原蛋白溶液获国家药监局批准上市,实现了山西省创新医疗器械零的突破。
京津冀、长三角、粤港澳大湾区等重点建设区域,创新医疗器械获批上市的数量较多,长三角区域中,上海市、江苏省、浙江省、安徽省均有创新医疗器械获批上市,数量分别为42个、34个、20个、1个;京津冀地区中,北京市和天津市有创新医疗器械获批上市,分别为64个和5个;粤港澳大湾区中,广东省共36个;福建省共3个;海南自由贸易港暂无创新医疗器械获批上市。
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:宋莉)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐
-

-