又获批4个!获批上市的新冠病毒检测产品增至14个
- 2020-03-01 20:59
- 作者:胡芳
- 来源:中国食品药品网
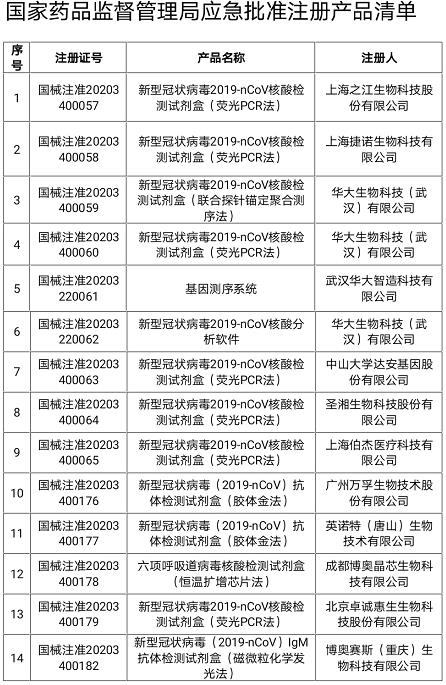
中国食品药品网讯(记者胡芳) 近日,国家药品监督管理局应急审批通过3家企业4个新型冠状病毒检测产品,包括2个化学发光法抗体检测试剂、2个荧光PCR法核酸检测试剂,进一步丰富了新型冠状病毒的检测方法,扩大了检测试剂的供应,全力服务疫情防控需要。
新冠肺炎疫情发生后,国家药监局迅速启动医疗器械应急审批程序,按照“统一指挥、早期介入、随到随审、科学审批”的原则和确保产品安全、有效、质量可控的要求,全力加快审评审批速度。此前,国家药监局已批准7家企业7个新型冠状病毒核酸检测产品(共9个注册证,表格中3、5、6配套使用)。
第一批应急审批医疗器械陆续获批后,国家药监局继续推动第二批医疗器械应急审批工作,应急审批的产品包括抗体类检测试剂、核酸荧光PCR检测试剂,以及其他方法学产品。
2月22日,国家药品监督管理局再次应急审批通过3家企业3个新型冠状病毒检测产品,包括2个胶体金法抗体检测试剂、1个恒温扩增芯片法核酸检测试剂,扩大了新型冠状病毒的检测方法和手段。
截至目前,国家药监局共批准新冠病毒核酸检测试剂10个,抗体检测试剂4个。
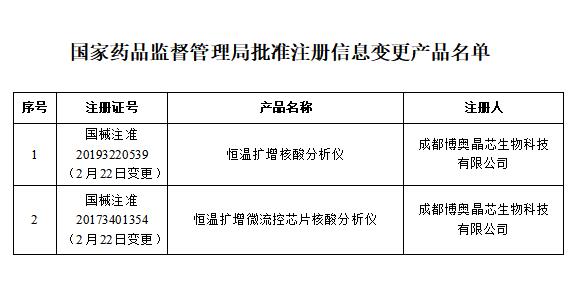
2月22日,国家药监局还批准了2个仪器设备变更文件,以配合相关产品使用。
国家药监局将根据疫情发展情况,继续做好相应产品应急审批工作。
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:李硕)
分享至
×
右键点击另存二维码!
网民评论
欢迎
登录
-
为你推荐
-

-

助解实操问题 助推新规落地 业界热议国家药监局药品经营监管新政
日前,国家药监局发布《关于进一步做好药品经营监督管理有关工作的公告》,围绕今年1月1日起施行的《药品经营和使用质量监督管理办法》,明晰实施标准和细化要求。 2024-05-06 16:18