一周法治播报(5.3~5.9)
- 2021-05-11 14:06
- 作者:陆悦
- 来源:中国食品药品网
“一周法治播报”来了!以下是5月3日~5月9日,各省级药监部门的法治动态。
政策文件
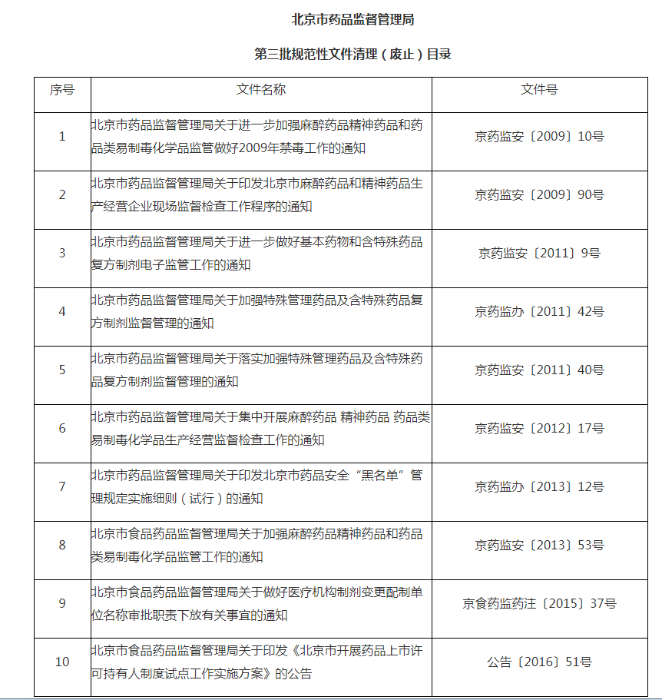
1.北京市药品监督管理局发布第三批规范性文件清理结果的公告,废止《北京市开展药品上市许可持有人制度试点工作实施方案》等10个规范性文件。
2.安徽省药品监督管理局发布《安徽省药品上市后变更备案管理工作程序(试行)》,对由省级药监部门负责实施的药品上市后备案类变更程序予以明确。工作程序为:持有人通过国家药监局网上办事大厅药品业务应用系统(以下简称业务系统)进行备案,提交备案资料;省局通过业务系统对持有人备案资料进行签收,对不属于备案类变更,不予签收并说明理由;对于签收的备案类变更,省局自签收之日起5日内对备案信息进行核对并予以公示;对需要进行资料审查的备案类变更,签收当日转省药品审评查验中心,在20日内对备案资料完成审查;必要时,依据审查及风险原则决定是否进行现场检查及抽样检验。审查结束后,省药品审评查验中心及时将审查意见报省局审核,省局在10日内作出审核结论。
3.新疆维吾尔自治区药品监督管理局发布关于医疗机构制剂注册及民族药制剂调剂使用相关事权调整的公告,明确由区药监局全面负责全区医疗机构制剂注册及调剂使用管理工作,各地(州、市)市场监督管理局(药品监管部门)不再对辖区内医疗机构制剂注册申报行使受理、现场考察、抽样检验事权以及民族医医疗机构制剂调剂使用签署意见的事权。
标准制定
4.山西省药品监督管理局公示第一批山西省中药配方颗粒质量标准,涉及白茅根、布渣叶、川楝子、大蓟、麸炒山药、红景天、罗汉果、拳参、山药、仙鹤草、小蓟等11种中药。为确保标准的科学性、合理性和适用性,该批质量标准公示15天。
5.四川省药品监督管理局发布《四川省中药配方颗粒质量标准制定工作程序及申报资料要求(试行)》,旨在规范该省中药配方颗粒标准研究申报、技术审评、复核检验及制定发布等工作。对于制定标准的品种提出四点要求:相应品种国家尚未公布标准;研究应按照《中国药典》《中药配方颗粒质量控制与标准制定技术要求》《四川省中药饮片标准研究技术指导原则》等开展;对应的中药材、中药饮片符合现行版《中国药典》、其它国家标准或省级中药材、中药饮片标准规定,对应的中药材、中药饮片如无法定标准的,应先申报省级中药材及饮片标准;对应的中药材、中药饮片同时收载于多省(市、区)地方标准中,省内企业、单位宜优先采用四川省中药材及饮片标准开展相应配方颗粒研究。
监督检查
6.广东省药品监督管理局在全省范围部署开展药品网络销售违法违规行为专项整治行动,专项整治按照“线上线下一致”原则,聚焦三项检查重点,以严厉打击药品网络销售违法违规行为。
7.四川省药品监督管理局发布通告显示,在2020年化妆品监督抽检中,经四川省药品检验研究院检验,发现涉及染发类不合格化妆品1批次,为标识为广州市凯维斯化妆品有限公司生产的凯维斯染发膏(葡萄酒红);标示为广州市艾娜斯化妆品有限公司生产的苾美斯染发膏(自然黑色)、标识为广州俪凝化妆品有限公司生产的俪缇染发膏(葡萄酒红)、委托方为杭州莫诺生物科技有限公司的洛洛森林婴幼儿接骨木修护精华霜等3批次化妆品不合格,经标示生产企业属地市场监管部门调查核实为假冒化妆品。(中国食品药品网综合整理/陆悦)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:陆悦)
分享至
右键点击另存二维码!
-
为你推荐
-

以律为舟,谋定而后动—— 医药企业出海新兴市场的九大考量
全球医药市场格局正在重塑,我国医药企业依托创新积淀与成本优势,正以前所未有的规模和速度扬帆出海。全球新兴市场的巨大增量空间、资本青睐的国际合作契机,为我国医药企业出海开辟了价值跃升... 2026-01-27 09:10 -

依案说法|实际销售软件产品与注册证信息不一致,如何处罚?
2025年12月,A市药监部门依据《条例》第八十六条规定,对B公司生产经营与实际注册信息不符产品的行为,作出没收违法所得,并处罚款;并责令立即停止销售涉案产品,对已销售产品实施召回的处罚决... 2026-01-27 09:05
互联网新闻信息服务许可证10120170033
网络出版服务许可证(京)字082号
©京公网安备 11010802023089号 京ICP备17013160号-1
《中国医药报》社有限公司 中国食品药品网版权所有