GVP逐条谈 | 77.“完美”应对研究期间的安全性信息
- 2021-09-09 17:00
- 作者:张春惠
- 来源:中国食品药品网
【条文】
《药物警戒质量管理规范》第五章 风险识别与评估
第三节 药品上市后安全性研究
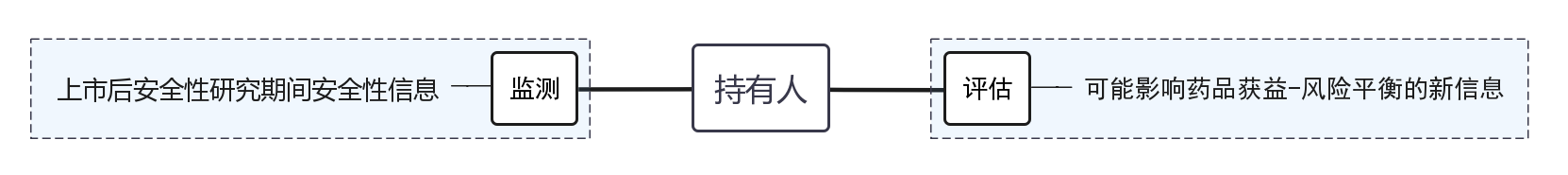
第七十七条 持有人应当监测研究期间的安全性信息,发现任何可能影响药品获益-风险平衡的新信息,应当及时开展评估。
【理解】
·监测研究期间的安全性信息
由于上市前安全性数据的局限性,GVP第七十七条规定了持有人应当监测上市后安全性研究期间的安全性信息。那么,持有人到底要监测研究期间的哪些安全性信息呢?
安全性信息指涉及患者或受试者安全和健康的事件,包括不良事件和其他一些需要上报的特殊情形:
(1) 不良事件范围:
不良事件(adverse event,AE);
不良反应(adverse drug reaction,ADR);
严重不良事件(serious adverse event,SAE);
可疑非预期严重不良反应(suspected unexpected serious adverse event,SUSAR)。
(2) 不良事件之外的其他安全性信息包括:
缺乏疗效;用药错误;药物误用;药物滥用或停药反应;职业暴露;意外暴露;妊娠或哺乳期用药;药物相互作用;父源性暴露;意外疗效;传染性传播;产品质量投诉;超说明书用药等。
Tips:
现阶段,我国临床试验期间安全性信息管理的主要依据为《药物临床试验质量管理规范》《药品注册管理办法》《药物临床试验期间安全信息评估与管理规范(试行)》和其他相关指导原则。
·评估可能影响药品获益-风险平衡的新信息
获益-风险平衡包括综合考虑疾病缓解的获益和治疗药物的风险。
获益与风险评估通常取决于社会通行的标准和受试者对风险和受益的判断。在上市后安全性研究中,持有人从监测到的安全性信息中发现可能影响药品获益-风险平衡的新信息,可包括来自上市后监测、临床研究、流行病学研究、其他科学文献、药品监督管理部门或药品不良反应监测机构发布的相关信息等,例如:
1. 药品说明书中未提及的药品不良反应,特别是严重的药品不良反应;
2. 药品说明书中已提及的药品不良反应,但发生频率、严重程度等明显增加的;
3. 疑似新的药品与药品、药品与器械、药品与食品间相互作用导致的药品不良反应;
4. 疑似新的特殊人群用药或已知特殊人群用药的变化;
5. 疑似不良反应呈现聚集性特点,不能排除与药品质量存在相关性的。
以上这些信息可能改变对药品的获益-风险评价结果并影响处方和用药决策,但还未能最终确认和评价,所以应及时开展评估。例如以下案例中,美国FDA警示心脏病患者使用拉莫三嗪有增加心律失常的风险,FDA准备评估同类药物是否对心脏有类似影响,并要求对这些药物进行安全性研究。其安全性信息为FDA收到的异常心电图(ECG)和其他一些严重问题(如胸痛、意识丧失和心脏骤停)的报告。
【实践影响】
持有人是药品安全责任的主体,应及时评估可能影响药品获益-风险平衡新的安全性信息,以优化用药方式、实现患者获益最大化,并保护患者、使其免于发生可避免的不良反应。
【延伸阅读】
《药物临床试验质量管理规范》(GCP)
《药品注册管理办法》
《药物临床试验期间安全信息评估与管理规范(试行)》
欧盟《药物警戒实践指南》2017年更新版 模块VIII(浙江太美医疗科技股份有限公司医学专员 张春惠)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:陆悦)
分享至
右键点击另存二维码!
-
为你推荐
-

行政处罚裁量 | 不确定法律概念有了确定的范围——浅析《药品监督管理行政处罚裁量适用规则》
《裁量规则》对“初次违法”“危害后果轻微”“及时改正”“充分证据”“情节严重”等不确定法律概念进行了不同程度的细化、明确、缩窄范围,并对适用这些不确定法律概念需要注意的事项给予规范... 2024-04-23 14:07 -