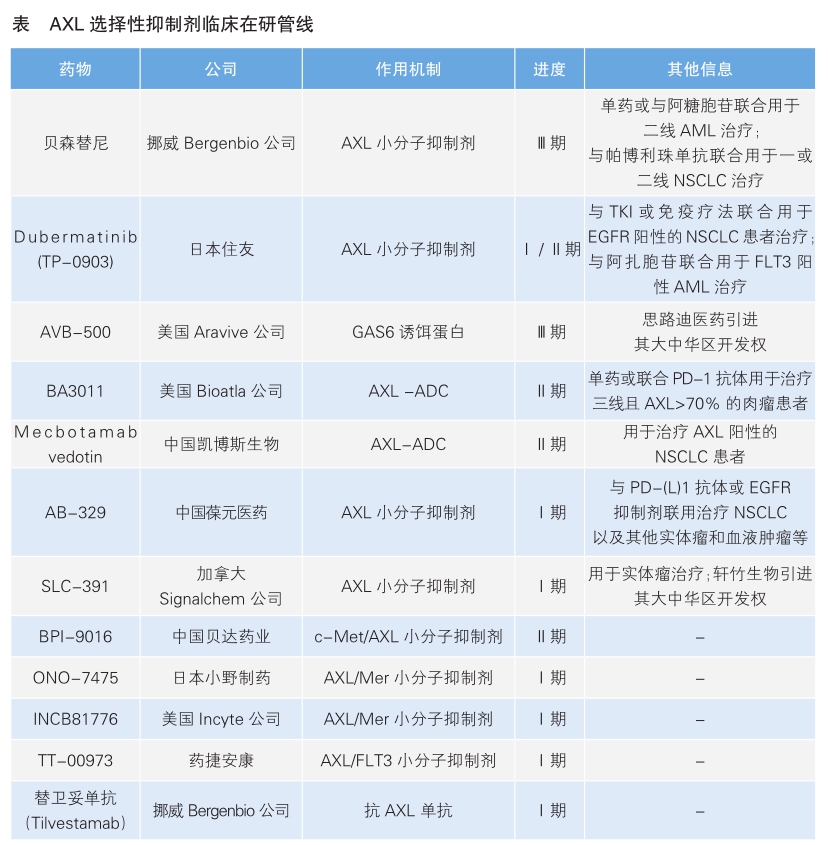
AXL选择性抑制剂:癌症治疗的潜力之星
- 2023-02-20 10:32
- 作者:陈倩
- 来源:中国医药报
AXL是受体酪氨酸激酶TAM的家族成员之一,在肿瘤中有促进肿瘤细胞存活、侵袭、免疫逃避等作用,长期以来都是抗肿瘤药物研发的热点。目前,靶向AXL的选择性抑制剂贝森替尼(Bemcentinib)和Batiraxcept都进入了Ⅲ期临床试验阶段,谁将成为AXL选择性抑制剂首个上市的产品,是业内关注的热点问题。
AXL在肿瘤微环境中的作用
AXL、Tyro3和Mer同属受体酪氨酸激酶的TAM家族。AXL及其主要配体GAS6在许多恶性肿瘤中均存在高表达,GAS6诱导AXL二聚化后,AXL受体胞内发生自身磷酸化,激活AXL受体自身酪氨酸蛋白酶活性,催化下游信号转导,包括JAK-STAT、PI3K-AKT和RAS-RAF-MEK-ERK通路,促进肿瘤细胞存活、增殖、迁移、侵袭、血管生成和免疫逃避等。
一直以来,研究人员都知道AXL与肿瘤相关,但AXL并不是传统意义上的致癌驱动因子,涉及AXL基因的突变、融合、扩增都不高,即使发现在乳腺癌中有扩增和错义突变,比例也仅有约2%。AXL蛋白在多个肿瘤细胞中检测到表达上调,且通常与不良预后有关。肿瘤的异质性一直是肿瘤治疗过程中的棘手问题,鉴于AXL对肿瘤细胞的多种作用,AXL抑制剂的开发被认为可能主要有两个方向:一是耐药性的肿瘤治疗;二是与同样“通杀”的免疫疗法联合,增强对异质性肿瘤的杀伤力。
目前已有一些公司开发了抑制剂,但都不是选择性的AXL抑制剂。如克唑替尼,最初被设计为MET抑制剂,但随后被发现对ALK和ROS1激酶具有有效活性,在基因改变驱动的非小细胞肺癌(NSCLC)治疗中具有优势。类似的还有卡博替尼、舒尼替尼等,均被批准用于实体瘤治疗。另一个值得注意的是FLT3/AXL双靶点抑制剂吉瑞替尼,已获美国食品药品管理局(FDA)批准用于FLT3突变的复发难治性急性髓系白血病(AML)治疗。
从贝森替尼看AXL靶点开发
贝森替尼是第一个进入临床研究阶段的AXL小分子抑制剂,目前处于Ⅲ期试验阶段,主要适应症为AML和NSCLC。目前贝森替尼与低剂量阿糖胞苷(LDAC)联合用于AML的二线治疗,已作为首批申报的适应症之一。
AML一直是恶性血液肿瘤中难以突破的领域,虽然近年来有不少靶向药物获批,包括BCL-2抑制剂Venetocl ax,该产品与去甲基化药物(HMA)联用成为AML患者的一线治疗新选择。此外还有针对特殊突变IDHI、CD33、FLT3的抑制剂等,但FLT3抑制剂耐药后的AML患者的治疗选择仍然有限。
2021年美国血液学年会(ASH)公布了一项贝森替尼联合LDAC用于治疗老年难治复发性AML的Ⅱ期临床试验(NCT02488408)初步数据。其中,在17例复发AML患者中,总体临床获益率为82%,4例获得完全缓解,7例无临床获益率,总体中位生存时间达13.3个月。该数据说明了AXL相关免疫调节机制在化疗复发患者中的重要性,且能延长疾病稳定时间。
在NSCLC领域,自帕博利珠单抗获批用于无特殊EGFR、ALK突变的NSCLC一线治疗后,更多免疫疗法冲向一线治疗,包括纳武利尤单抗+伊匹木单抗双免疫疗法等。而对于经免疫治疗后复发的人群,目前治疗选择很少,主要治疗选择为多西他赛或紫杉醇,但客观缓解率不到10%。
业界看好AXL抑制剂与PD-1/PD-L1抑制剂联用,实现抗肿瘤协同作用。目前贝森替尼在NSCLC领域主要是与帕博利珠单抗联用,用于三种人群的二线治疗:一是未接受PD-1抑制剂治疗的患者;二是仅接受过PD-(L)1抑制剂单药治疗后疾病进展的人群;三是接受过PD-(L)1和化疗联合治疗后疾病进展的人群。研究主要是探索在PD-(L)1表达较低的人群中,AXL抑制剂是否能增强帕博利珠单抗的疗效。根据2021年国际肺癌研究协会(IASLC)年会公布的贝森替尼与帕博利珠单抗联用治疗NSCLC患者的研究数据,队列A目前结果显示,该疗法在cAXL阳性人群中临床获益率为73%;队列B目前结果显示,该疗法在免疫治疗后复发但AXL阳性的患者中,临床获益率为85%;而在这两个队列中的cAXL阴性人群中,临床获益率分别仅为40%和0%。考虑到PD-(L)1抑制剂联合或不联合化疗在NSCLC一线治疗领域将得到更广泛的运用,所以贝森替尼与帕博利珠单抗联用作为免疫治疗后复发的二线治疗手段的疗效就尤为重要。目前初步肿瘤应答结果已经显示,但最终还是需要进行对照试验结果来验证其能否解决肿瘤免疫治疗的耐药问题。
AXL抑制剂的竞争格局
目前AXL抑制剂的研发都集中在高选择性小分子激酶靶向药物。2020年底,Genmab和ADC Therapeutics两家公司分别宣布中止其靶向AXL的抗体偶联药物(ADC)Enapotamab vedotin和ADCT-601的临床研究,原因可能是ADC毒性过大,在靶向广泛表达的肿瘤特异受体无法显示优势。2022年9月,凯博斯生物公布了Mecbotamab vedotin的Ⅱ期临床试验初步结果,该疗法基于Conditionally Active Biologics(条件活性生物制剂)技术平台, 用于治疗先前PD-1/L1、EGFR或ALK抑制剂治疗失败的AXL阳性NSCLC患者,在9名可评估患者中,观察到2名部分缓解(PR)和1名完全缓解,客观缓解率达43%。在Mecbotamab vedotin针对肉瘤治疗的临床试验中,8名多形性肉瘤患者中有4名观察到PR,7名骨肉瘤患者中有4名观察到无进展生存。
其他AXL抑制剂的研发也在继续。2016年,日本住友以首付款2亿美元、总金额约6.5亿美元收购Tol er o制药时即获得了包括TP-0903在内的4个AXL抑制剂。2020年,我国两家药企也引进了AXL抑制剂,分别是葆元医药从日本第一三共公司引进了AB-329的全球开发权,思路迪医药以2.19亿美元从美国Aravive公司获得AVB-500的大中华区开发及商业化授权。AVB-500用于治疗铂耐药性卵巢癌的适应症,已获得美国FDA授予的快速通道资格认定。贝森替尼或AVB-500都可能成为最早获批上市的AXL高选择性抑制剂。
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:陆悦)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐