每周医药看点(11月10日—16日)
- 2025-11-18 10:44
- 作者:
- 来源:中国食品药品网
商务部、公安部、国家药监局等5部门联合发布关于调整《向特定国家(地区)出口易制毒化学品管理目录》《特定国家(地区)目录》的公告;国家药监局、海关总署发布公告,公布供通关申报参考的药用类麻醉药品和精神药品海关商品编号……11月10日—16日,医药行业的这些动态值得关注。
行业·政策动态
1.商务部、公安部、应急管理部、海关总署和国家药监局联合发布关于调整《向特定国家(地区)出口易制毒化学品管理目录》《特定国家(地区)目录》的公告,将美国、墨西哥、加拿大增列入《特定国家(地区)目录》,并单独增列针对上述3个国家的13种易制毒化学品。
2.国家药监局、海关总署发布《关于药用类麻醉药品和精神药品进出口申报事项的公告》,公布供通关申报参考的药用类麻醉药品和精神药品海关商品编号,要求实际进出口商品超出该编号范围时应如实申报。
3.国家药监局决定,对上海黄海制药有限责任公司的扶正化瘀胶囊继续给予二级保护,保护期限为2025年11月10日—2030年7月20日。
4.国家药监局药品审评中心(CDE)发布《重组糖蛋白激素类产品药学研究与评价技术指导原则》,旨在进一步指导和规范重组糖蛋白激素类药物的研发和上市申请。
5.CDE就《中药提取物质量控制研究技术指导原则(征求意见稿)》公开征求意见。制定该指导原则,旨在促进中药新药研发守正创新,指导申请人开展中药创新药1.2类(从单一植物、动物、矿物等物质中提取得到的提取物及其制剂)的研发。
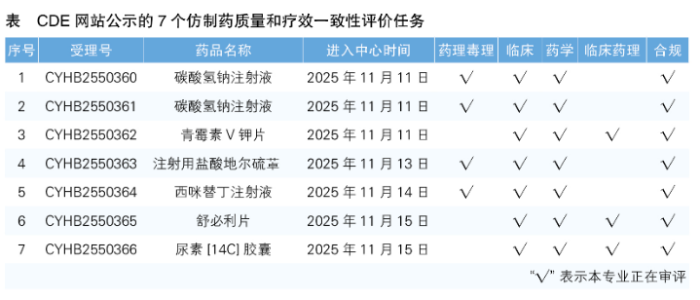
6.CDE网站公示7个仿制药质量和疗效一致性评价任务(详见表),涉及碳酸氢钠注射液等品种。
产品研发·上市信息
1.国家药监局发布4期药品批准证明文件送达信息,共包括355个受理号,涉及重庆精准生物技术有限公司等企业。
2.CDE承办受理65个新药上市申请,包括SYS6010等。
3.复宏汉霖宣布,其60mg/ml和120mg/1.7ml规格的地舒单抗注射液获英国药品和健康产品管理局(MHRA)批准上市。
4.箕星药业宣布,其在研口服小分子GLP-1受体激动剂CX11获美国食品药品管理局(FDA)批准开展治疗2型糖尿病的Ⅱ期临床试验。
5.上海医药宣布,下属上海上药中西制药有限公司醋酸艾司利卡西平片的简略新药申请已获美国FDA批准。
医药企业观察
1.乘典生物宣布,与英国生物科技公司BioCorteX达成战略合作,此次合作将结合乘典生物创新的双特异性融合蛋白(BsFP)平台与BioCorteX的科技生物技术,共同推进下一代免疫治疗药物的开发。
2.来凯医药宣布,与齐鲁制药签订独家许可协议。根据协议,来凯医药授予齐鲁制药在中国研究、开发和商业化乳腺癌候选药物LAE002的独家许可权。来凯医药最高可获得总额20.45亿元的首付款及里程碑款项,以及基于产品净销售额的十余到二十余个百分点的梯度分成。
3.南京医药宣布,与诺华医药科技(浙江)有限公司(以下简称诺华)签署商业合作协议,拿下诺华首款在华获批的放射配体疗法药物镥[177Lu]特昔维匹肽注射液的相关商业化权益。
4.药康生物宣布与益诺思达成战略合作,双方将在模型开发、安评应用与海外拓展三大领域深度协同,打造“中国模式动物+中国药代安评”联合出海的新路径。
药品集中采购
1.国家组织药品联合采购办公室发布《关于国家组织药品集中采购部分中选药品信息变更的通知(第七批)》。通知显示,按照《全国药品集中采购文件》等文件要求,中选企业满足一定条件时可变更上市许可持有人、生产企业等信息且保留中选资格,本次同意变更信息的中选药品包括注射用特利加压素、西格列汀二甲双胍片(Ⅱ)、拉考沙胺片等。
2.河北省医用药品器械集中采购中心发布《关于发布河北省中药配方颗粒集中带量采购文件的通知》。根据采购文件,此次集采共覆盖277种中药配方颗粒,其中联动具有中药配方颗粒国家药品标准且其他省已集采药品200种;按照以量换价原则,聚焦河北省内临床使用量大、采购金额大的中药配方颗粒77种。(刘鹤整理)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐