每周医药看点(2月23日—3月1日)
- 2026-03-05 15:37
- 作者:
- 来源:中国医药报
罕见病药物研发交流座谈会在国家药监局药品审评中心(CDE)召开;CDE就罕见疾病创新药物研发鼓励试点计划(“关爱计划-延伸”)相关工作文件公开征求意见……2月23日—3月1日,医药行业的这些动态值得关注。
行业政策及药监动态
1.罕见病药物研发交流座谈会在CDE召开。会议指出,国家药监局不断加强罕见病用药保障,打好政策“组合拳”,建立并畅通鼓励创新、加快引进和临时进口“三条通道”,我国罕见病用药的上市数量和速度均显著提升,仅2025年就有48个罕见病药物获批上市。
2.CDE就罕见疾病创新药物研发鼓励试点计划(“关爱计划-延伸”)相关工作文件公开征求意见。制定该试点计划,旨在鼓励创新药向临床治疗需求迫切的罕见疾病领域布局,关注并探讨解决源头性创新研发中的科学问题。
3.CDE发布《新药全球同步研发中基于多区域临床试验数据进行获益-风险评估的指导原则(试行)》。指导原则主要阐述在新药全球同步研发中基于多区域临床试验数据进行上市申请时,对单区域进行获益-风险评估的一般要求,重点关注在获益-风险评估框架下对全球同步研发临床试验数据的评估考虑。
4.CDE发布《化学合成寡核苷酸药物(创新药)药学研究技术指导原则(试行)》。指导原则适用于反义寡核苷酸,小干扰核酸(siRNA)、核酸适配体等化学合成寡核苷酸创新药物的上市申请,不包括mRNA等生物合成的核酸药物、抗体偶联核酸药物等。
5.国家药监局食品药品审核查验中心就《药品生产企业整改报告编订指南(征求意见稿)》公开征求意见。征求意见稿中所指的整改报告是指药品生产企业接受药品监管部门组织的现场检查后,针对检查发现的缺陷,按照实际整改情况,编订的反映企业调查分析、风险评估、风险控制(含纠正措施和预防措施)、完成情况等内容以及整改证明材料的一系列文件和记录。
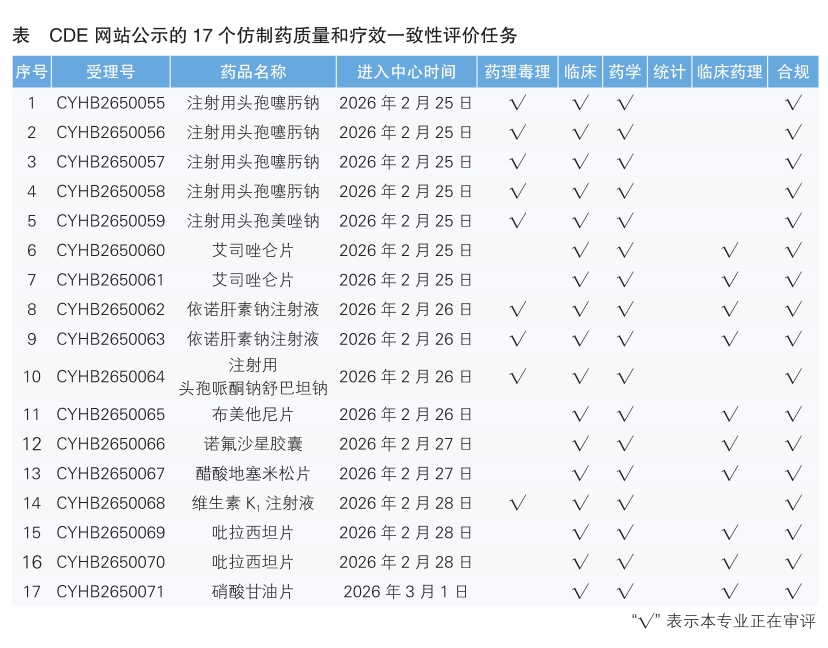
6.CDE网站公示17个仿制药质量和疗效一致性评价任务(详见表),涉及注射用头孢噻肟钠等品种。
产品研发上市信息
1.国家药监局发布5期药品批准证明文件送达信息,共包括268个受理号,涉及山东益健药业有限公司等企业。
2.CDE承办受理112个新药上市申请,包括温胆汤颗粒等。
3.亚虹医药发布公告称,公司产品APL-1702拟用于治疗宫颈高级别鳞状上皮内病变患者的上市许可申请已获得欧洲药品管理局受理。
4.汇宇制药宣布,公司向美国食品药品管理局(FDA)申报的依托泊苷注射液、氟尿嘧啶注射液的新药申请(NDA)均已获得批准。
医药企业观察
1.前沿生物宣布,与葛兰素史克达成独家授权许可协议。根据协议,葛兰素史克将获得前沿生物两款siRNA管线在全球范围内的独家开发、生产及商业化权利;前沿生物将获得4000万美元首付款,并在两个项目中累计获得最高9.63亿美元的开发、监管及商业化里程碑付款,同时享有两款产品全球净销售额的分级特许权使用费。
2.和铂医药宣布,与英国Solstice Oncology公司达成授权协议及股权合作,授予对方一款临床阶段候选产品HBM4003在大中华区以外地区的独家开发及商业化权益。根据协议,和铂医药将获得总价值逾1.05亿美元的前期对价。此外,基于未来特定里程碑事件的达成,和铂医药还有资格获得最高约11亿美元的开发、监管及商业化里程碑付款,以及基于大中华区以外地区净销售额的分级特许权使用费。
3.先为达生物宣布,与辉瑞中国就埃诺格鲁肽注射液达成商业化战略合作协议。根据协议,辉瑞中国将获得埃诺格鲁肽注射液在许可区域的独家商业化权益;先为达生物有权获得辉瑞中国支付的最高可达4.95亿美元的首付款、注册及销售里程碑付款。
4.药明合联宣布,与美国生物科技公司Earendil Labs达成战略合作。根据合作协议,药明合联将向Earendil Labs授权其自主研发的WuXiTecan-2载荷连接子技术,并授予Earendil Labs在全球范围内针对多个特定靶点抗体偶联候选药物的独家开发权。本次合作潜在总交易金额预计可达8.85亿美元。
药品集中采购
1.国家组织集采药品协议期满品种接续采购办公室发布《关于公布国家组织集采药品协议期满品种接续采购(LC-YPJX-2026-1)中选结果的通知》。根据通知,浙江海正药业股份有限公司的阿他伐他汀口服常释剂型等中选。
2.上海市医药集中招标采购事务管理所发布《关于暂停部分药品采购资格的通知》。通知显示,根据《国家药监局关于27批次不符合规定药品的通告(2026年第5号)》,自2月28日0时起,暂停唐山红星药业有限责任公司两款不同规格的醋酸曲安奈德乳膏采购资格。(刘鹤整理)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐