新旧法规体系中药品上市后注册管理事项变更对比
- 2021-01-22 16:05
- 作者:王海燕
- 来源:中国食品药品网
药品上市后变更管理是药品全生命周期管理的重要环节。为强化药品上市后变更管理,强化药品上市许可持有人(MAH)药品上市后变更管理主体责任,1月13日,国家药品监督管理局正式发布《药品上市后变更管理办法(试行)》(以下简称《办法》)。该文件一方面作为药品监管部门药品注册和生产监督管理工作的有效衔接,加强药品监管部门对药品上市后监管的规范化管理;另一方面,逐步完善了新药品监管法规制度体系建设,在现行药品注册管理法规体系中具有非常重要的地位。
现行药品注册管理主要法规体系图
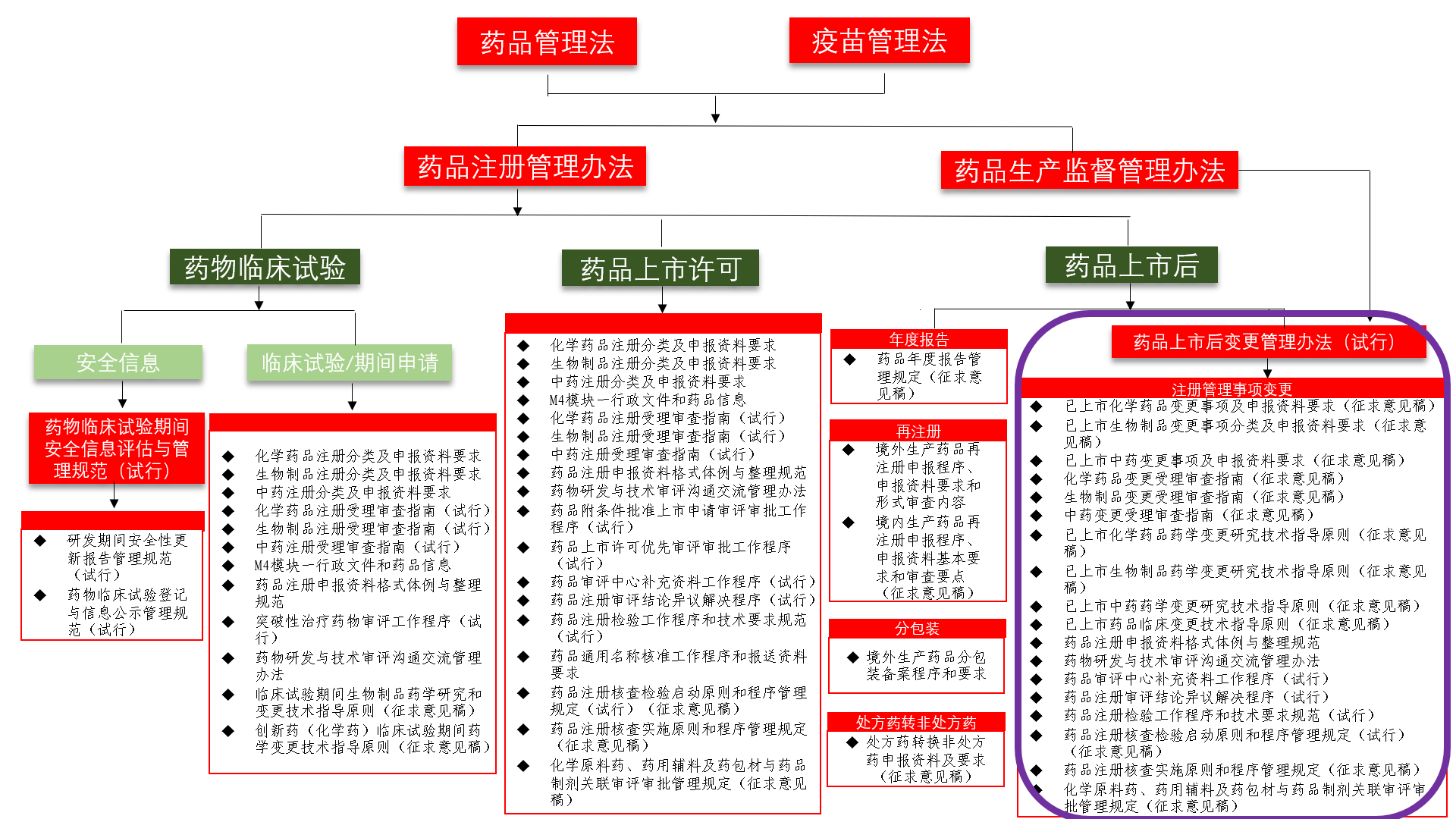
本文结合《办法》及有关文件要求,对新旧药品注册管理法规体系中药品上市后注册管理事项变更进行横向对比,以供参考学习。
注册变更事项分类
原法规环境
原《药品注册管理办法》第八章“补充申请的申报与审批”第一百一十条规定:变更研制新药、生产药品和进口药品已获批准证明文件及其附件中载明事项的,应当提出补充申请,并在附件4“药品补充申请注册事项及申报资料要求”中将补充申请注册事项分为,“国家食品药品监督管理局审批的补充申请事项”“省级食品药品监督管理部门批准国家食品药品监督管理局备案或国家食品药品监督管理局直接备案的进口药品补充申请事项”和“省级食品药品监督管理部门备案的补充申请事项”。
新法规环境
2019年颁布实施的新《药品管理法》新增第七章“药品上市后管理”,其中第七十九条明确,对药品生产过程中的变更,按照其对药品安全性、有效性和质量可控性的风险和产生影响的程度,实行分类管理。新《药品注册管理办法》第七十七条规定,药品上市后的变更,按照其对药品安全性、有效性和质量可控性的风险和产生影响的程度,实行分类管理,分为审批类变更、备案类变更和报告类变更;第七十八条至第八十条就审批类变更、备案类变更和报告类变更情形作出明确规定。
申报资料要求
原法规环境
原《药品注册管理办法》附件4中明确了药品补充申请注册事项及申报资料要求,且国家药监局药审中心(以下简称药审中心)先后发布《已上市化学药品变更研究的技术指导原则(一)》(2008年)、《生物制品生产工艺过程变更管理技术指导原则》(2008年)、《已上市中药变更研究技术指导原则(一)》(2011年)、《疫苗生产场地变更质量可比性研究技术指导原则》(2014年)、《已上市化学药品生产工艺变更研究技术指导原则》(2017年)、《已上市中药生产工艺变更研究技术指导原则》(2017年),以及《生物制品上市后变更研究技术指导原则(征求意见稿)》(2017年)和《疫苗上市后生产工艺变更研究技术指导原则(征求意见稿)》(2019年)。
根据各补充申请事项的工作流程不同,审批和备案事项需分别提出申请。
新法规环境
新《药品注册管理办法》发布后,药品监管部门在前期已发布的指导原则基础上,参考FDA、EMA、ICH对变更的分类以及相关指导原则,结合国内研发与生产现状,撰写发布《已上市化学药品变更事项及申报资料要求(征求意见稿)》《已上市生物制品变更事项分类及申报资料要求(征求意见稿)》《已上市中药变更事项及申报资料要求(征求意见稿)》《化学药品变更受理审查指南(征求意见稿)》《生物制品变更受理审查指南(征求意见稿)》《中药变更受理审查指南(征求意见稿)》《已上市化学药品药学变更研究技术指导原则(征求意见稿)》《已上市生物制品药学变更研究技术指导原则(征求意见稿)》《已上市中药药学变更研究技术指导原则(征求意见稿)》《已上市药品临床变更技术指导原则(征求意见稿)》,明确各类药品注册变更分类、申报资料要求和相应技术要求等。
《办法》的政策解读中明确,药品同时发生审批类和备案类关联的变更,或备案类变更是以审批类变更获得批准为前提时,持有人可以将审批类变更和备案类变更合并申报药审中心进行技术审评,备案类变更需按照药品补充申请收费标准缴费。
此外,《已上市药品临床变更技术指导原则(征求意见稿)》中明确:多种情形临床变更同时申报,应按其中最高类型变更的程序要求进行申请和审评审批;《已上市化学药品药学变更研究技术指导原则(征求意见稿)》《已上市生物制品药学变更研究技术指导原则(征求意见稿)》《已上市中药药学变更研究技术指导原则(征求意见稿)》中均提出“关联变更”总体上需按照技术要求较高的变更类别进行研究。
关于持有人变更
原法规环境
原《药品注册管理办法》附件4中明确:“新药的技术转让”属报“国家食品药品监督管理局审批的补充申请事项”。依据《食品药品监管局关于印发<药品技术转让注册管理规定>的通知》,申请药品技术转让,应当填写《药品补充申请表》,按照补充申请的程序和规定提交申请。符合规定的,发给《药品补充申请批件》及药品批准文号。
对于进口药品,制药厂商名称、注册地址变更,属报“国家食品药品监督管理局审批的补充申请事项”,无需进行技术审评。
改变国内药品生产企业名称,属报“省级食品药品监督管理部门批准国家食品药品监督管理局备案申请事项”。
新法规环境
新《药品管理法》第四十条规定,“经国务院药品监督管理部门批准,药品上市许可持有人可以转让药品上市许可。受让方应当具备保障药品安全性、有效性和质量可控性的质量管理、风险防控和责任赔偿等能力,履行药品上市许可持有人义务”。新《药品注册管理办法》第七十八条将“持有人转让药品上市许可”列为以补充申请方式申报的变更。
《办法》第二章第一节明确了持有人变更管理具体要求。
申请变更境内生产药品的持有人,受让方应当在取得相应生产范围的药品生产许可证后,向药审中心提出补充申请;境外持有人之间变更的,由变更后持有人向药审中心提出补充申请。药审中心同意变更的,核发药品补充申请通知书,药品批准文号和证书有效期不变。
持有人名称、生产企业名称、生产地址名称等变更,应当完成药品生产许可证相应事项变更后,向所在地省级药品监管部门就药品批准证明文件相应管理信息变更进行备案。境外生产药品上述信息的变更向药审中心提出备案。
同时,《办法》附件4中明确了药品上市许可持有人变更的申报资料要求,资料要求中除提交历次批准文件和证明性文件外,还需要提交受让方对拟转让药品的生产场地、处方、生产工艺、质量标准等应当与原药品一致、不发生变更的承诺。
关于已在境内上市的境外生产药品转移至境内生产的情形
原法规环境
《关于印发药品技术转让注册管理规定的通知》规定,已获得《进口药品注册证》的品种,其生产技术可以由原进口药品注册申请人转让给境内药品生产企业,按照补充申请的程序和规定报送有关资料和说明。
新法规环境
《办法》第十条规定,已在境内上市的境外生产药品转移至境内生产的,应当由境内申请人按照药品上市注册申请的要求和程序提出申请,相关药学、非临床研究和临床研究资料(适用时)可提交境外生产药品的原注册申报资料,符合要求的可申请成为参比制剂。
同时,该条的实施设置了2年的过渡期,境内持有人可在2023年1月15日前继续按照《关于印发药品技术转让注册管理规定的通知》要求开展研究并申报补充申请。
关于生产场地变更
原法规环境
原《药品注册管理办法》附件4中明确,“国内药品生产企业内部改变药品生产场地”为经省级药监部门批准国家药监部门备案的补充申请事项,申请资料中应当提供变更后的《药品生产许可证》。因此,变更药品生产场地需由申请人向省级药监部门分别提出变更《药品生产许可证》和药品注册批准证明文件申请。
改变进口药品的产地为报国家药监部门审批的补充申请事项。
新法规环境
《办法》中优化药品生产场地变更的申报程序。
《办法》明确,药品上市后发生药品生产场地变更的,只需向省级药品监管部门提出变更《药品生产许可证》申请。《办法》第十四条对具体程序进行了细化明确,《药品生产许可证》变更获得批准后,由省级药品监管部门直接在变更系统中更新药品注册批准证明文件及其附件上的药品生产场地变更信息。生物制品变更中涉及需要向药审中心提出补充申请事项的,持有人按照本办法提出补充申请。
对于境外持有人变更药品生产场地且变更后生产场地仍在境外的,应按照相关技术指导原则进行研究、评估和必要的验证,向药审中心提出补充申请或备案。
关于原料药变更
原法规环境
原《药品注册管理办法》附件4,“改变进口药品制剂所用原料药的产地”为报国家药监部门备案的补充申请事项;“改变国内生产药品制剂的原料药产地”为报省级药监部门备案的补充申请事项。
新法规环境
结合新《药品注册管理办法》明确建立的化学原料药、辅料及直接接触药品的包装材料和容器关联审评审批制度,《办法》进一步规定原料药变更原则。
已经通过审评审批的原料药发生变更的,原料药登记人应按照现行药品注册管理有关规定、药品生产质量管理规范、技术指导原则确定变更管理类别后经批准、备案后实施或报告,相关信息由登记人及时在登记平台更新。变更实施前,原料药登记人应将有关情况及时通知相关制剂持有人,便于制剂持有人开展后续工作。
未通过审评审批,且尚未进入审评程序的原料药发生变更的,原料药登记人可以通过药审中心网站登记平台随时更新相关资料。
此外,《化学原料药、药用辅料及药包材与药品制剂关联审评审批管理规定(征求意见稿)》也明确,化学原料药发生变更应按照现行注册管理有关规定执行,并及时告知关联制剂上市许可持有人,药品上市许可持有人应充分评估对制剂产品质量的影响,并按相关管理规定进行注册申报。《已上市化学药品药学变更研究技术指导原则(征求意见稿)》中列举了变更原料药生产工艺、变更原料药生产场地和变更制剂所用原料药的供应商的风险分类适用情形。
其他注册管理事项变更
原法规环境
原《药品注册管理办法》附件4中,将生产工艺、药用辅料、质量标准等生产过程变更,按照监管要求分为国家药监部门审批、省级药监部门审批、国家药监部门备案、省级药监部门备案等四种情形。
新法规环境
《办法》第十七条明确:生产设备、原辅料及包材来源和种类、生产环节技术参数、质量标准等生产过程变更的,持有人应当充分评估该变更可能对药品安全性、有效性和质量可控性影响的风险程度,确定变更管理类别,按照有关技术指导原则和药品生产质量管理规范进行充分研究、评估和必要的验证,经批准、备案后实施或报告。
持有人可依据药审中心发布的《已上市化学药品药学变更研究技术指导原则(征求意见稿)》《已上市生物制品药学变更研究技术指导原则(征求意见稿)》《已上市中药药学变更研究技术指导原则(征求意见稿)》等对相应类别药品的上市后变更进行研究和分类,也可自主选择使用先进的变更管理工具进行管理,按照风险分为重大变更、中等变更和微小变更。对于无法确定变更管理类别的,《办法》第三章“变更管理类别确认及调整”中也明确了与省级药品监管部门或药审中心沟通及具体实施情况。
关于审批类变更获得批准后执行时间问题
原法规环境
未予明确审批类变更获得批准后,在药品生产中何时实施。
新法规环境
《办法》第二十五条明确:持有人应当在提出变更的补充申请时承诺变更获得批准后的实施时间,实施时间原则上最长不得超过自变更获批之日起6个月,涉及药品安全性变更的事项除外。
关于审评/备案时限问题
原法规环境
原《药品注册管理办法》中明确了需要进行技术审评的补充申请时限为40日,对于合并申报事项及备案类补充申请时限未予明确。
新法规环境
新《药品注册管理办法》中明确,审批类变更的补充申请审评时限为60日,补充申请合并申报事项的,审评时限为80日,其中,涉及临床试验研究数据审查、药品注册核查检验的审评时限为200日。《办法》中对备案事项的时限作出具体明确,要求药审中心或省级药品监管部门应当自备案完成之日起5日内公示有关信息,省级药品监管部门自备案完成之日起30日内完成对备案资料的审查,必要时可实施检查与检验。(王海燕)
本文仅代表作者观点,不代表本站立场。
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:李硕)
分享至
右键点击另存二维码!
-
为你推荐
-

委托生产新规深解 | 我国药品委托生产监管迈向系统化治理
今年1月6日,国家药监局发布《关于加强药品受托生产监督管理工作的公告》,标志着我国药品委托生产监管进入了系统化、精细化、协同化治理新阶段。 2026-03-30 16:04 -

依案说法|未按规定销售特殊管理药品的法律适用探讨
本案例较有代表性,我国对麻醉药品、精神药品实施目录管理,近年来已将右美沙芬、纳呋拉啡等药品纳入第二类精神药品。在普通药品刚转为特殊药品的初期,常会涉及原有库存药品未按规定销售问题。... 2026-03-30 15:59
互联网新闻信息服务许可证10120170033
网络出版服务许可证(京)字082号
©京公网安备 11010802023089号 京ICP备17013160号-1
《中国医药报》社有限公司 中国食品药品网版权所有









