每周医药看点(5.18—5.24)
- 2022-05-26 09:38
- 作者:刘思慧
- 来源:中国食品药品网
中国食品药品网讯 国务院办公厅印发《“十四五”国民健康规划》,提到将根据需要适时调整国家免疫规划疫苗种类;国家药监局发布第五十四批仿制药参比制剂目录;CDE发布《静脉全身麻醉药的临床评价技术指导原则》……5月18日—5月24日,医药行业的这些动态值得关注。
行业政策动态
1.国务院办公厅印发《“十四五”国民健康规划》。其中提到,根据需要适时调整国家免疫规划疫苗种类;加强免疫规划冷链系统管理,提升追溯能力。保障药品质量安全。完善国家药品标准体系,推进仿制药质量和疗效一致性评价。建立符合中药特点的质量和疗效评价体系。构建药品和疫苗全生命周期质量管理机制,推动信息化追溯体系建设,实现重点类别来源可溯、去向可追。稳步实施医疗器械唯一标识制度。
2..国家药监局发布仿制药参比制剂目录(第五十四批),涉及盐酸曲马多缓释片等药品。
3.国家药监局发布公告,决定对肠炎宁制剂、茵栀黄口服制剂和银杏内酯注射液等药品说明书【不良反应】【禁忌】和【注意事项】项进行统一修订。
4.国家药监局发布公告,保妇康凝胶和调经养颜颗粒由处方药转换为非处方药。品种名单及非处方药说明书范本一并发布。
5.国家药监局综合司对《关于医用透明质酸钠产品管理类别的公告(修订草案征求意见稿)》公开征求意见。该征求意见稿对2009年发布的《关于医用透明质酸钠产品管理类别的公告》进行修订,明确医用透明质酸钠类产品分类界定有关原则,指导规范医用透明质酸钠相关产品的注册和监管工作。征求意见截止时间为2022年6月16日。
6.国家药监局药品审评中心(CDE)发布《静脉全身麻醉药的临床评价技术指导原则》。《指导原则》适用于在我国研发的静脉全麻与镇静创新药,需要开展验证性临床试验的仿制药也可参考《指导原则》中技术标准进行试验方案优化。
7.CDE发布《化学药品及生物制品说明书通用格式和撰写指南》,以规范申报资料的提交。
产品研发/上市信息
1.世界卫生组织在其官网发布消息,正式将康希诺生物股份公司重组新型冠状病毒疫苗(5型腺病毒载体)列入其紧急使用清单。该疫苗成为继国药中生北京公司新冠灭活疫苗、北京科兴中维公司新冠灭活疫苗后第三个被列入世卫组织紧急使用清单的国产疫苗。
2.国家药监局通过优先审评审批程序批准拜耳公司申报的1类创新药维立西呱片(商品名:唯可同/Verquvo)上市。该药适用于近期心力衰竭失代偿经静脉治疗后病情稳定的射血分数降低(射血分数<45%)的症状性慢性心力衰竭成人患者,以降低发生心力衰竭住院或需要急诊静脉利尿剂治疗的风险。
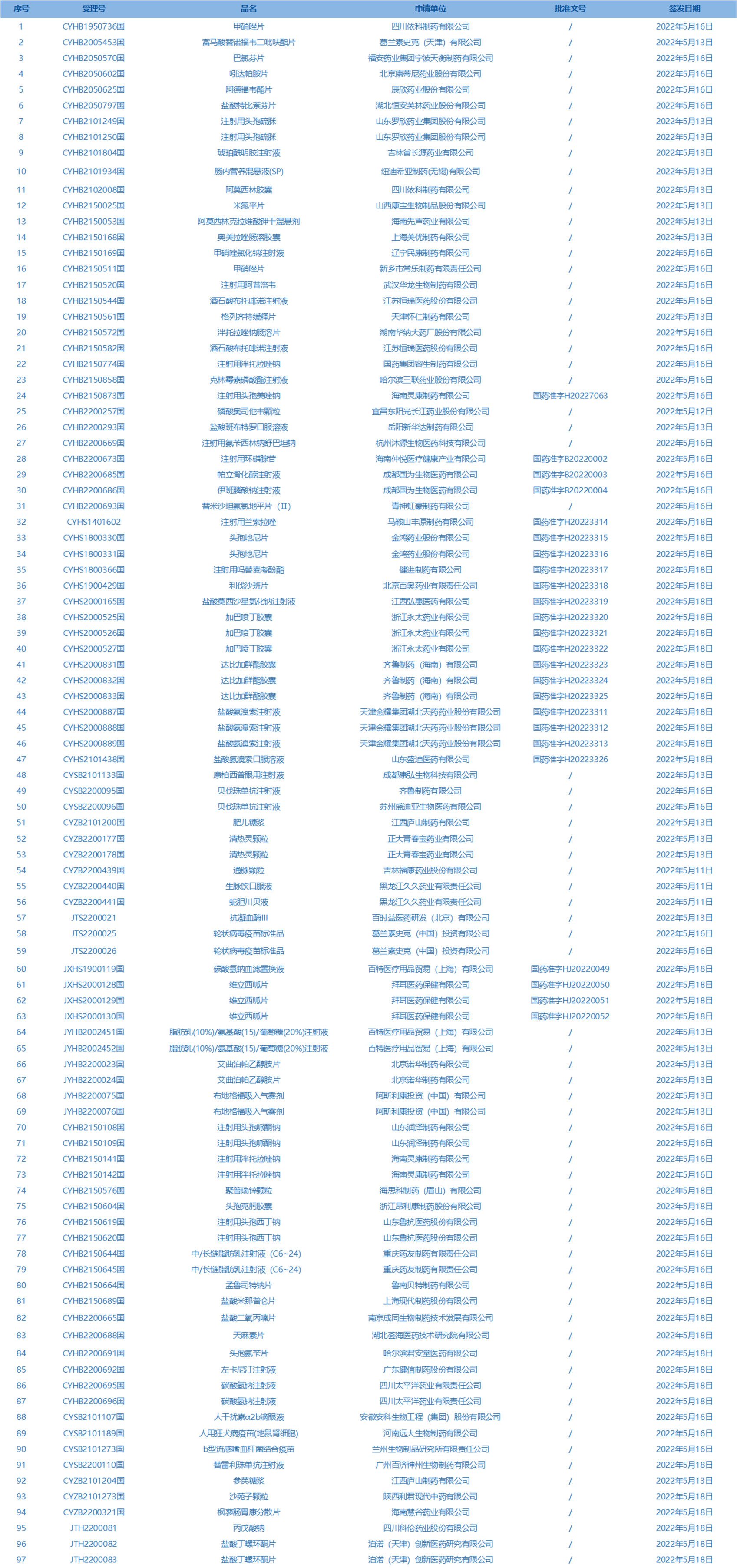
3.国家药监局发布2期药品批准证明文件待领信息,共包括97个受理号,涉及海南先声药业有限公司等企业。(截至5月24日)
4.CDE网站公示3个仿制药一致性评价任务,涉及二甲双胍格列吡嗪片等药品。(截至5月24日)

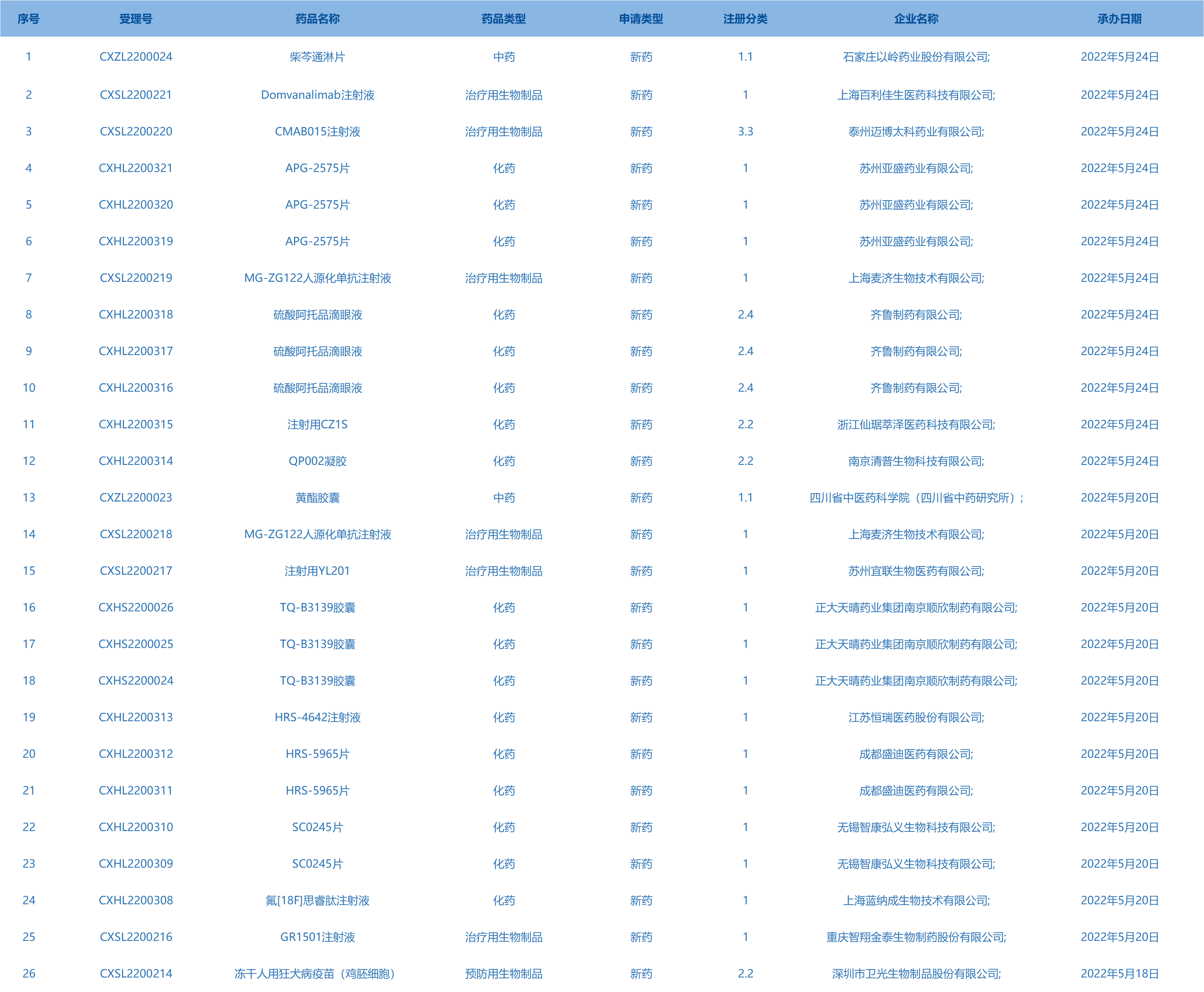
5.CDE承办受理26个新药上市申请,包括柴芩通淋片等药品。(截至5月24日)
医药企业观察
1.普利制药发布公告称,收到阿拉伯联合酋长国卫生和预防部签发的左乙拉西坦注射液的批准通知;收到荷兰药物评价委员会(CBG)签发的碘帕醇注射液上市许可。
2.前沿生物发布公告称,公司核心产品艾可宁收到阿塞拜疆卫生部核准签发的药品注册证书。
3.步长制药发布公告称,其全资子公司山东步长神州制药有限公司收到哈萨克斯坦卫生部核准签发的关于宫瘤消胶囊及消乳散结胶囊的保健品注册证书。
4.白云山发布公告称,其全资子公司中一药业收到澳大利亚药物管理局(TGA)颁发的GMP证书。
5.复星医药发布公告,其位于美国的控股子公司Fosun Pharma USA和美国VerImmune公司签订《独家许可及选择协议》,获得VerImmune公司许可,在区域内(即中国)及领域内(即治疗、缓解、诊断或预防人类或动物疾病领域)使用其专有技术和专利独家临床开发、进口及商业化基于类病毒颗粒的肿瘤免疫药物VERI-101。根据协议,VerImmune公司将获得至多总计1.25亿美元的首付款及里程碑款项,以及根据许可产品于区域内的年度净销售额达成情况、按约定比例区间的销售提成。
6.贵州百灵宣布与宁夏回族自治区中医医院暨中医研究院签订《技术开发(合作)合同》,双方拟共同参与医疗机构制剂“糖宁通络片”项目的研究和开发。
7.海正药业宣布与旺实生物签订《战略合作协议》及《委托生产框架协议》。根据《战略合作协议》,双方拟在小分子创新药VV116的产品加工、生产、国际注册、市场开发等领域建立战略合作关系,该战略合作方式不具有排他性,协议有效期为自协议生效之日起8年。另据《委托生产框架协议》,旺实生物将委托海正药业生产VV116产品,具体数量、价格以及特殊要求,以双方基于此委托生产框架协议签署的具体合同为准,协议有效期为5年。
8.东诚药业发布公告称,其全资子公司安迪科与美国ImaginAb, Inc.正式签署许可协议,安迪科为独家经销商,将取得ImaginAb专利权下规定的权利及相关数据,进而在中国开展目标产品zirconium Zr 89 crefmirlimab berdoxam的开发、注册、制造和销售。
9.博雅生物宣布与高特佳集团签署《战略合作框架协议》,将就单采血浆站投资建设及经营管理提升、质量管控体系建设、生产工艺优化提升、智能与信息化、血液制品行业投资并购等事宜展开合作。
10.海利尔药业发布公告,拟设立子公司香港海阔有限公司(具体名称以最终核定为准)。新公司拟定注册资本为人民币9600万元,山东海利尔认缴资本金占注册资本100%。
药品集中采购
1.河南省医保局就《十三省(区、市、兵团)药品集中带量采购采购文件(征求意见稿)》公开征求意见,河南、山西、内蒙古、湖北、 湖南、广西、海南、重庆、贵州、青海、宁夏、新疆、新疆生产建设兵团等十三省(区、市、兵团)组成省际联盟,对国采第二、第四批协议期满的44个品种开展接续集中带量采购。值得注意的是,此次集采将分为采购单一、采购单二来进行,但是具体如何分组,此次文件暂时没有公布。
2.湖南省医保局发布《关于做好国家组织药品集中采购(胰岛素专项)中选结果执行前准备工作的通知》,明确国采中选品种,按中选价格申报挂网,预填充、特充、畅充型胰岛素产品在同企业同品种笔芯型胰岛素产品中选价格基础上每支可增加3元。此外,原省采购平台已联动挂网的6个非中选胰岛素类药品,暂以原省采购平台挂网价在新平台申报挂网。
3.广东省医保局、广东省卫健委联合发布《关于落实第六批国家组织药品(胰岛素专项)带量采购和使用工作的通知》,明确第六批集采(胰岛素专项)首年采购周期为2022年5月31日至2023年5月30日,采购周期为2年。续签购销协议时,原则上不少于该中选产品上年度协议采购量。【中国食品药品网综合整理/刘思慧】
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐













