每周医药看点(9.6—9.12)
- 2023-09-14 13:50
- 作者:刘思慧
- 来源:中国食品药品网
中国食品药品网讯 国家药监局发布《2022年度药品审评报告》;国家药监局药品审评中心发布《中国新药注册临床试验进展年度报告(2022年)》……9月6日—9月12日,医药行业的这些动态值得关注。
行业政策动态
1.国家药监局发布《2022年度药品审评报告》。报告显示,2022年,药品审评交出亮眼成绩单:全年审评通过建议批准21个创新药,其中3个为首创新药(First-in-Class);整体按审评时限审结率提升至99.8%,且多个注册申请类别按时限审结率取得历史性突破;重组新冠病毒蛋白疫苗(CHO细胞)获批上市,4个新冠病毒治疗药物获批用于治疗新冠病毒感染肺炎,38件退热止咳类新冠病毒感染对症治疗药物药品注册申请获得应急审评批准;66个儿童用药获批上市,数量创历史新高;10个中药新药(含中药提取物)获批上市,按古代经典名方目录管理的中药复方制剂获批上市实现零的突破;在2022年世界卫生组织疫苗国家监管体系(NRA)评估中,药品注册和上市许可板块获得满分100分和最高评级4级,标志着我国药品审评机构已步入国际先进行列。
2.国家药监局、公安部、国家卫生健康委发布关于调整麻醉药品和精神药品目录的公告,自2023年10月1日起施行。公告指出,将泰吉利定列入麻醉药品目录;将地达西尼、依托咪酯(在中国境内批准上市的含依托咪酯的药品制剂除外)列入第二类精神药品目录;将莫达非尼由第一类精神药品调整为第二类精神药品。
3.国家药监局综合司就《药品网络交易第三方平台检查指导原则(征求意见稿)》公开征求意见,该原则拟适用于指导药品监管部门对提供第三方平台服务的企业开展监督检查工作,督促企业依法履行法定义务,落实平台主体责任。征求意见稿中提出常规检查重点考虑因素、有因检查重点考虑因素、检查方式等,并附检查要点。
4.国家药监局药品审评中心(CDE)发布《中国新药注册临床试验进展年度报告(2022年)》。《报告》显示,2022年,药物临床试验登记与信息公示平台登记临床试验总量达3410项(以临床试验登记号计),为历年最高,且临床试验启动效率进一步提高。2022年度共批准21个创新药(不含中药提取物和新增适应证品种),获准上市所用时间平均为7.6年,其中10个上市用时在5年内。
5.CDE就《罕见病基因治疗产品临床试验技术指导原则(征求意见稿)》公开征求意见。该原则将结合罕见病特征、基因治疗产品特征,对罕见病基因治疗产品的临床研发提出建议,为罕见病基因治疗产品开展临床试验提供参考。
6.CDE就《间充质干细胞防治移植物抗宿主病临床试验技术指导原则(征求意见稿)》公开征求意见。该指导原则旨在提供关于间充质干细胞防治移植物抗宿主病临床试验的建议,提高相关产品的研究和申报效率,尽快满足患者的临床需求。征求意见稿主要分为3个部分,分别为概述、临床试验考虑、与监管机构的沟通。
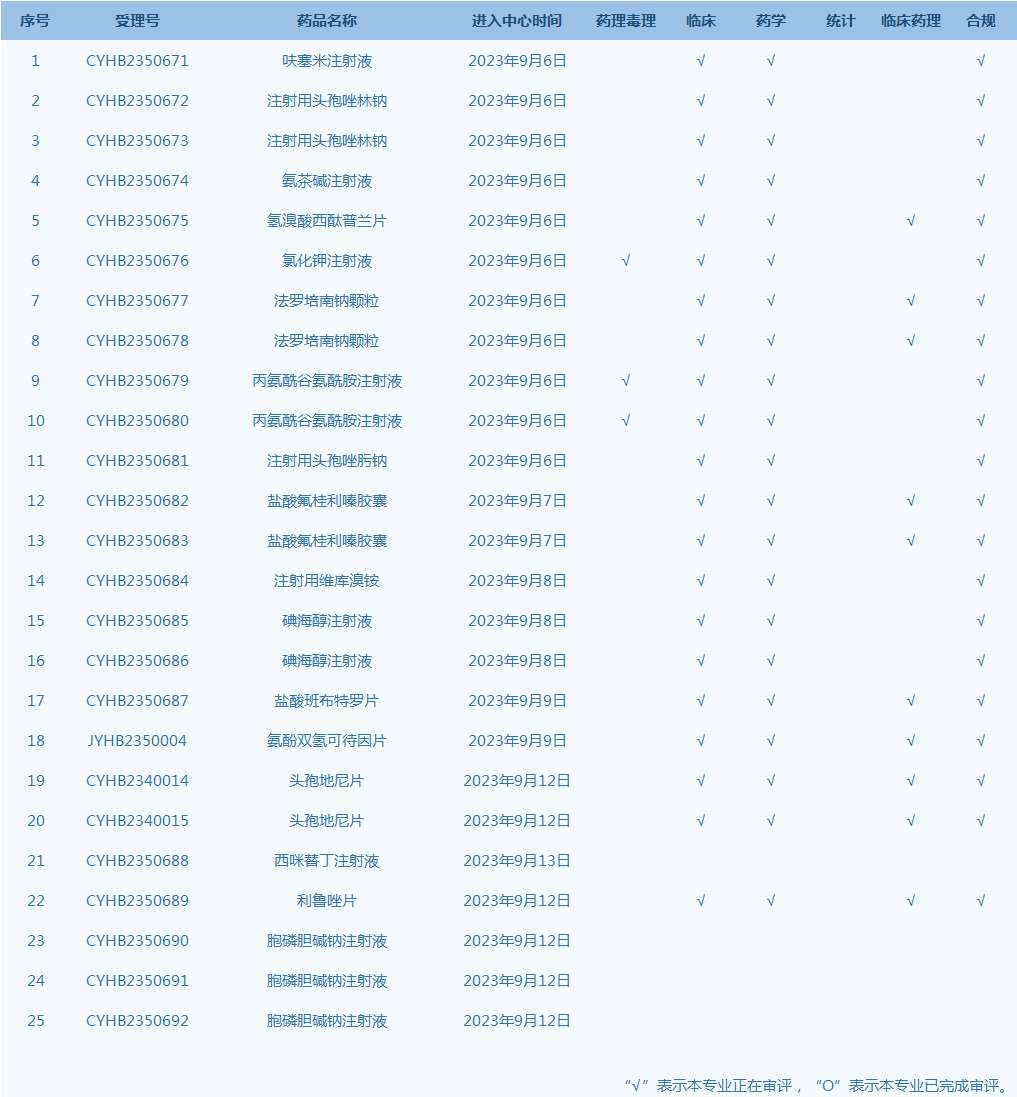
7.CDE网站公示25个仿制药一致性评价任务,涉及呋塞米注射液等品种。(截至9月12日)
产品研发上市信息
1.国家药监局通过优先审评审批程序附条件批准上海津曼特生物科技有限公司申报的纳鲁索拜单抗注射液(商品名:津立生)上市。该药品适用于治疗不可手术切除或手术切除可能导致严重功能障碍的骨巨细胞瘤成人患者。
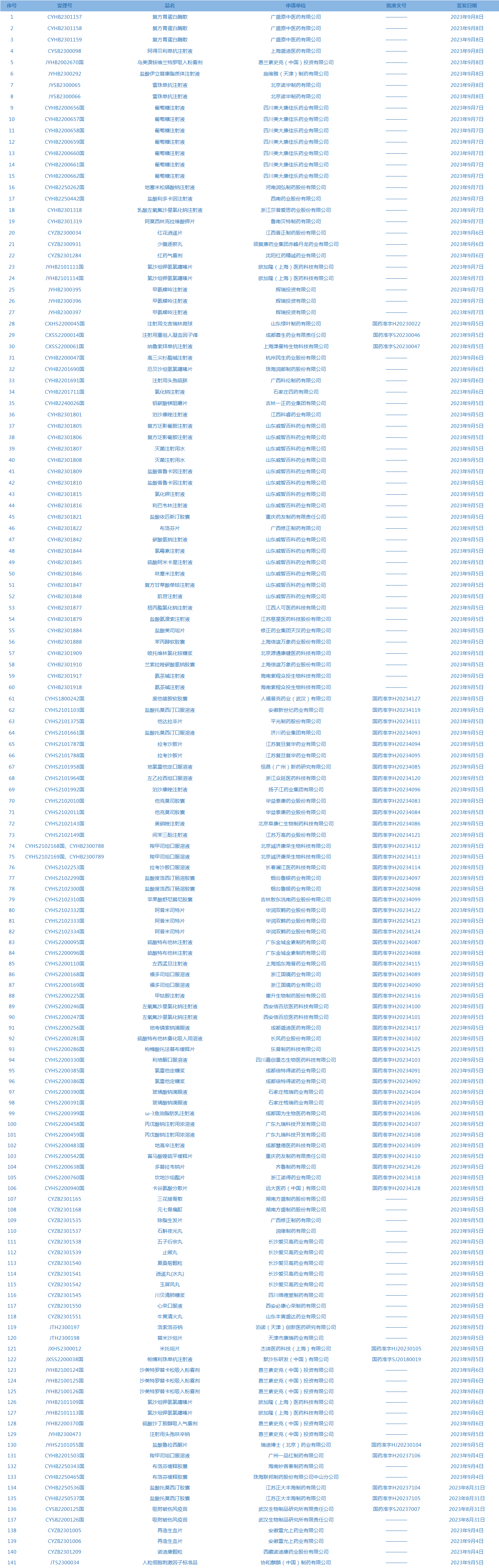
2.国家药监局发布4期药品批准证明文件送达信息,共包括141个受理号,涉及广盛原中医药有限公司等企业。(截至9月12日)
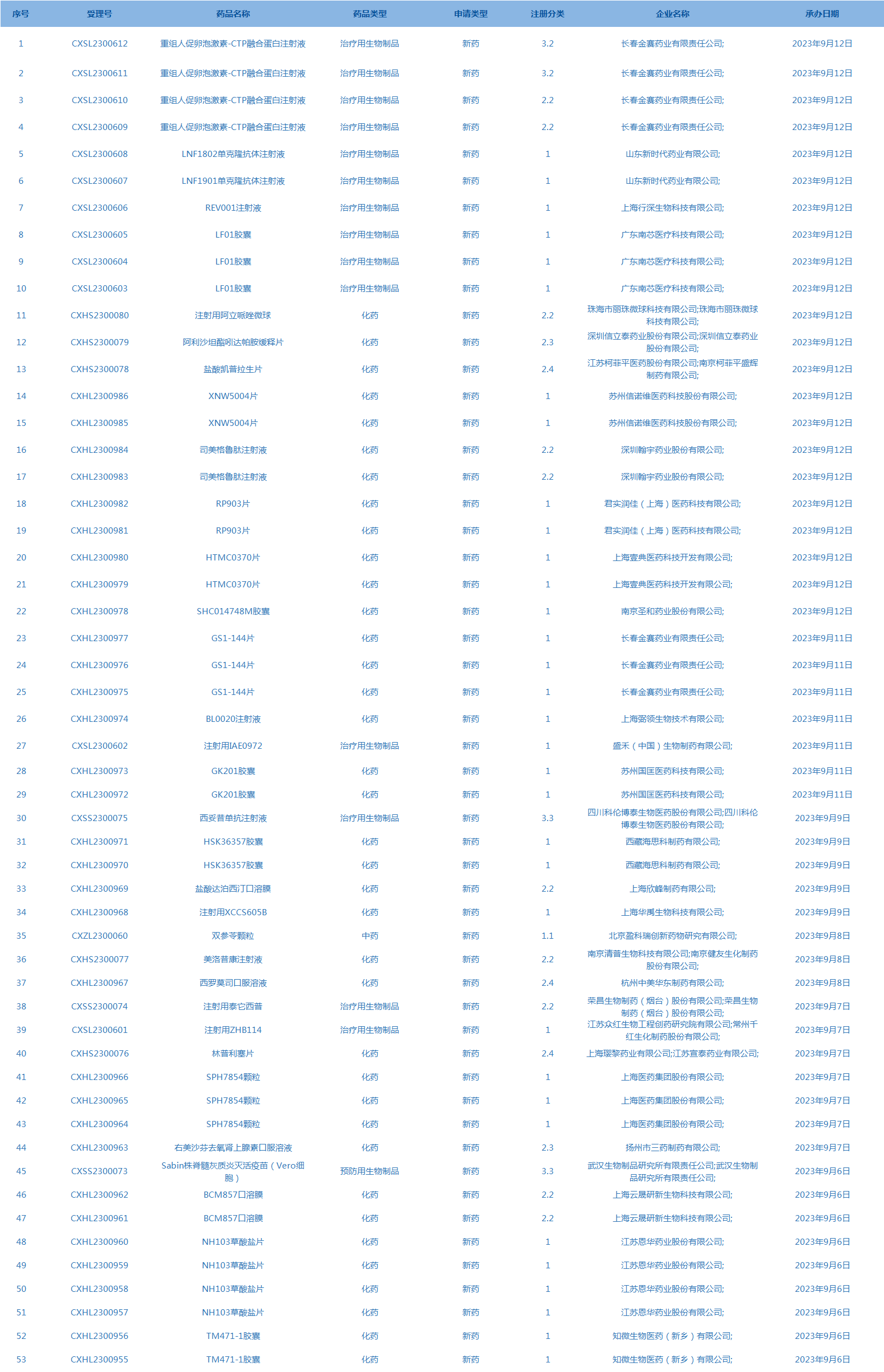
3.CDE承办受理53个新药上市申请,包括LNF1802单克隆抗体注射液等药品。(截至9月12日)
5.康华生物发布公告称,收到美国食品药品管理局(FDA)的通知,同意公司重组六价诺如病毒疫苗在美国进入临床研究。
6.和誉发布公告称,公司附属公司上海和誉生物医药科技有限公司创新CSF-1R抑制剂Pimicotinib(ABSK021)被欧洲药品管理局(EMA)批准进入一项针对腱鞘巨细胞瘤(TGCT)患者的有效性和安全性的随机、双盲、安慰剂对照、多中心的Ⅲ期临床研究。
7.百济神州宣布其BTK抑制剂泽布替尼(百悦泽)在智利、厄瓜多尔获批,用于治疗慢性淋巴细胞白血病(CLL)或小淋巴细胞淋巴瘤(SLL)成人患者。
8.易慕峰宣布其基于SNR技术平台研发的新一代自体CAR-T产品IMC008近期已获得美国FDA孤儿药资格,用于治疗胰腺癌患者。
9.纽福斯宣布其候选药物NFS-05用于治疗显性遗传性视神经萎缩(ADOA)完成澳大利亚治疗用品管理局(TGA)临床试验备案,被批准开展临床试验。NFS-05是一款在研眼科基因治疗新药。
10.森朗生物宣布收到美国FDA孤儿药开发办公室(OOPD)正式书面回函,其研发的靶向CD7的CAR-T细胞产品(SENL101自体T细胞注射液)被授予孤儿药资格,用于治疗成人复发或难治性T淋巴母细胞淋巴瘤/白血病(T-LBL/ALL)。
医药企业观察
1.鹭燕医药发布公告称,公司控股子公司海南鹭燕医药有限公司因经营发展及鹭燕医药海南总部基地项目建设需要,注册资本拟由人民币3500万元增至人民币1亿元。
2.联环药业发布公告称,公司控股子公司成都亚中生物制药有限责任公司拟申请在全国中小企业股份转让系统(新三板)挂牌。
3.贵州三力与贵州健康农、三力健康共同投资设立贵州三康企业管理合伙企业(有限合伙),认缴出资额人民币1亿元。其中,贵州三力作为有限合伙人出资500万元,占认缴出资额的5.00%;三力健康作为普通合伙人出资5500万元,占认缴出资额的55.00%;贵州健康农作为有限合伙人出资4000万元,占认缴出资额的40.00%。
4.沙砾生物宣布完成4亿元人民币的B轮融资,本轮融资由中金资本旗下基金领投,前海方舟、联东投资、源禾资本、禾方田合伙企业以及原股东夏尔巴投资、德诚资本、经纬中国跟投。本轮融资将用于支持其肿瘤浸润淋巴细胞(TIL)疗法管线的开发,包括GT101的关键临床试验以及多项下一代基因编辑型TIL管线的开发。
药品集中采购
1.山东省公共资源交易中心发布《中药配方颗粒采购联盟集中采购公告》,由山东、山西、内蒙古、辽宁、吉林、黑龙江、安徽、江西、海南、云南、西藏、陕西、青海、新疆、新疆生产建设兵团组成省际联盟,代表上述地区医药机构开展中药配方颗粒集中带量采购工作。采购品种为具有中药配方颗粒国家药品标准的200个品种,各品种采购周期原则上为2年。
2.宁夏医药采购平台网站公示宁夏回族自治区医疗机构第三批药品联盟议价采购文件和采购目录,维生素D2、地佐辛、棕榈酸帕利哌酮等28个产品纳入此次采购目录。
(刘思慧整理)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐













