每周医药看点(11.8—11.14)
- 2023-11-16 09:45
- 作者:刘思慧
- 来源:中国食品药品网
中国食品药品网讯 CDE发布《糖尿病视网膜病变相关中药新药临床研发技术指导原则(试行)》,传奇生物与诺华达成授权合作……11月8日—11月14日,医药行业的这些动态值得关注。
行业政策动态
1.11月13日,2023年“全国安全用药月”活动在京启动。本届安全月以“安全用药 健康为民”为主题,通过开展药品安全网络知识竞赛、药品安全互动体验活动、药品检验公众开放日活动、“寻找身边最美药师”活动等,持续普及药品安全知识,推进社会共治。
2.为贯彻落实《国务院办公厅关于加快推进电子证照扩大应用领域和全国互通互认的意见》(国办发〔2022〕3号),推动电子证照全国互通互认,全国一体化政务服务平台药品监管电子证照工程标准已发布35项,实现药品监管证照发证清单标准“全覆盖”。
3.国家药监局药品审评中心(CDE)发布《糖尿病视网膜病变相关中药新药临床研发技术指导原则(试行)》,自发布之日起施行。该指导原则主要适用于处方来源于中医药理论和中医临床实践,且申请人认为可用于治疗或预防糖尿病视网膜病变(以下简称糖网)、糖尿病黄斑水肿的中药新药。该指导原则指出,中药新药的研发多源于临床,中医临床实践也是中药研发的过程,研究者应当重视中医药理论在阐释糖网不同分期和分型的病机特点、指导临床遣方用药、总结处方功能主治、发现患者获益以及精准获益人群特征等方面的重要作用,在临床实践中挖掘中药用于糖网的疗效及其临床优势和特点。
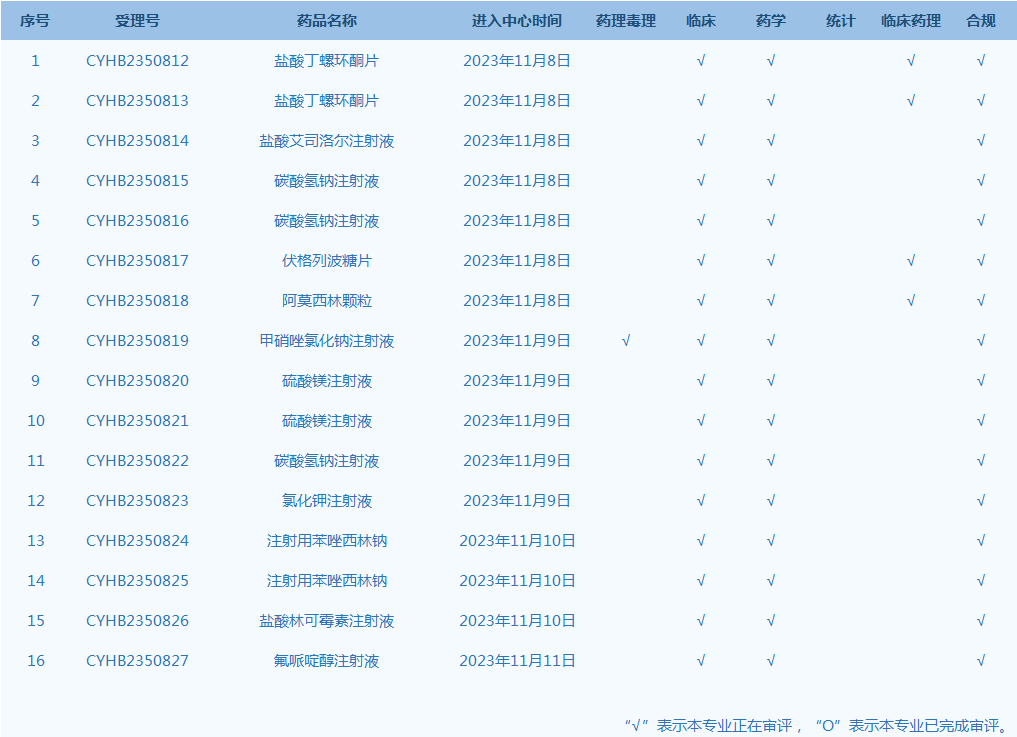
4.CDE网站公示16个仿制药一致性评价任务,涉及盐酸丁螺环酮片等品种(截至11月14日)。
产品研发上市信息
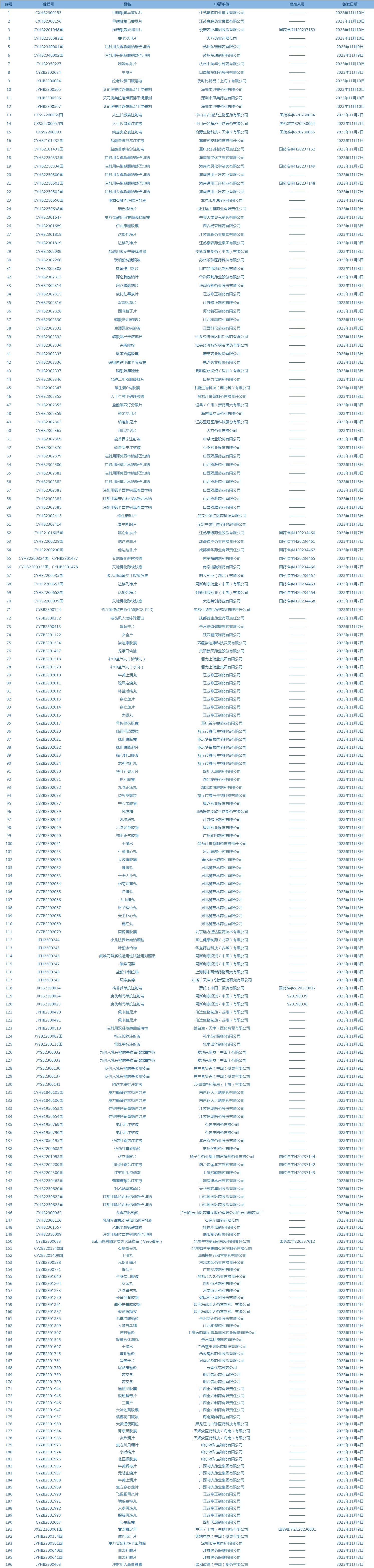
1.国家药监局发布3期药品批准证明文件送达信息,共包括196个受理号,涉及江苏豪森药业集团有限公司等企业(截至11月14日)。
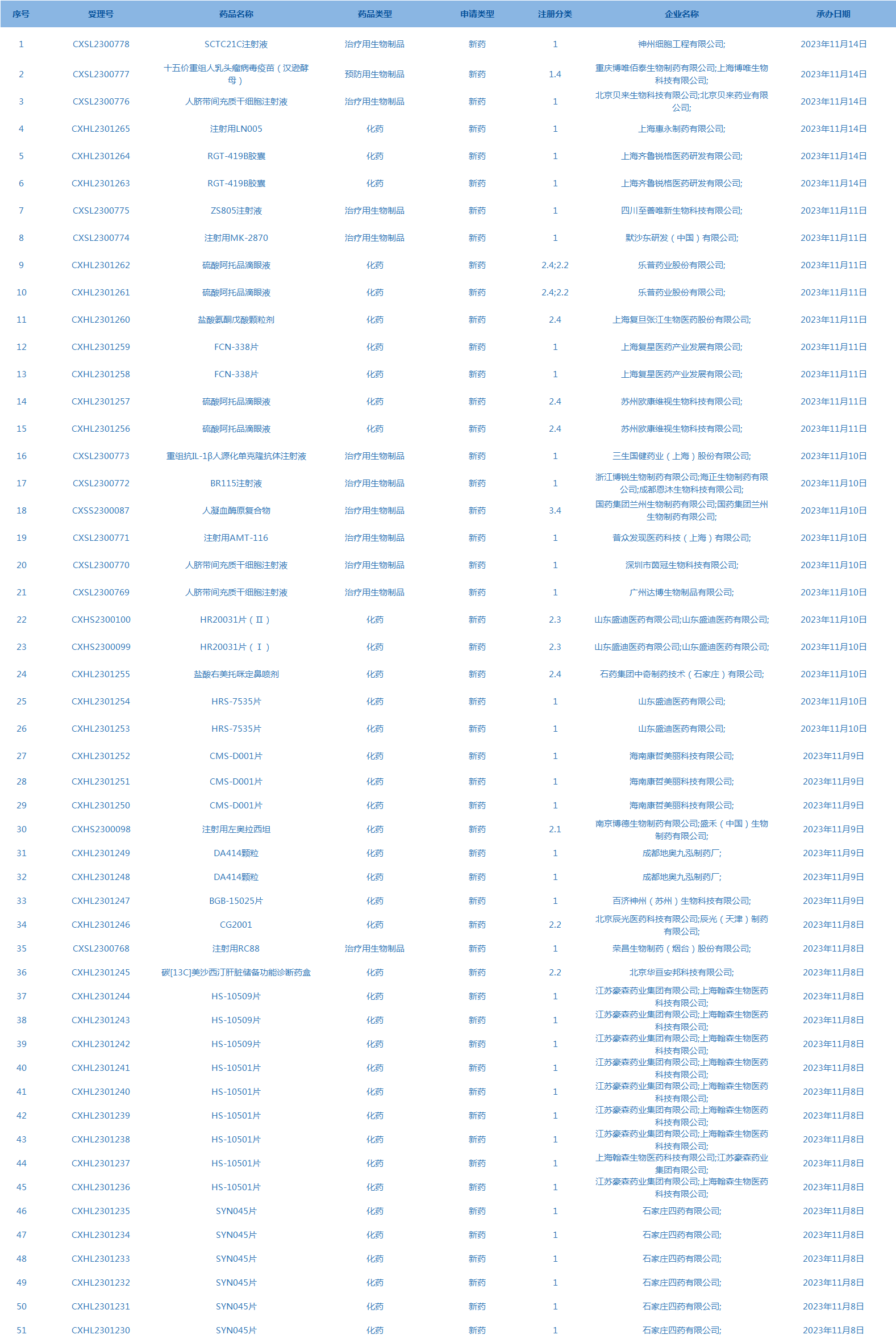
2.CDE承办受理51个新药上市申请,包括SCTC21C注射液等药品(截至11月14日)。
3.普利制药发布公告称,公司收到以色列卫生部药剂司签发的依替巴肽注射液的上市许可。
4.汇宇制药发布公告称,公司全资子公司SeacrossPharmaceuticals Ltd.于近日收到巴基斯坦药品管理局核准签发的关于公司产品奥沙利铂注射液的上市许可。
5.和誉医药宣布,其自主研发的抗耐药突变小分子成纤维细胞生长因子受体4(FGFR4)抑制剂ABSK012获美国FDA批准,可开展其单药在晚期实体瘤患者中的首次Ⅰ期临床试验。
医药企业观察
1.传奇生物正式宣布,其全资子公司传奇生物爱尔兰有限公司与诺华(Novartis)就传奇生物的特定靶向DLL3的嵌合抗原受体T细胞(CAR-T)疗法签订了独家全球许可协议,包括其自体CAR-T细胞疗法候选药物LB2102。传奇生物授予诺华开发、制造和商业化这些细胞疗法的全球独家权利,诺华可以将其T-Charge平台应用于其生产。根据许可协议,传奇生物将获得1亿美元的预付款,并有资格获得高达10.1亿美元的临床、监管和商业里程碑付款以及分级特许权使用费。
2.华东医药全资子公司中美华东与圣因生物(SanegeneBio)达成战略合作,双方将基于圣因生物的LEAD创新技术平台,共同开发针对慢性代谢性疾病的siRNA药物,并进一步探讨在其他治疗领域开发新型siRNA药物的合作机会。
3.诚益生物宣布与阿斯利康达成一项独家许可协议。阿斯利康将开发和商业化诚益生物发现的小分子GLP-1受体激动剂(GLP-1RA)ECC5004,用于包括肥胖症、2型糖尿病和其他合并症的潜在治疗。根据协议条款,诚益生物将获得1.85亿美元的首付款。此外,诚益生物还将有资格获得高达18.25亿美元的未来临床、注册和商业化里程碑付款。同时,诚益生物还将有资格获得该产品净销售额的分级特许权使用费。
4.基石药业宣布将RET抑制剂普吉华(普拉替尼胶囊)在中国大陆的独家商业化推广权授予艾力斯医药。基石药业继续拥有普拉替尼胶囊在中国大陆研发、注册等推广权之外的权益。根据协议条款,基石药业将获得首付款和后续的研发里程碑付款,并将继续获得普拉替尼胶囊在中国大陆的销售收入,艾力斯医药将从基石药业收取服务费。
5.思派健康发布公告称,公司全资附属公司思派健康产业投资有限公司与上海罗氏制药有限公司(以下简称罗氏制药中国)订立不具法律约束力的战略合作协议。根据战略合作协议,公司与罗氏制药中国将全面利用并结合其各自的业务布局、技术资源及客户资源优势,本着优势互补、互惠互利、合作共赢和友好协商的原则,在医药分销渠道、创新支付、医患管理、院外数据和真实世界研究等方面达成合作意向。公司及罗氏制药中国将高效利用公司覆盖全国多个城市的专业特药医药业务和高标准药品配送团队,进一步提升肿瘤及其他特殊疾病患者的用药可及性和服务可及性。同时,双方亦将探索多元化及创新的支付方式,通过惠民保(作为国家基本医疗保险的补充),提升患者对创新药品的可及性。
药品集中采购
1.山东省公共资源交易中心发布《关于公布省际联盟中药配方颗粒集中带量采购中选结果的通知》,此次省际联盟中药配方颗粒集中带量采购共产生13404个中选产品,其中涉及6893个代表品,与最高有效申报价相比,代表品的平均降幅为44.62%,最高降幅93.57%。
2.江苏省医保局网站公示了第四轮药品集中带量采购拟中选结果。此次拟中选品种包括313个西药、84个中成药,分别涉及193家、75家企业。按江苏集采规则,西药独家报价不高于本产品省级集采最低价的,拟中选;非独家品种有效报价由低至高排序,排名在同组前50%的企业拟中选,或在同品种最高有效申报价基础上降幅达40%,拟中选。(刘思慧整理)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐













