每周医药看点(4月8日—4月15日)
- 2024-04-16 09:09
- 作者:刘思慧
- 来源:中国食品药品网
中国食品药品网讯 国家药监局公布药品说明书适老化及无障碍改革试点名单(第二批);枸橼酸铋钾胶囊由处方药转换为非处方药……4月8日—4月15日,医药行业的这些动态值得关注。
行业政策动态
1.工业和信息化部、国家发展改革委等七部门印发《推动工业领域设备更新实施方案》(以下简称《方案》)。《方案》指出,更新升级试验检测设备,在医药等重点行业,围绕设计验证、测试验证、工艺验证等中试验证和检验检测环节,更新一批先进设备,提升工程化和产业化能力。
2.国家药监局发布公告,枸橼酸铋钾胶囊由处方药转换为非处方药。品种名单及其非处方药说明书范本一并发布。
3.国家药监局发布公告,决定对玉屏风制剂(含口服液、胶囊、颗粒、袋泡茶、丸、滴丸、软胶囊7种剂型)、元胡止痛制剂说明书中的【不良反应】【禁忌】和【注意事项】项进行统一修订。
4.国家药监局公布药品说明书适老化及无障碍改革试点名单(第二批),包括匹伐他汀钙片、缬沙坦氢氯噻嗪片、阿司匹林肠溶片等102种药品。
5.CDE网站公示27个仿制药一致性评价任务,涉及盐酸维拉帕米注射液等品种(截至4月15日)。

产品研发上市信息
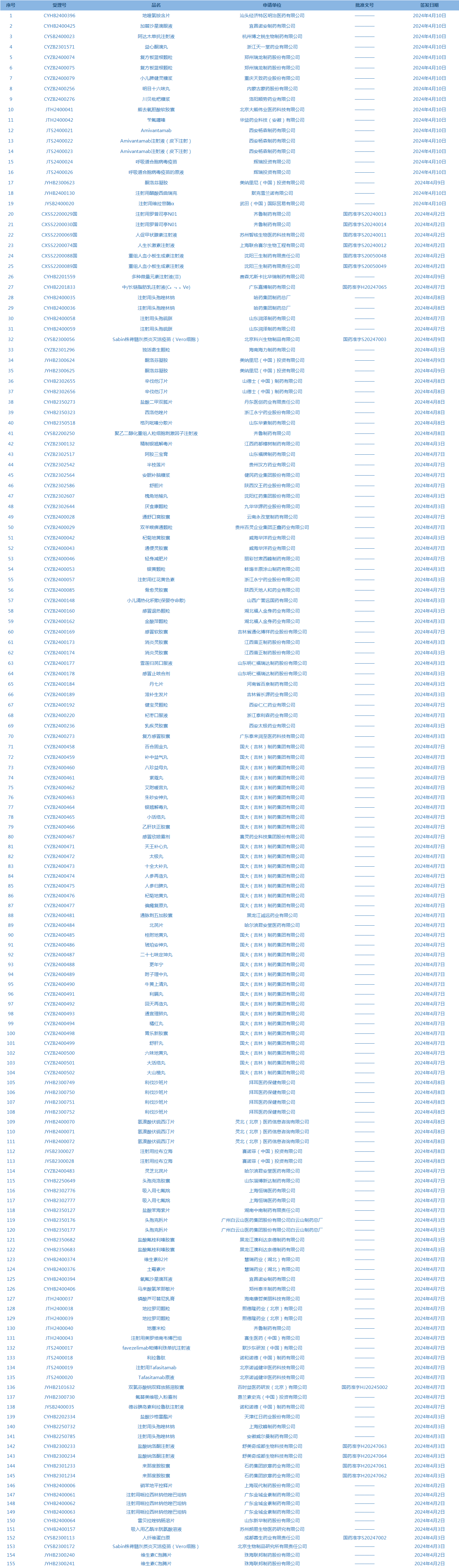
1.国家药监局发布5期药品批准证明文件送达信息,共包括155个受理号,涉及哈药集团制药总厂等企业(截至4月15日)。
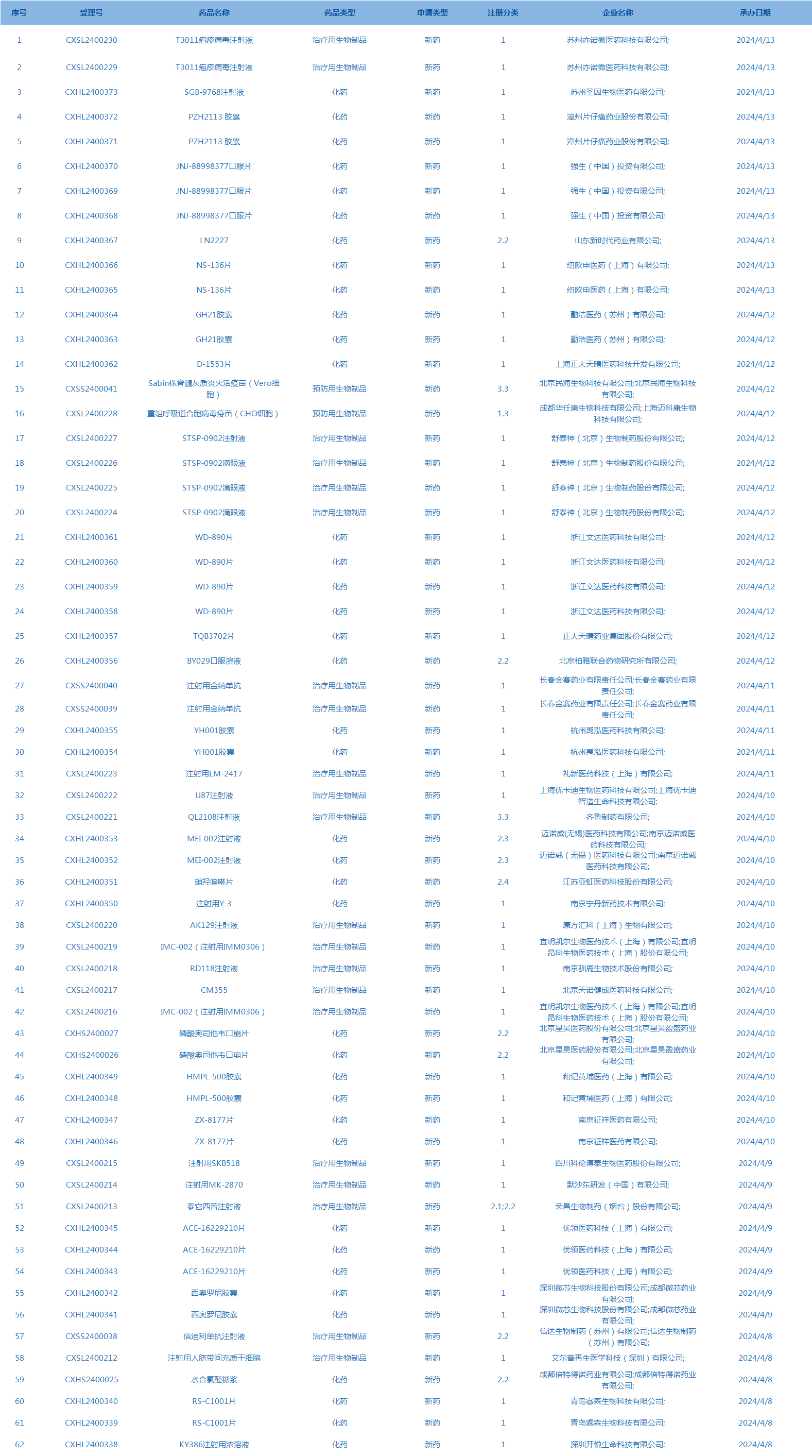
2.CDE承办受理62个新药上市申请,包括T3011疱疹病毒注射液等药品(截至4月15日)。
3.凡恩世宣布,美国食品药品管理局(FDA)授予其DLL3/CD47双抗PT217快速通道资格,用于治疗接受铂类药物化疗后出现疾病进展的广泛期小细胞肺癌(ES-SCLC)患者,无论其是否接受过免疫检查点抑制剂联合治疗。
4.同宜医药宣布,其自主研发的第二代Bi-XDC双配体偶联药物CBP-1019已经获得美国FDA孤儿药资格,用于治疗食管癌。
5.先声药业旗下抗肿瘤创新药公司先声再明宣布,其人源化GPRC5D-BCMA-CD3三特异性抗体SIM0500获得美国FDA授予的快速通道资格,针对适应证为:用于既往接受过≥3线治疗(包括一种蛋白酶体抑制剂、一种免疫调节剂及一种抗CD38单克隆抗体),且对于已知可以提供临床获益的标准治疗耐药,或无法耐受的多发性骨髓瘤患者。
6.同源康医药宣布,其自主研发的新一代口服、高效、高选择性的小分子YAP/TEAD抑制剂TYK-01054获美国FDA批准开展临床研究。
医药企业观察
1.勤浩医药宣布与阿斯利康建立临床研究合作,双方将探索SHP2抑制剂GH21联合甲磺酸奥希替尼治疗非小细胞肺癌(NSCLC)的临床疗效。据悉,该项研究为开放性、多中心、Ⅰb/Ⅱ期临床研究,旨在评估联合治疗在伴有表皮生长因子受体(EGFR)突变的晚期NSCLC患者中口服给药的安全性、耐受性、药代动力学和初步有效性,首例患者已于近期完成首次给药 。
2.德昇济医药宣布完成由欧洲生命科学投资企业Medicxi主导的6200万美元A+轮融资,现有投资者经纬中国和药明康德风险投资基金也参与了此轮融资。本轮融资资金将用于加速德昇济医药产品管线在临床前和临床阶段的开发,特别是推动首款产品D3S-001的全球临床试验。
3.智核生物宣布完成近亿元人民币C+轮融资。本轮融资由元禾控股领投,裕智资本、见素资本、苏州领军创投跟投,原股东锐合资本继续支持。本轮募集资金将主要用于该公司即将上市的首个产品—人促甲状腺素注射液(rhTSH)的商业化、SNA002等创新放射性诊断药物的临床试验,以及SNA014、SNA025等新靶点治疗性核药的IND推进等。
药品集中采购
1.北京市医保局发布《关于公示十五省(区、市)联盟地区接续药品视同中选产品资格确认结果的通知》,共包括37家药企的26个品种、45个品规。如果相关企业同意按该产品现行最低集采接续中选价格供应北京市的,将视同具有北京中选产品资格。
2.河南省医保局、河南省财政厅联合印发《河南省集中带量采购药品和医用耗材货款医保基金与医药企业直接结算实施方案》(以下简称《方案》),《方案》要求,各统筹地区医保经办机构统一在医保基金支出户下设立药品医用耗材直接结算子账户进行分账核算,用于支付中选产品货款,接收医疗机构返款,每月向财政部门提交用款计划,财政部门根据经办机构提交的用款计划将资金从社会保障基金财政专户拨入直接结算子账户,用于保障中选产品货款结算。(刘思慧整理)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐