一周法治播报(7.12-7.18)
- 2021-07-19 14:34
- 作者:陆悦
- 来源:中国食品药品网
“一周法治播报”来了!以下是7月12日-7月18日,各省级药监部门的法治动态。
法规文件
1.上海市药监局发布通告,将部分市级许可事项委托下放各区市场监管局。自7月15日起,新申请的下列许可事项由各区市场监管局办理,市药监局已受理的申请仍按原流程办理:科研、教学购用麻醉药品、精神药品(含对照品)以及医疗用毒性药品审批的受理、现场核查、审查、许可决定、制证、送达等环节;非药品生产企业《咖啡因购用证明》审批的受理、现场核查、审查、许可决定、制证、送达等环节;药品医疗器械互联网信息服务审批受理、审查、许可决定、制证、送达等环节,并且实施告知承诺制,允许申请人选择一般流程或告知承诺流程申请该许可;化妆品生产许可受理和发证环节。
2.江西省药监局印发《中药饮片不符合药品标准尚不影响安全性有效性”认定指导意见(试行)》,文件自发布之日起施行。文件明确,中药饮片经检验“不符合药品标准,尚不影响安全性、有效性”的认定,限于检验项目中性状项目中的大小、形状、厚薄及表面色泽,检查项目中的杂质、水分、灰分。文件列举了符合上述要求的情形以及除外情形。
3.四川省卫生健康委员会、四川省药监局发布《关于加强全身麻醉药管理的通知》,规范该省对全身麻醉药(以下简称全麻药)生产、流通以及使用环节的管理,保障用药安全。
4.云南省药监局印发《云南省药品监督管理局促进中药传承创新发展三年行动方案》。《方案》要求,到2024年,实现以下发展目标:一是传承创新环境明显改善,进一步建立健全云南省中药民族药传承创新的体制机制;二是标准管理能力不断提高,力争3年内修订省级药材标准、中药饮片炮制规范、中药配方颗粒质量标准100个、标准物质60个、民族药药材标准提升20个以上;三是中药新药(院内制剂)研发、中药二次开发取得新突破,力争3年内实现5个中药(民族药)院内制剂申报注册、30个中药(民族药)申报传统工艺备案、1个中药院内制剂品种向新药转化的阶段性目标等;四是建立一支与中药(民族药)产业发展和新时代药品监管工作相适应的中药审评员、检查员队伍;五是监管水平安全形势持续向好,推进全省中药的高质量发展。
《方案》从加大中药创新研发平台建设力度、促进中药创新发展,建立健全省级层面药品审评审批及备案体系,强化中药质量安全监管,完善中药标准体系,强化技术支撑体系建设,提高信息化管理水平六个方面,列举了20项重点工作任务。
标准规范
1.安徽省药监局公示第一批中药配方颗粒标准草案,意见反馈时间为30天(自7月16日起)。本次制定的中药配方颗粒标准包含14个品种。
监督检查
1.山西省药监局印发《关于进一步加强可用于医疗美容的医疗器械监管的通知》,要求切实规范可用于医疗美容的医疗器械生产、经营行为,加大监督检查力度,依法严惩违法违规行为。
2.山西省药监局发布通告,山西君雁药业有限公司忻州分公司严重违反《药品经营质量管理规范》的规定,为防控药品质量风险,依据《中华人民共和国药品管理法》第九十九条,对该企业采取暂停销售的风险防控措施。
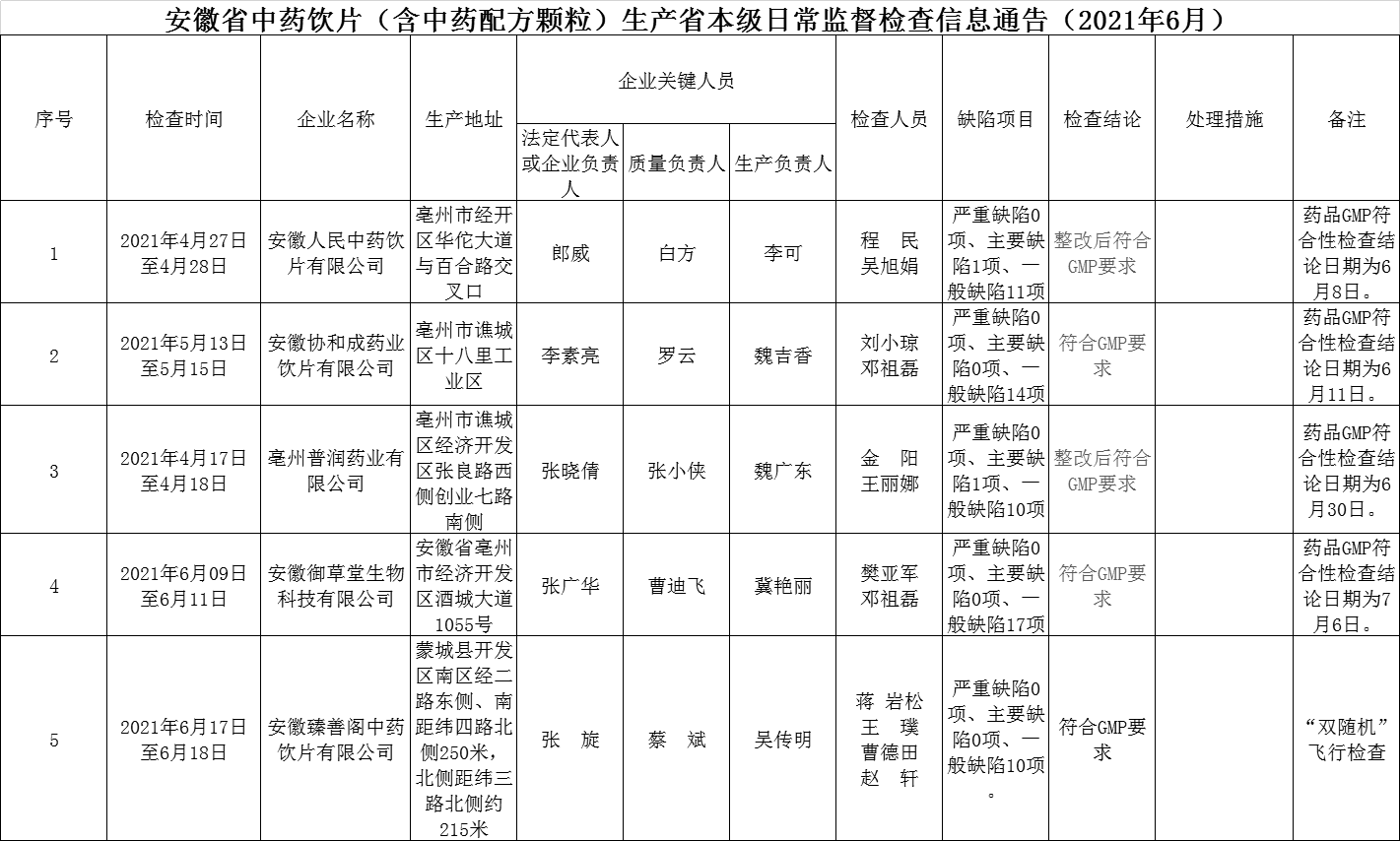
3.安徽省药监局发布安徽省中药饮片(含中药配方颗粒)生产省本级日常监督检查信息通告(2021年6月),涉及5家企业。检查结果如下:
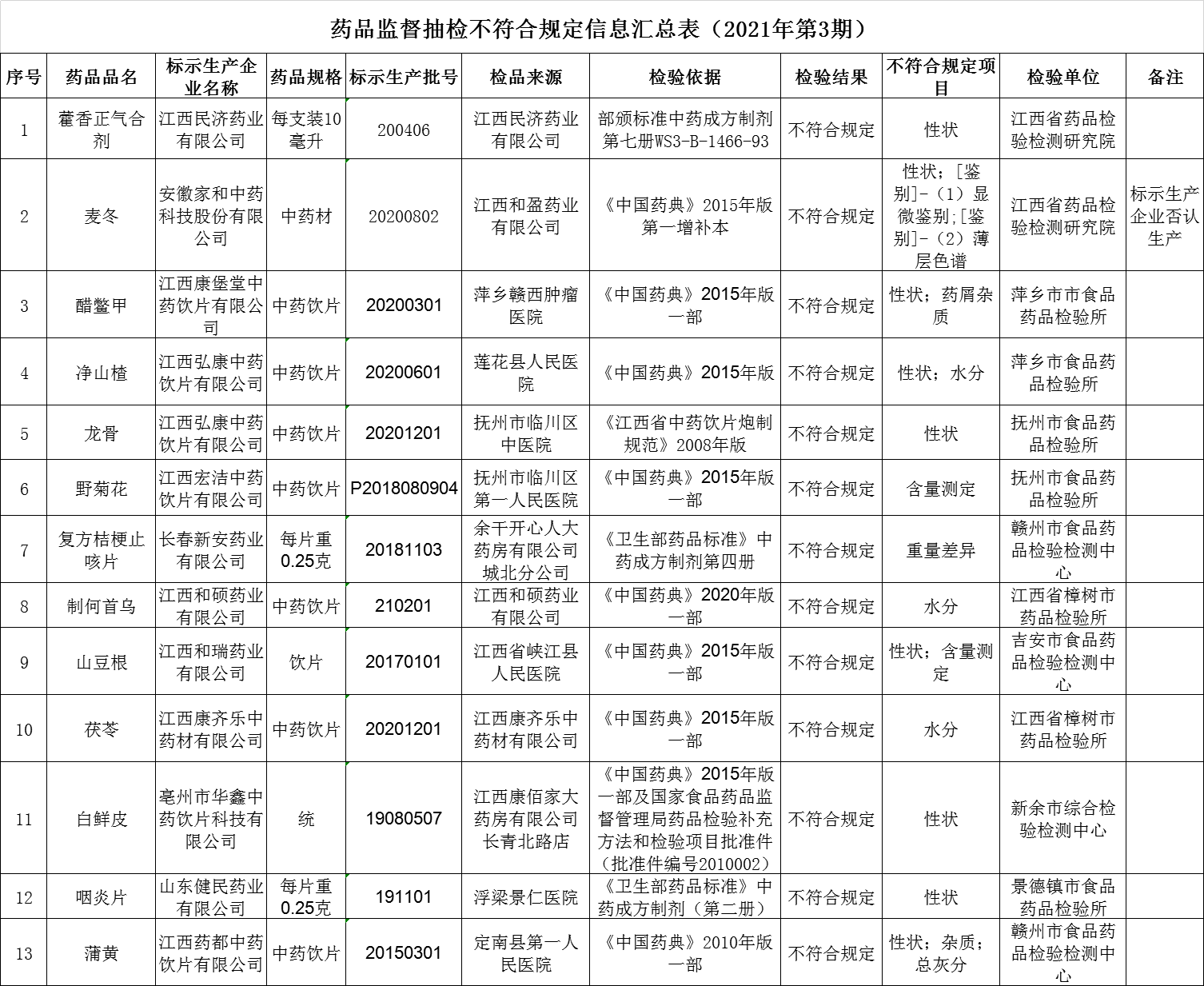
4.江西省药监局发布2021年第3期药品监督抽检信息公告。公告显示,麦冬、醋鳖甲等13个药品品种共13批次不符合规定,不符合规定项目包括性状、水分、重量差异、含量测定等。具体项目如下:
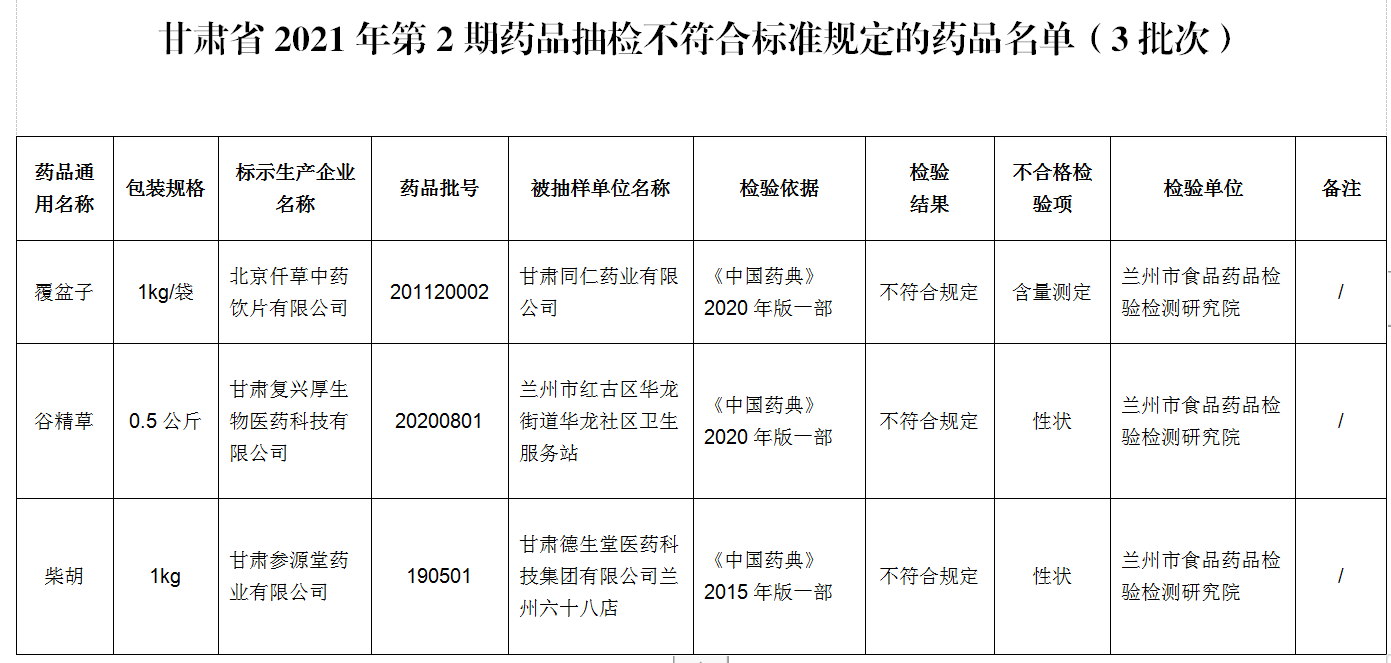
5.甘肃省药监局发布2021年第2期药品质量公告。公告显示,标示为北京仟草中药饮片有限公司等3家企业生产的3批次药品不符合标准规定。不合格产品名单如下:
(中国食品药品网 陆悦/整理)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:陆悦)
分享至
右键点击另存二维码!
-
为你推荐
-

药品管理法实施条例大家谈|中药饮片监管迎来哪些变化
新修订《中华人民共和国药品管理法实施条例》(以下简称《实施条例》)细化完善了中药饮片研制、生产、销售、使用、标签等管理制度,增加了履行药品上市许可持有人(以下简称持有人)义务、禁止... 2026-05-14 16:53 -

药监部门是否应告知举报人不予立案决定
《市场监督管理投诉举报处理办法》(以下简称《处理办法》)已于4月15日起正式施行。该办法在《市场监督管理投诉举报处理暂行办法》(以下简称《暂行办法》)基础上作出较大幅度修订。其中,删... 2026-04-22 14:58
互联网新闻信息服务许可证10120170033
网络出版服务许可证(京)字082号
©京公网安备 11010802023089号 京ICP备17013160号-1
《中国医药报》社有限公司 中国食品药品网版权所有