每周医药看点(7.23—29)
- 2021-07-30 15:44
- 作者:刘思慧
- 来源:中国食品药品网
中国食品药品网讯 国家药监局发布《关于药械组合产品注册有关事宜的通告》,明确药械组合产品申报注册、属性界定、审评审批相关内容和要求;发布第四十三批仿制药参比制剂目录;国家卫生健康委办公厅印发《关于规范开展药品临床综合评价工作的通知》,同时配发《药品临床综合评价管理指南(2021年版 试行)》……7月23日-29日,医药行业的这些事情值得关注。
行业政策动态
1.国家药监局发布《关于药械组合产品注册有关事宜的通告》,明确药械组合产品申报注册、属性界定、审评审批相关内容和要求。《通告》自发布之日起实施。
2.国家药监局再次就《医疗器械注册自检工作规定(征求意见稿)》公开征求意见。征求意见截止时间为7月31日。与上一次征求意见稿相比,此次发布的《征求意见稿》从检验能力、管理体系、自检依据标准等方面突出强调了医疗器械注册自检能力要求。
3.国家药监局发布第四十三批仿制药参比制剂目录,涉及他克莫司注射液等药品。
4.国家药监局决定对维生素B6注射剂说明书【不良反应】【禁忌】等项目进行统一修订。其中,维生素B6注射液说明书【不良反应】项应增加,上市后药品不良反应监测发现本品有以下不良反应/事件报告:全身性反应、皮肤及其附件、胃肠系统、神经精神系统等;【禁忌】项应增加对本品及所含成分过敏者禁用。
5.国家卫生健康委办公厅印发《关于规范开展药品临床综合评价工作的通知》,对各地和各类医疗卫生机构药品临床评价工作进行部署;同时配发《药品临床综合评价管理指南(2021年版 试行)》,明确药品临床综合评价具体流程、内容与维度,聚焦技术评价与政策评价两条主线,从安全性、有效性、经济性、创新性、适宜性、可及性6个维度开展科学规范的整合分析与综合研判。
6.国家药监局药审中心(CDE)就《“风险分析与管理计划”撰写指导原则(征求意见稿)》公开征求意见。《征求意见稿》以国际人用药品注册技术协调会指导原则《E2E:药物警戒计划》的要求和建议为基准,结合中国上市许可申请审评过程中对风险评价的考虑和关注重点,阐述“风险分析与管理计划”撰写的一般考虑和原则,并提供了撰写模板。征求意见截止日期为8月22日。
7.CDE就《体重控制药物临床试验技术指导原则(征求意见稿)》公开征求意见,以鼓励和推动体重控制药物研发。征求意见截止日期为8月22日。
8.国家药典委公示3个药用辅料标准草案,分别为共聚维酮、三氯蔗糖和蔗糖硬脂酸酯;公示2个国家药品标准草案,分别为补天灵片和复方鱼腥草合剂标准草案。上述公示期均自发布之日起3个月。
产品研发/上市信息
1.国家药监局发布2期药品批准证明文件待领信息,共包括151个受理号,涉及罗氏(中国)投资有限公司等企业。(截至7月29日)
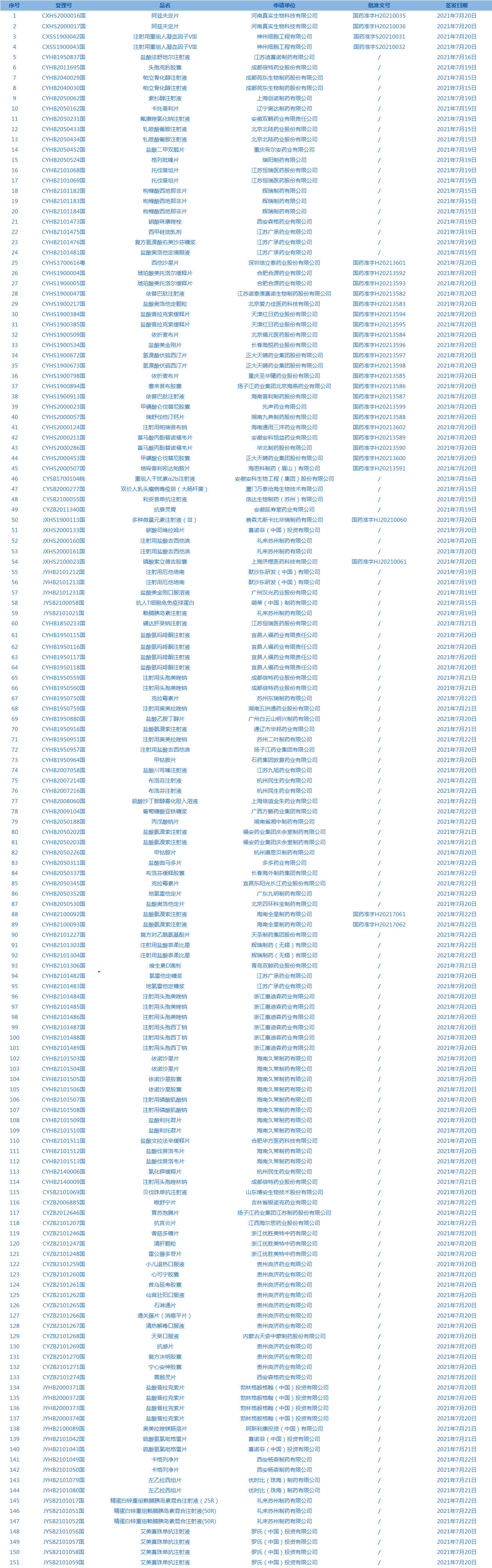
2.国家药监局发布3期医疗器械批准证明文件(准产)待领信息,共包括72个受理号,涉及浙江信纳医疗器械科技有限公司等企业。(截至7月29日)
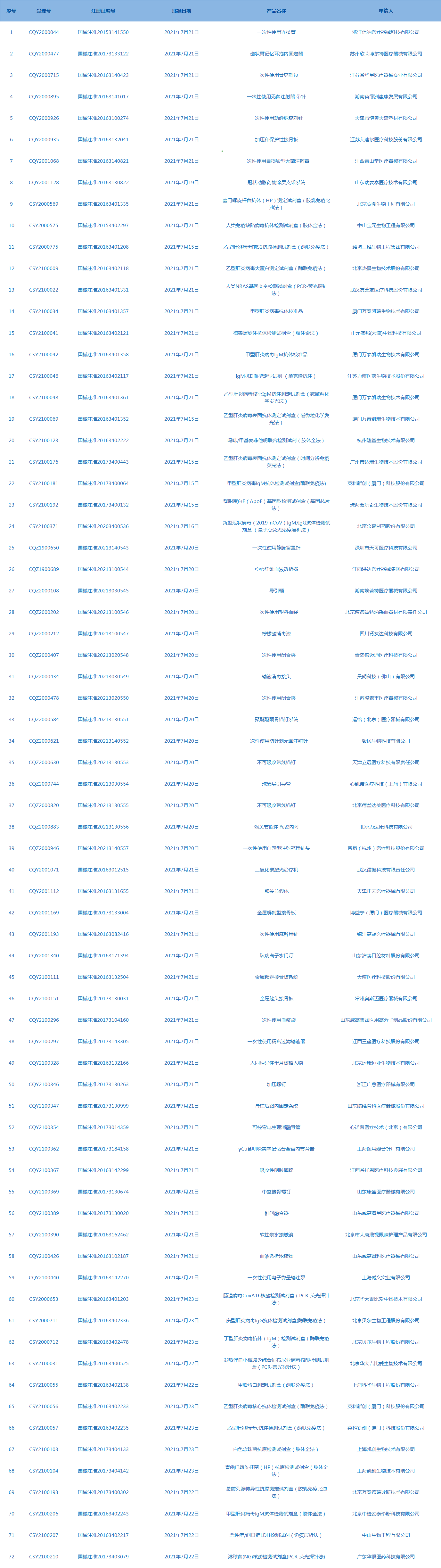
3.CDE网站公示17个仿制药一致性评价任务,涉及注射用头孢他啶等药品。(截至7月29日)
4.CDE承办受理44个新药上市申请,包括重组抗PD-1人源化单克隆抗体注射液等药品。(截至7月29日)
医药企业观察
1.石四药集团发布公告,该公司全资附属石家庄四药作为买方与卖方天津乾鼎企业管理合伙企业(有限合伙)订立收购协议,买方已同意购买而卖方已同意出售辰欣药业2766.14万股目标股份,相当于辰欣药业6.1015%股权,总代价为3.54亿元人民币,即每股目标股份人民币12.8元,较目标公司股份于紧接收购协议日期前一个交易日在上交所所报的收市价每股人民币12.15元溢价约5.35%。
2.药明康德子公司合全药业与诺诚健华达成战略合作协议。根据协议,合全药业将成为诺诚健华首选CDMO合作伙伴,为诺诚健华在研及后续管线产品(包括小分子药物、多肽、寡核苷酸、复杂化学偶联药物等)提供原料药研发及委托生产服务,包括但不限于原料药的工艺开发、生产、分析,以及支持新药申报的注册文件准备等。
3.海南普利制药与中国科学院高能物理研究所签署了《共建医药创新技术中心合作协议》,双方将优势互补、互惠共赢,聚焦于硼中子药物、mRNA核酸药物、纳米多肽药物、蛋白药物以及靶向递送系统等领域,开发面向重大疾病防治领域的医药创新药物并进行战略合作,成立医药创新技术中心。
4.江苏恩华药业与比利时Complix NV公司签署了《药物开发与许可协议》,双方将合作利用Complix专有的细胞跨膜抗体“CPABs”技术平台,针对中枢神经领域的药物靶点进行创新生物药的研发。
5.蓝帆医疗宣布以自有资金5亿元人民币在上海设立全资子公司蓝帆医疗(上海)有限公司,主要承载全球创新研发总部基地、投资孵化平台、高端医疗器械生产、全球商业总部的建设。
6.华仁药业全资子公司拟收购西安恒聚星医药有限公司暨安徽恒星制药有限公司100%股权。本次收购事项的交易对价为8亿元人民币。
7.柳州医药与上海康达卡勒幅医疗科技股份有限公司签署了《合资经营协议》,拟共同投资设立广西康达卡勒幅医疗科技有限公司(暂定名,最终以登记机关核准的名称为准)。目标公司注册资本为人民币5,000万元,公司以自有资金出资2,500万元,占目标公司注册资本的50%。
8.安徽中科拓苒宣布,已完成近亿元人民币的A轮融资,此次融资将用于加速推进该公司相应产品管线的开发。本轮融资由安徽省科技成果转化基金、中科国元基金、安元创新基金、上海山蓝资本等多家投资机构共同参与。
9.嘉越医药已完成逾3亿元B轮融资,本轮融资由国投创业和红杉资本中国基金共同领投,领承创投和乡融资本跟投。本轮融资将用于创新药管线多项后期临床和中期临床项目的推进。
10.广州麓鹏制药完成3500万美元Pre-B轮融资,本次融资由淡马锡领投,清池资本、礼来亚洲基金、丰川资本等跟投。本轮募集资金将用于其BCL-2抑制剂LP-108、LP-118、LP-168等多款在研产品的临床研究以及多个临床前项目的开发。
11.赞荣医药宣布完成4000万美元B轮融资,本轮融资由奥博资本领投,原有股东启明创投、夏尔巴投资、聚明创投、幂方资本持续跟投。本轮融资资金将用于持续自主开发项目的临床研究、临床前研究和人才引进。
药械集中采购
1.四川省医疗保障局就《关于进一步做好我省基本医疗保险、工伤保险和生育保险地方调增乙类药品消化工作的通知(征求意见稿)》公开征求意见,明确丁硼软膏剂等145种药品于2022年1月1日起不再纳入四川省基本医疗保险、工伤保险和生育保险支付范围。上述药品在调出前,继续按规定予以支付。
2.浙江省医疗保障局等5部门印发《浙江省药品医用耗材集中带量采购暂行办法》,将探索建立省级统筹、省市联动、市级联合的具有浙江特色的集中带量采购新模式。
3.甘肃省药品和医用耗材集中采购网发布《甘陕联盟2021年度药品集中带量采购文件》,将优先遴选医保目录内采购金额高、临床使用成熟、可替代性强、市场竞争充分等类型的化学药品进行集采,涉及51个品规。此次集采药品不区分质量层次,按照医保类型分两组采购,每组确定1家企业中选,约定采购量为计算基数的50%,中选药品价格降幅超过50%的,每多2个百分点增加1%的约定采购量,最多不超过计算基数的70%。最终通过综合评分和议价谈判的方式产生中选结果。【中国食品药品网综合整理/刘思慧】
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
为你推荐