改良型新药市场进入高速增长期——临床更优效 研发更高效 回报更迅速
- 2022-11-14 14:04
- 作者:弗若斯特沙利文
- 来源:中国医药报
由于具有研发风险较低、研发周期短、回报率高等特点,改良型新药赛道逐渐受到行业关注。获益于更好的安全性、有效性和依从性,并且在以临床价值为导向的药品审评审批制度改革、新型制剂技术升级等因素影响下,改良型新药市场规模快速增长。
兼具临床优效性和研发优势
改良型新药指在已知活性成分的基础上,对其结构、剂型、处方工艺、给药途径、适应症等进行优化后,具有明显临床优势的药品,要求境内外均未上市,属于化学药品注册分类第2类。改良型新药划分为四个细分类别:2.1类,包括光学异构体,成酯,成盐,酸根、碱基或金属元素,其他非共价键衍生物等;2.2类,包括新剂型、新处方工艺、新给药途径等;2.3类,即新复方制剂;2.4类,即新适应症。
>>在临床需求方面,改良型新药具有明显的临床优势,有助于增强药物有效性、安全性及患者依从性。
改良型新药是对已上市药品的升级改良,强调“优效性”,相较于被改良的药品,具有增强药效、降低副作用、提高患者的服药依从性等明显临床优势。在增强药物有效性方面,改良型新药可以通过优化目标化合物结构或优化剂型提升药效。通过对化合物结构上的优化,例如对已知活性成分成酯改善药物的稳定性及延长半衰期、对已知活性成分增加药物的溶解度等;制剂的优化包括使用纳米制剂、缓控释制剂、口腔膜剂等新型制剂提升生物利用度。在增强药物安全性方面,改良型新药可在不增加新的安全性风险的基础上降低现有治疗方式的风险。例如,紫杉醇白蛋白纳米粒的血液毒性、消化道毒性和神经毒性均低于紫杉醇注射液及紫杉醇脂质体,显著降低了过敏发生率,提升了药物安全性。在增强患者依从性方面,改良型新药注重通过给药系统、制剂类型的改变,更加方便患者使用。例如,帕洛诺司琼胶囊会因患者呕吐症状影响药效发挥,且易使患者对服药产生抗拒心理;而改良后的口腔膜剂不会因呕吐症状而脱落,用药方式友好且使用场景灵活,患者依从性更好。
>>在药物研发方面,改良型新药具备低成本、高回报、生命周期长的显著优势。
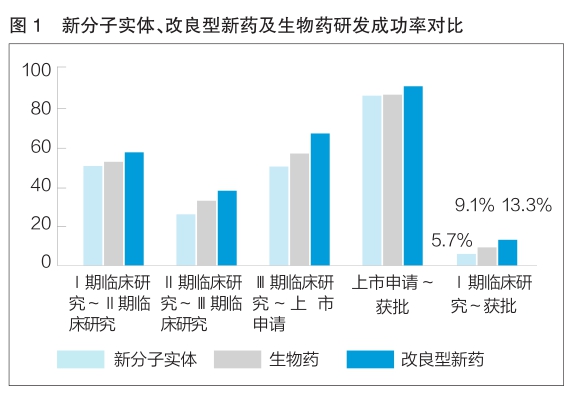
与创新药相比,改良型新药的研发投入较低,且具有较高的研发成功率,选择开发改良型新药的企业承担的研发风险更小。此外,研发创新药需要开展大量临床前研究和临床试验,耗时长且资金投入巨大;而研发改良型新药可以不必重复大量临床试验来证明其安全性和有效性,大大缩短研究时间并降低资金投入,因此改良型新药上市速度更快,有利于抢占市场先机。根据Biotechnology Innovation Organization数据,在研发成功率方面,改良型新药是新分子实体的2.3倍,研发费用和研发时间也均远少于新分子实体。
与仿制药相比,改良型新药具备较高的专业壁垒,如需要更加复杂的制造工艺等;此外,改良型新药有更长的市场独占期,生命周期明显拉长,因此可以避免过于激烈的市场竞争,获得更高的回报。
对创新药的原研厂家而言,研发改良型新药可对原有专利进行补充,从而延长专利保护期;而对其他企业而言,通过研发申报改良型新药,可以快速占据市场份额,是将自身技术优势转化为市场优势的重要手段。
迎来研发和上市浪潮
在过去5年间,改良型新药领域掀起研发浪潮,临床试验申请数量呈逐年增加趋势,2021年获批临床试验申请数量是2017年的8.5倍。临床试验申请数量居于前五位的企业,既包括专注于改良型新药赛道的创新药企,也包括大型药企。专注于改良型新药企业产品多为2.2类新剂型,如力品药业;而大型药企如恒瑞、强生等,除2.2类新剂型外,还有一部分2.3类新复方制剂产品。
据国家药监局药品审评中心相关数据统计,截至今年8月,已有107个改良型新药处于临床试验阶段。从注册分类来看,2.2类新剂型为主流,2.1类改结构产品和2.3类新复方制剂相对较少;从治疗领域看,主要集中在神经系统相关疾病,主要原因是神经疾病领域患者对于用药依从性和安全性要求更高,更易接受改良型新药。
截至今年8月,已有24个2.1类、2.2类、2.3类化学改良型新药获批上市。整体而言,治疗领域集中在抗感染、抗肿瘤及精神障碍类疾病。从注册分类上看,2.2类占比最大,2.1类和2.3类占比较少。主要原因是,2.1类改结构产品较难筛选出合适的药物活性成分,需要药物活性成分本身与异构体在药效或毒副反应方面存在差异并通过临床试验证实优势;2.3类新复方制剂也并非简单的“1+1=2”,面临制剂工艺技术壁垒高、杂质成分分析难等挑战。
>>2.1类改良型新药在研和上市情况
截至今年8月,在研2.1类改良型新药共计15个。1/3在研药物在开发时就考虑申报特殊剂型,注册路径为“2.1+2.2”类或 “2.1+2.2+2.4”类。主要原因是研发方考虑改结构不一定满足临床优效,以及避免上市后集采被并组。药企在立项时,可参考恒瑞医药硫酸氢伊伐布雷定缓释片的“2.1+2.2”类申报策略,即可规避化合物晶型专利期限制,将普通固体口服制剂改为缓释制剂,也减少了集采并组几率。
截至今年8月,3个2.1类改良型新药已获批上市,其中两个药物的活性成分为左奥硝唑。左奥硝唑是奥硝唑的左旋体,金药源药物研究院研发的左奥硝唑氯化钠注射液的立题依据为降低奥硝唑中枢神经系统的毒性反应。临床数据表明,左奥硝唑在抗厌氧菌感染方面的疗效与奥硝唑相当,总不良反应发生率明显低于奥硝唑,因此具有明显的临床优势。
>>2.2类改良型新药在研和上市情况
截至今年8月,在研2.2类改良型新药共计77个。从剂型上看,常见的注射剂、缓释/控释片以及口服液体制剂占比较多。
从临床试验来看,在研药物中仅有2个药物做生物等效性(BE)试验,均为口溶膜剂型。由于BE试验结果并不一定能证明药物具有临床优势,预计未来改良型新药仅通过BE试验来支持上市的难度会增大。
从治疗领域来看,神经系统相关疾病治疗药物占比最大,适应症主要为镇痛、镇静、治疗帕金森等疾病;其次为抗肿瘤药物,其中针对化疗药物如紫杉醇、多西他赛、伊立替康作剂型改良的较多,也有针对化疗引起的恶心呕吐的药物作剂型改良的,如力品药业的盐酸帕洛诺司琼口颊膜;此外,眼科药物占比也较大,如阿托品,目前在研的阿托品企业多以2.2类、2.4类或“2.2+2.4”类进行申报。
截至今年8月,共计18个2.2类改良型新药获批上市,主要围绕奥氮平、孟鲁司特、恩替卡韦、紫杉醇、利培酮等大品种作剂型改良。剂型以口溶膜为主,主要原因是口溶膜仅需完成BE试验,研发周期较短。此外,获批药物中也不乏注射剂的创新剂型,如微球、脂质体等。
>>2.3类改良型新药在研和上市情况
截至今年8月,在研2.3类改良型新药共计15个。从治疗领域来看,心血管系统药物、抗感染药物、呼吸系统药物占比较大。心血管疾病患者通常患有并发症,面临耐药性问题,单方制剂往往疗效不佳,需要使用复方制剂以不同机制的药物组合进行治疗。其中,降压药是重点开发的领域,往往以沙坦类、地平类、烟酸为基础组合,如信立泰的SAL0107成分为“阿利沙坦+氨氯地平”。抗感染药物耐药性、耐受性问题突出,也是复方制剂的重点开发领域。呼吸系统药物主要针对慢性阻塞性肺疾病、哮喘等适应症开发复方制剂,往往以糖皮质激素类、β2受体激动剂、抗胆碱能受体进行组合。目前,联合用药已成为慢性阻塞性肺 病治疗的趋势,因此相关复方制剂的开发热度有所上升。
截至今年8月,已有3个2.3类改良型新药获批上市,其中2个为治疗哮喘及慢性阻塞性肺病的吸入制剂。从获批药物完成的临床试验来看,已获批的2.3类改良型新药均进行了较大规模的临床试验。相比之下,2.1类改结构和2.2类改剂型的产品中,部分药物由于能够桥接被改良品种的临床安全性和有效性数据,临床试验速度更快。
多重因素驱动市场持续扩容
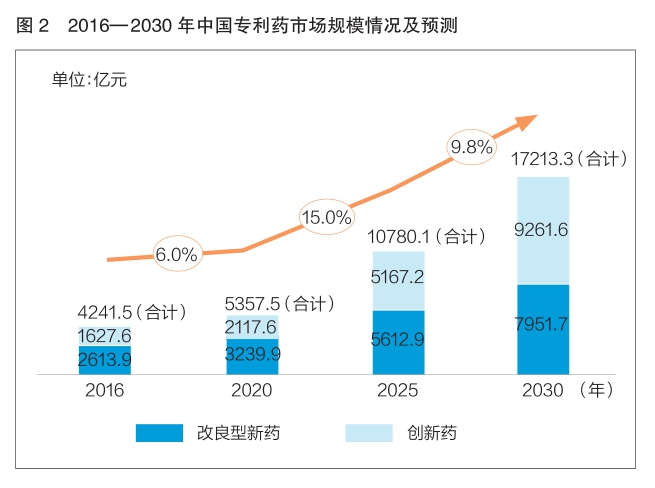
改良型新药在中国医药市场起步较晚,但由于更好的安全性、有效性和依从性,满足了未被解决的临床需求,在技术进步、支付能力提升等因素驱动力下,其市场规模快速增长。2016年至2020年,中国改良型新药市场规模已从2613.9亿元增加到3239.9亿元,年复合增长率(CAGR)为5.5%。预计到2025年,中国改良型新药市场规模将达到5612.9亿元(CAGR=11.6%),并将于2030年达到7951.7亿元(CAGR=7.2%)。
改良型新药市场可分为创新制剂药物及其他改良型新药两大市场。2016年至2020年,中国创新制剂市场规模已从983.7亿元增加至1326.7亿元,CAGR为7.8%。预计创新制剂市场规模增长速度将超过整体改良型新药市场,在2025年达到2458.8亿元(CAGR=13.1%);至2030年,创新制剂市场规模将达到3733.3亿元(CAGR=8.7%)。
改良型新药市场高速增长的驱动因素包括以下四方面:
>>治疗需求的增长与升级
随着中国经济社会发展和卫生健康服务水平的不断提高,人口老龄化进程加快,慢性病患者数量不断扩大。慢性病患者通常需要长时间甚至终身服药,药物的副作用和依从性问题更为突出。改良型新药有助于提高药物疗效,减少用药次数,增强患者依从性,降低副作用,改善安全性,对慢性病患者吸引力巨大。
>>患者支付能力持续提高
随着中国社会经济快速发展,医疗保健消费水平也在稳步提升,人均医疗保健消费支出已从2017年的1451元增长到了2021年的2115元。人们对于疾病治疗有更全面的认知和治疗意愿,从而提高了患者对于药物的支付能力。此外,随着越来越多的药品被纳入国家医保目录,患者的可负担能力及药物可及性进一步提升。
>>创新制剂技术进步
制剂药物递送系统涉及制剂技术、药用辅料、给药装置、制剂设备、检测设备和包装材料等多个学科。目前中国已经创建了药物制剂国家工程研究中心,并建立了多个创新制剂平台,包括激光打孔渗透泵控释片、缓释微粒、缓释混悬剂、生物黏附制剂、经皮给药制剂、长效注射微球、注射用脂质体等技术平台,并设计制造了相应的设备和生产线,同时重点加强对渗透泵、微孔膜、长效缓释、靶向、定时脉冲等国际先进剂型及相关辅料的研究。中国创新制剂技术整体水平持续提高,与国际先进水平差距逐步缩小,从而能够持续支撑我国改良型新药行业稳步发展。
>>有利的政策驱动
当前,中国药品审评审批制度改革以鼓励创新和重视临床价值为导向,仿制药质量和疗效一致性评价、药品上市许可人制度等政策的实施,有力激发了医药行业的创新热情。
2020年12月,国家药监局药品审评中心发布《化学药品改良型新药临床试验技术指导原则》,进一步明确改良型新药的临床优势,对改良型新药做出明确的临床试验路径指导。在国家利好政策的驱动下,改良型新药的研发将驶入快车道,带动医药行业整体技术水平不断提升。
(弗若斯特沙利文供稿)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:陆悦)
分享至
右键点击另存二维码!
-
为你推荐