每周医药看点(7.19—7.25)
- 2023-07-27 09:28
- 作者:刘思慧
- 来源:中国食品药品网
中国食品药品网讯 六部门联合印发《深化医药卫生体制改革2023年下半年重点工作任务》;国家药监局修订《药品检查管理办法(试行)》部分条款……7月19日—7月25日,医药行业的这些动态值得关注。
行业政策动态
1.国家卫生健康委、国家发展改革委、财政部、人力资源社会保障部、国家医保局、国家药监局联合印发《深化医药卫生体制改革2023年下半年重点工作任务》,明确2023年下半年深化医改的重点任务和工作安排。这些重点工作任务主要包括促进优质医疗资源扩容和区域均衡布局、深化以公益性为导向的公立医院改革、促进多层次医疗保障有序衔接、推进医药领域改革和创新发展、健全公共卫生体系、发展壮大医疗卫生队伍。
2.国家药监局发布关于修订《药品检查管理办法(试行)》部分条款有关事宜的通知。此次主要修改完善了第三章《检查程序》和第九章《检查结果的处理》等有关条款,经过修订后,现场检查结论和综合评定结论均不再有“基本符合要求”。
3.国家药监局发布公告,银黄含片等4种药品转换为非处方药。品种名单及非处方药说明书范本一并发布。
4.国家医保局公布《谈判药品续约规则》及《非独家药品竞价规则》。《谈判药品续约规则》提出,对达到8年的谈判药纳入常规目录管理;对未达8年的谈判药,连续协议期达到或超过4年的品种以简易方式续约或新增适应证触发降价的,降幅减半。
5.国家药监局药品审评中心发布《其他来源于古代经典名方的中药复方制剂药学研究技术指导原则(试行)》。指导原则主要围绕其他来源于古代经典名方的中药复方制剂的特点,明确药学研究的一般要求。药材、饮片、制备工艺、质量标准等具体研究工作应当参照相关技术指导原则开展。
6.国家药监局药品审评中心发布《中药新药临床试验用药品的制备研究技术指导原则(试行)》。指导原则旨在为中药创新药、中药改良型新药等中药新药临床试验用药品(包括试验药物、安慰剂)的制备、质量控制等研究提供技术指导,以保证临床试验用药品质量,满足临床试验需求。
7.国家药监局药品审评中心就《腺相关病毒载体类体内基因治疗产品临床试验申请药学研究与评价技术指导原则(征求意见稿)》《放射性标记人体物质平衡研究技术指导原则(征求意见稿)》《细胞和基因治疗产品临床相关沟通交流技术指导原则(征求意见稿)》公开征求意见,征求意见时限均为自发布之日起1个月。
8.国家药监局药品审评中心网站公示21个仿制药一致性评价任务,涉及注射用头孢呋辛钠等药品。(截至7月25日)

产品研发上市信息
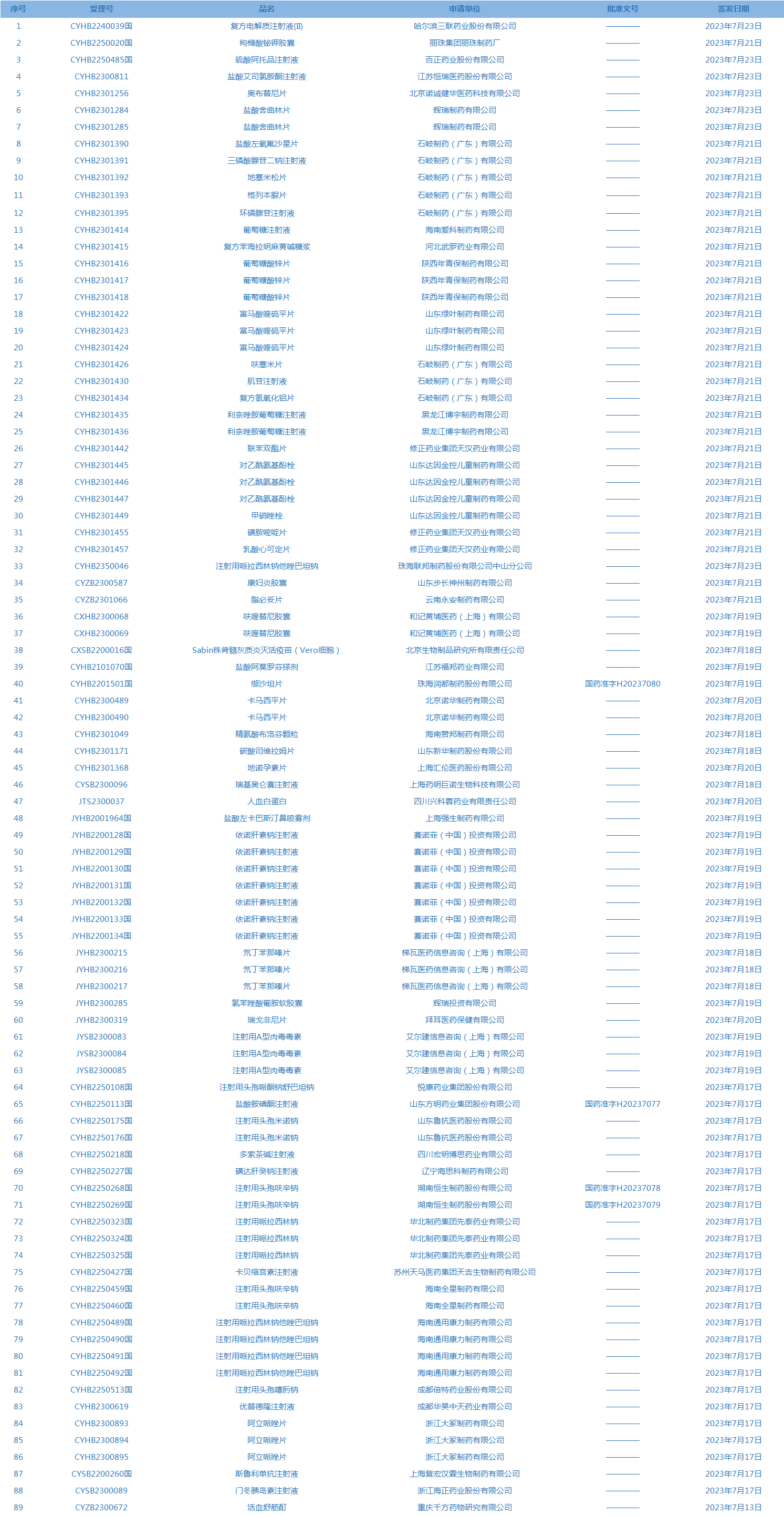
1.国家药监局发布3期药品批准证明文件送达信息,共包括89个受理号,涉及哈尔滨三联药业股份有限公司等企业。(截至7月25日)
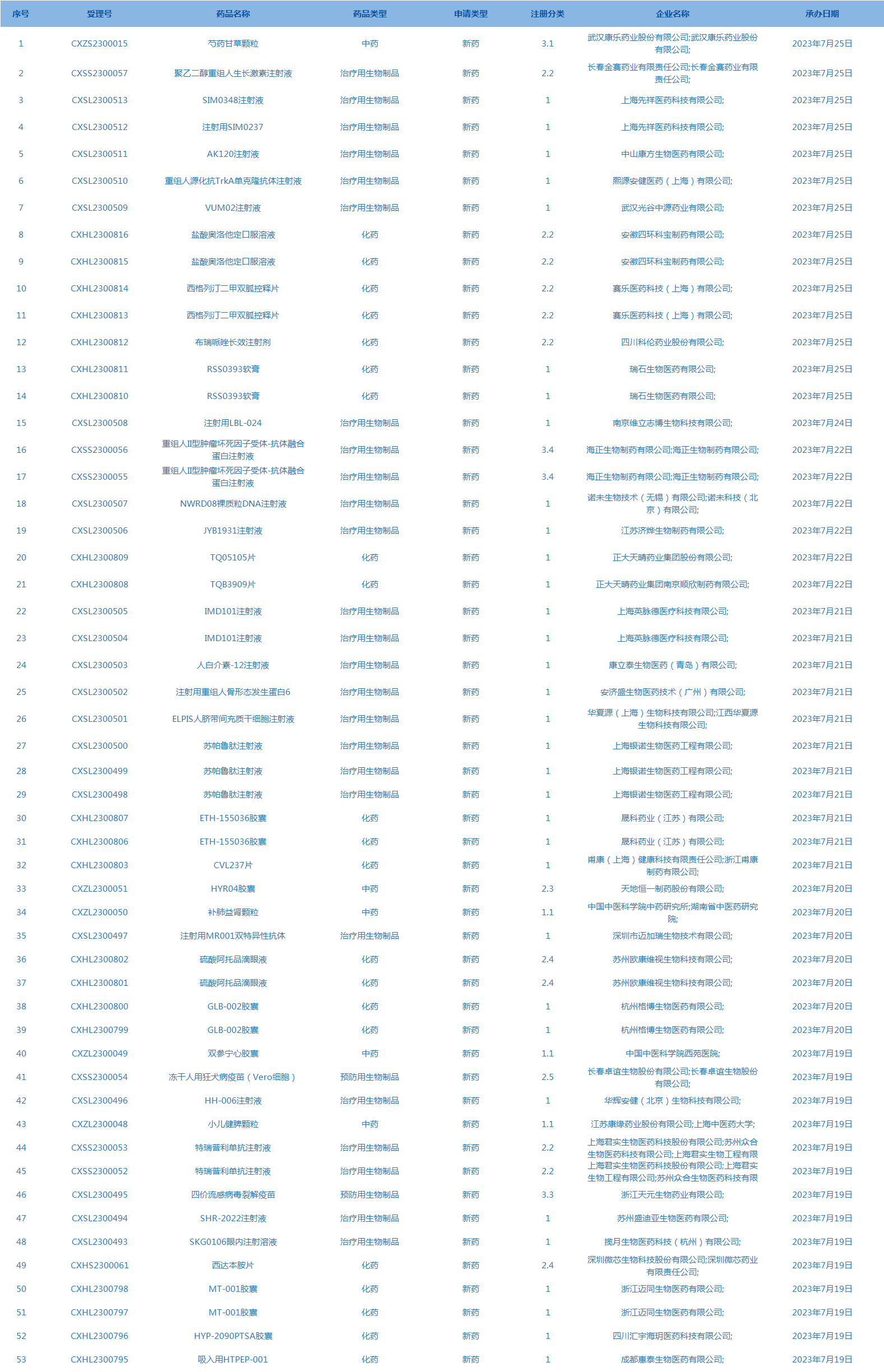
2.国家药监局药品审评中心承办受理53个新药上市申请,包括SIM0348注射液等药品。(截至7月25日)
3.康希诺生物发布公告称,公司收到加拿大卫生部关于重组带状疱疹疫苗(腺病毒载体)临床试验申请的无异议函。
4.汇宇制药发布公告称,公司收到芬兰药品管理局(FIMEA)颁发的GMP证书,认证范围为小容量注射剂、冻干粉针剂、无菌粉剂、无菌原料药。
5.普利制药发布公告称,公司收到加拿大卫生部签发的注射用比伐芦定的上市许可。
6.百济神州发布公告称,欧洲药品管理局(EMA)人用药品委员会(CHMP)发布其推荐百泽安®(替雷利珠单抗注射液)获得上市许可的积极意见,建议批准百泽安®单药治疗用于治疗既往接受过含铂化疗的不可切除、局部晚期或转移性食管鳞状细胞癌(ESCC)成人患者。
7.健友股份发布公告称,其子公司健进制药收到美国食品药品管理局(FDA)签发的注射用亚叶酸钙,USP,50mg/瓶,100mg/瓶,200mg/瓶,350mg/瓶和500mg/瓶,单剂量的ANDA批准通知(ANDA号:216590)。
医药企业观察
1.艾德生物宣布与AstraZeneca UK Limited的子公司KuDOS PharmaceuticalsLimited(以下简称阿斯利康)签署合作协议。根据协议,艾德生物自主研发的人类同源重组修复缺陷(HRD)检测产品将作为阿斯利康PARP抑制剂利普卓®(奥拉帕利片)卵巢癌适应证在中国的伴随诊断,并将积极推进HRD检测产品在中国的注册上市。
2.苑东生物发布公告称,公司拟以全资子公司苑东生物投资管理(上海)有限公司作为投资主体对上海超阳实施1000万元人民币的增资。本次增资完成后,公司将间接持有上海超阳14.29%的股权,上海超阳成为公司的参股公司;上海超阳对外转让相关技术或产品,公司具有优先购买权;且上海超阳承诺不直接从事与公司研发、生产、销售的技术或产品相同的业务。
3.普米斯生物宣布与BioNTech公司达成战略研究合作、项目引进选择以及全球许可协议。根据协议条款,BioNTech公司将获得普米斯生物用于治疗恶性肿瘤的一款临床前研究阶段双特异性抗体和一款临床研究阶段单克隆抗体的全球独家选择权。普米斯生物将获得BioNTech公司提供的预付款,并在BioNTech公司选定临床前研究阶段双特异性抗体后,获得临床研究、注册和商业里程碑付款以及分级销售提成。
4.丽珠集团宣布与华汇拓医药签署专利及技术转让协议。根据协议,华汇拓医药同意将其研发的HHT120项目在大中华区内的所有权利、所有权和权益转让并转移给丽珠集团。丽珠集团需向华汇拓医药支付相应的专利及技术转让费(包括首付款、开发里程碑金)及销售提成。
5.罗欣药业发布公告称,公司控股子公司山东罗欣拟以债转股方式对其全子公司裕欣药业增资人民币7.5亿元。本次增资完成后,裕欣药业的注册资本由人民币5000万元增加至8亿元,山东罗欣仍持有裕欣药业100%股权。
6.高维医药宣布完成数千万人民币的天使轮融资,本轮融资由贝达生物医药产业基金、西湖创新投资等多家投资机构联合投资。本轮融资的资金将主要用于支持高维医药建立高维生物学驱动的创新药发现平台,满足为癌症、神经退行性疾病等重大疾病提供创新药物解决方案的研发投入及申报推进的需求。
药品集中采购
1.湖南省医保局发布《关于开展2023年省际药品价格联动挂网工作的通知(征求意见稿)》。该征求意见稿显示,本次联动挂网后,将对挂网药品价格进行全面梳理,对同通用名同剂型下挂网价格差异较大药品(化学药品、生物制剂单位可比价超1.8倍,中成药日均费用超3倍)将进行价格纠偏。
2.江西省医保局公示《干扰素省际联盟采购拟集采品种目录》。江西省拟牵头开展干扰素集中带量采购,聚乙二醇干扰素α-2b注射剂、人干扰素α1b注射剂、人干扰素α2a注射剂等14个干扰素品种拟纳入此次省际联盟集采。
(刘思慧整理)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐













