每周医药看点(10.25—10.31)
- 2023-11-02 09:38
- 作者:刘思慧
- 来源:中国食品药品网
中国食品药品网讯 国家药监局发布《药品说明书适老化及无障碍改革试点工作方案》;国家卫生健康委药物政策与基药司公示《第三批鼓励仿制药品建议目录》;第七十三批仿制药参比制剂目录发布……10月25日—10月31日,医药行业的这些动态值得关注。
行业政策动态
1.国家药监局发布实施《药品说明书适老化及无障碍改革试点工作方案》(以下简称《方案》)。《方案》显示,国家药监局决定在部分口服、外用等药品制剂中开展药品说明书适老化及无障碍改革试点,确定八省(市)为试点省份,并提供三种试点方式,供药品上市许可持有人选择。第一种是提供纸质药品说明书(大字版),药品说明书(大字版)与药品说明书(完整版)内容一致,仅部分项目的字体、格式加大、加粗印制。鼓励同时提供电子药品说明书(完整版)。第二种是提供纸质药品说明书(完整版),同时提供电子药品说明书(完整版)。第三种是提供纸质药品说明书(简化版),同时提供电子药品说明书(完整版)。药品说明书(简化版)应当原文引用药品说明书(完整版)的部分项目,只涉及字体、格式的调整,不对内容进行修改。《方案》还鼓励药品上市许可持有人提供药品说明书、标签的语音播报服务、盲文信息,满足老年人、盲人和其他有视力障碍患者的安全用药需求。
2.国家药监局发布第七十三批仿制药参比制剂目录,涉及盐酸丙卡巴肼胶囊等品种。
3.国家卫生健康委药物政策与基药司公示《第三批鼓励仿制药品建议目录》,目录共有41个品种,包括社会广为关注的罕见病用药氯巴占(片剂、膜剂、混悬剂)等,公示时间为5个工作日。
4.国家药监局药品审评中心(CDE)就《按古代经典名方目录管理的中药复方制剂药学申报资料撰写指导原则(征求意见稿)》《中药制剂稳定性研究技术指导原则(征求意见稿)》《中药特征图谱研究技术指导原则(征求意见稿)》《药物临床试验样本量估计指导原则(征求意见稿)》《治疗慢性心力衰竭药物临床试验技术指导原则(征求意见稿)》公开征求意见。征求意见时限均为自发布之日起一个月。
5.CDE网站公示16个仿制药一致性评价任务,涉及盐酸二甲双胍肠溶胶囊等品种。(截至10月31日)
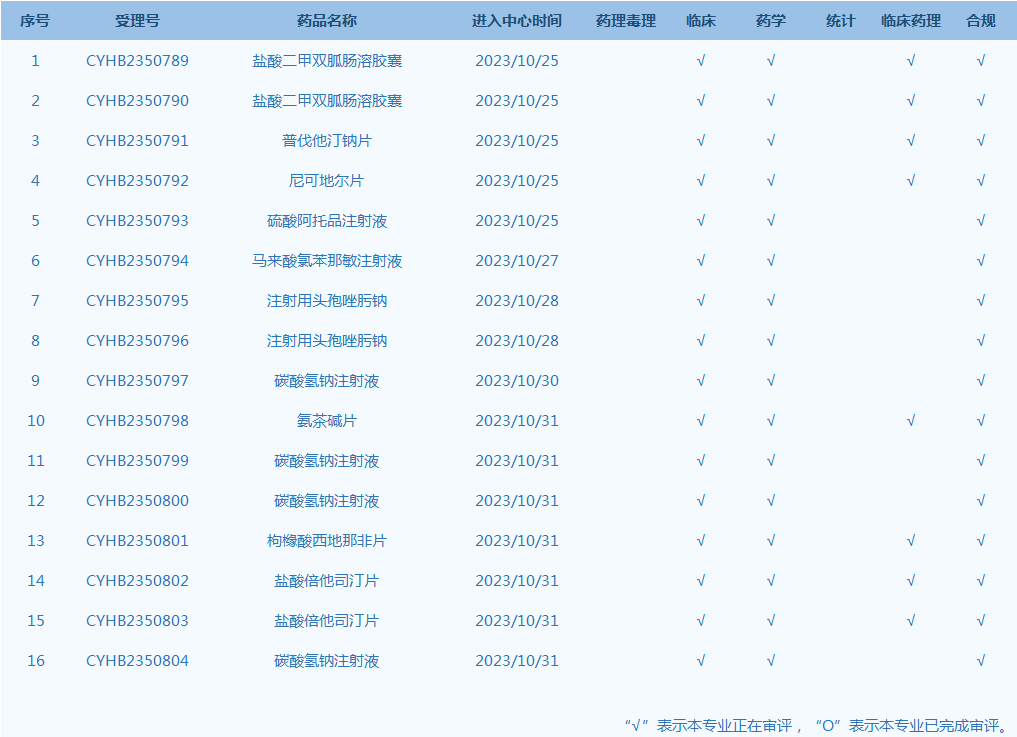
产品研发上市信息
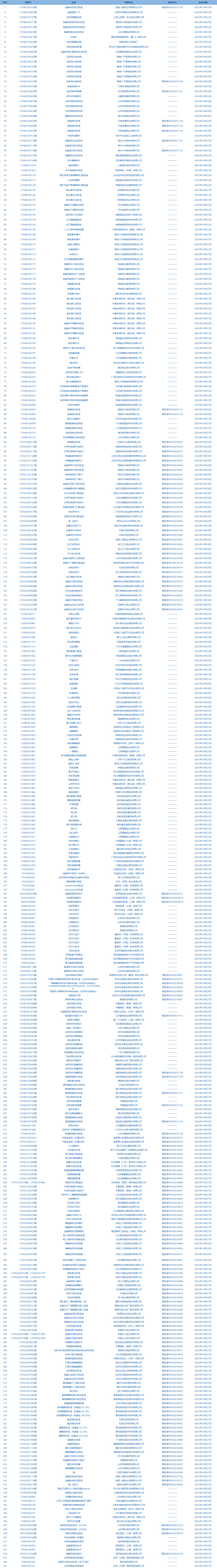
1.国家药监局发布2期药品批准证明文件送达信息,共包括357个受理号,涉及宜昌人福药业有限责任公司等企业。(截至10月31日)
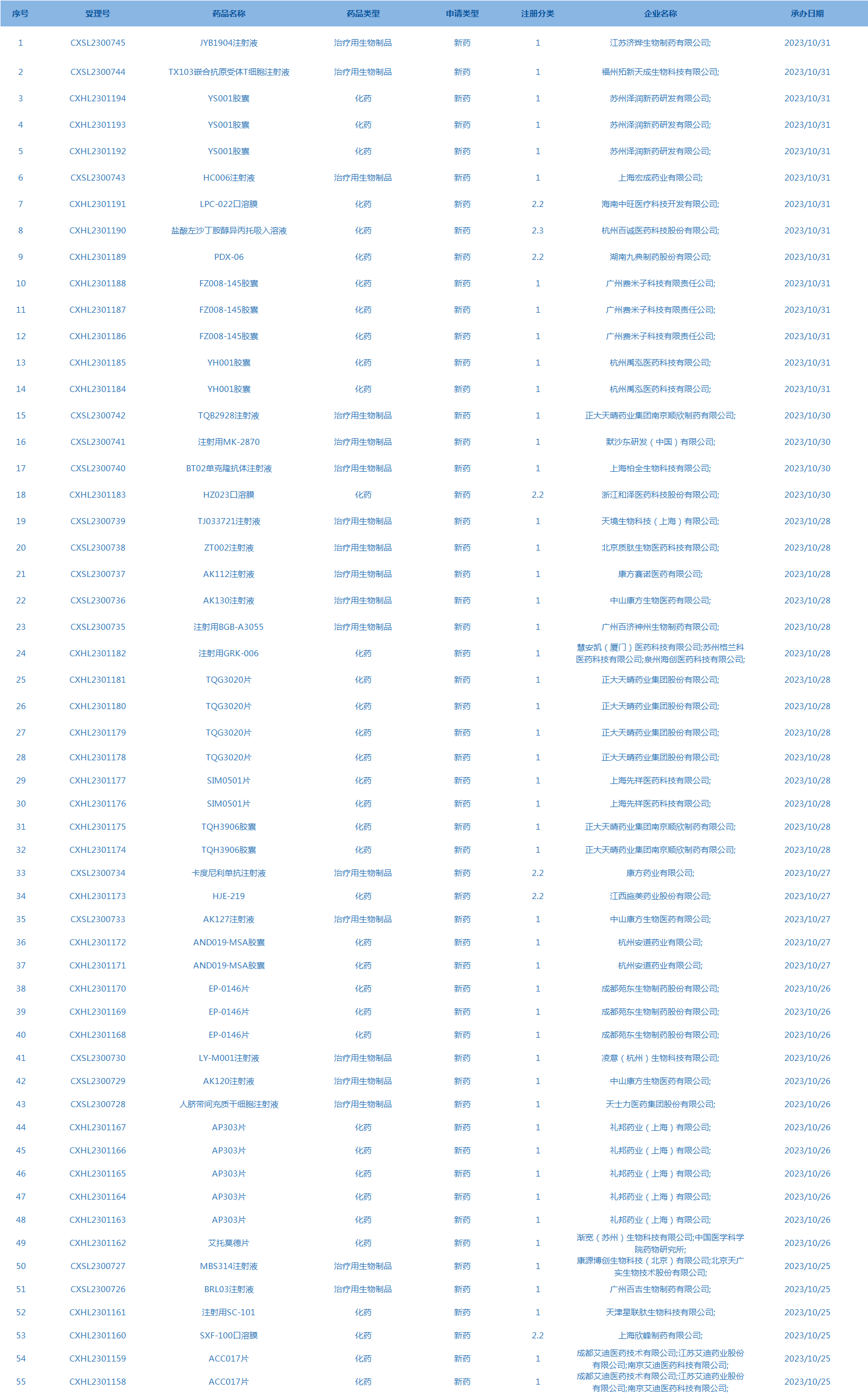
2.CDE承办受理55个新药上市申请,包括JYB1904注射液等药品。(截至10月31日)
3.君实生物与Coherus BioSciences宣布,美国食品药品管理局(FDA)批准其特瑞普利单抗(toripalimab)联合吉西他滨/顺铂作为晚期复发或转移性鼻咽癌(NPC)患者的一线治疗。
4.艾力斯医药宣布,其海外合作伙伴ArriVent Biopharma获得美国FDA授予伏美替尼突破性疗法认定,用于治疗先前未接受过治疗、局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)且伴有表皮生长因子受体(EGFR)20号外显子插入突变患者。
5.劲方医药宣布,其高选择性CDK9抑制剂SLS009(GFH009)获得美国FDA授予快速通道资格,治疗复发/难治性成人外周T细胞淋巴瘤(PTCL)患者。
6.乐普生物宣布,其自主研发的EGFR靶向抗体偶联药物(ADC)产品MRG003获得美国FDA的新药临床试验(IND)批准,用于治疗晚期鼻咽癌(NPC)及晚期头颈鳞癌(HNSCC)。
医药企业观察
1.恒瑞医药宣布与默克公司就其自主研发的PARP1抑制剂HRS-1167达成独家许可协议。该协议还包括恒瑞自主研发的Claudin-18.2抗体药物偶联物(ADC)SHR-A1904的独家选择权。根据协议,恒瑞将获得1.6亿欧元的首付款、高至9000万欧元的技术转移费和行权费、研发里程碑付款、销售里程碑付款,以及高至两位数百分比的销售提成。默克将获得HRS-1167在中国大陆以外的全球范围内开发、生产和商业化的独家权利,SHR-A1904在中国大陆以外的全球范围内开发、生产和商业化的独家选择权,及HRS-1167和SHR-A1904在中国大陆与恒瑞共同商业化的选择权。
2.复宏汉霖宣布与Intas Pharmaceuticals达成合作,授予后者在欧洲和印度对前者开发的抗PD-1单抗H药汉斯状(斯鲁利单抗)包括广泛期小细胞肺癌(ES-SCLC)在内的多项适应证及特定剂型进行独家开发和商业化的权利。根据协议,复宏汉霖将负责斯鲁利单抗在欧洲和印度的临床开发及上市后的产品生产和供应,并将从此次交易中获得4200万欧元的首付款、可达4300万欧元的监管里程碑付款、可达1亿欧元的商业化里程碑付款及两位数比例的合作区域净利润特许权使用费。
3.舶望制药宣布完成3亿元人民币A+轮融资,本轮融资由国投招商领投,华盖资本、元希海河基金、老股东三一创新投资跟投。本轮融资资金将用于进一步推进公司4个临床管线的全球开发、多个临床前候选药物分子(PCC)的发现、修饰技术平台和肝外递送技术平台的迭代升级,以及完善公司的专业团队建设。
4.镔铁生物宣布完成超亿元A轮融资,本次融资由国投创业领投,黄埔医药基金、元希海河基金等共同投资。本轮融资资金将用于加速推进针对KRAS G12V突变的新型TCR-T细胞治疗产品申请注册临床试验,以及多个后续创新管线的产品开发以及国际合作。
药品集中采购
1.山东省医保局发布《关于执行全国中成药联盟集中采购药品中选结果的通知》,《通知》要求,11月15日起,全省参加全国中成药集采的公立医疗机构(含驻鲁军队医疗机构)和医保定点社会办医疗机构,按规定执行全国中成药集采中选结果。按照采购文件要求,非中选药品和流标药品均纳入监控管理。医疗机构采购非中选药品不得超过同采购组实际采购量的10%;确需使用流标药品的,医疗机构实际采购量不得超过医疗机构在本次集采报量的50%。医保目录内的中选药品以中选价格作为医保支付标准,价格高于中选药品价格的非中选药品,医保个人先行自付比例提高10个百分点。
2.北京市医保局发布《关于执行2023年全国中成药联盟采购中选结果有关工作的通知》,《通知》明确,10月31日起,北京市医疗机构全面执行带量采购中选结果。非中选等其他相关药品采购政策,后续按照全国中成药联合采购办公室要求统筹推进。
3.江西省医保局就《十五省(区)联盟药品集中带量采购文件(征求意见稿)》公开征求意见,由该省牵头的15省(区)药品集采即将启动。此次由江西牵头的15省(区)集采联盟地区包括吉林省、黑龙江省、安徽省、河南省、湖北省、广西壮族自治区、贵州省、云南省、西藏自治区、陕西省、青海省、宁夏回族自治区、新疆维吾尔自治区和新疆生产建设兵团。采购周期原则上为2年,购销协议每年一签。集采品种为未过评的20个化学药品。
4.福建省医保局发布《福建省第四批药品集中带量采购公告(第1号)》,公布了该省第四批药品集采文件,包括化学药及中成药两部分。其中,化学药有50个品种,中成药有24组共44个品种。
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐













