王拥军院士团队TASTE-2研究登上《英国医学杂志》 脑细胞保护剂联合取栓显著降低致残
- 2026-01-09 15:04
- 作者:木子
- 来源:中国食品药品网
中国食品药品网讯 近日,中国卒中治疗研究取得重大进展。由首都医科大学附属北京天坛医院王拥军院士团队牵头完成的一项针对缺血性卒中患者的大规模临床研究(TASTE-2),在国际顶级医学期刊《英国医学杂志》(BMJ,IF:42.7)上正式发表全文结果。研究证实,在标准的血管内取栓治疗(EVT)基础上,联用国产创新药依达拉奉右莰醇,可显著提升急性大血管闭塞性卒中患者90天的功能独立比例,且安全性良好。这标志着由中国学者领衔的“脑细胞保护+再灌注”联合治疗方案,获得了国际学术界的高级别认可,为全球卒中治疗提供了新的“中国方案”。

TASTE-2研究2026年1月7日发表于BMJ杂志
卒中是我国成年人致死、致残的首位病因,其中约70%为缺血性卒中(AIS)。目前,急性缺血性卒中治疗已进入“再灌注时代”,血管内取栓是救治大血管闭塞患者的“金标准”。尽管取栓术能实现高达70%-90%的血管再通,但仍有近一半的患者留下不同程度的残疾。如何进一步保护缺血脑组织、降低卒中致残,仍是全球面临的临床难题。
国际权威学术组织STAIR曾提出,缺血性卒中治疗中理想的脑细胞保护策略应能多靶点干预缺血损伤,并与再灌注治疗联合。由中国自主研发的多靶点脑细胞保护剂依达拉奉右莰醇率先在该领域获得成功的临床验证。
该大规模随机双盲对照试验在中国106家中心开展,共纳入1362名患者。所有患者均在发病24小时内接受取栓治疗,并随机分组,在取栓前开始接受依达拉奉右莰醇或安慰剂治疗,持续约两周。
研究主要目标是评估患者90天后的功能独立(改良Rankin量表评分0-2分,即恢复完全生活自理能力)的情况。最终数据显示,相较于安慰剂组,依达拉奉右莰醇显著改善了患者90天功能独立结局,且两组在严重不良事件、死亡率等安全性指标上无显著差别。
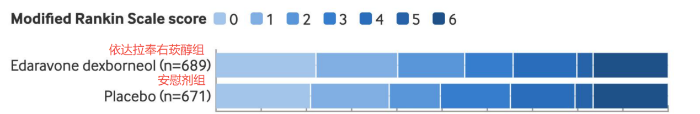
TASTE-2结果显示,患者治疗后恢复功能独立(90天mRS 0~2分)比例上,依达拉奉右莰醇组(55.0%)与安慰剂组(49.6%)相比有显著提高(P=0.047)
值得注意的是,亚组分析显示,入院时影像学与临床症状不匹配的患者可从治疗中获得更明显的获益(55.5%vs42.9%)。这提示,依达拉奉右莰醇在血管内治疗前使用,可能通过减轻缺血再灌注损伤和继发性炎症而发挥“冻结半暗带”的作用。急性缺血性卒中治疗有望从单纯依赖“时间窗”向更精准的“组织窗”评估的重要转变。对于存在明显“不匹配”的患者,积极采取联合治疗(脑细胞保护剂+再灌注治疗)可能带来显著获益。
“TASTE-2研究的结果非常令人鼓舞。”研究第一作者,北京天坛医院王春娟教授表示:“它首次在严格设计的大样本临床试验中证实,在取栓这一强大血流重建基础上,加用多靶点脑保护药物能够进一步为患者带来功能获益。这不仅仅是药物的成功,更代表了一种治疗理念的落地——即‘血管再通’与‘脑细胞保护’协同并重的综合治疗模式,这可能成为未来卒中治疗的新标准。”
依达拉奉右莰醇注射用浓溶液是先声药业有限公司自主研发的多靶点脑细胞保护剂,国家1类新药。该药物含依达拉奉和右莰醇两种活性成分,可高效透过血脑屏障,通过抗炎和清除自由基双效协同,减少脑缺血引发的级联损伤。作为全球卒中治疗领域自2015年以来唯一获批上市销售的创新药,该药物历时12年研发,并两次获得国家“重大新药创制”专项支持。
北京天坛医院王拥军教授团队主导的TASTE研究,以及北京大学第三医院樊东升教授牵头的TASTE-SL研究,分别证实了依达拉奉右莰醇注射剂型,以及舌下片剂型对非取栓AIS患者的疗效。相关数据于2021年和2024年发表在国际神经病学顶级期刊STROKE(《卒中》)和JAMA Neurology(《美国医学会神经病学杂志》),为医学界重启了卒中脑细胞保护研究的大门。依达拉奉右莰醇舌下片也获美国食品药品监督管理局(FDA)突破性疗法认定,是全球卒中治疗领域首个被FDA认定为突破性疗法的创新药。
TASTE-2研究,证实了AIS患者在取栓前使用依达拉奉右莰醇可进一步获益,以新的临床证据不断拓展着科学对“脑细胞保护”的认知。BMJ杂志的高级别临床证据发表,有望推动脑细胞保护相关药物作为取栓等血管内治疗的联合用药,为进一步提升卒中治疗效果,减少卒中致残。(木子)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:郭肖)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐