1月份美国Clinicaltrial数据库临床试验数据显示—— 非小细胞肺癌药物研发最为活跃
- 2026-03-05 15:33
- 作者:陈宇哲
- 来源:中国医药报
根据美国Clinicaltrial数据库数据,今年1月份,全球新开由企业资本主导的临床试验总数为792项,数量较去年12月份下降9.07%;单月新开临床试验数量高于去年同期水平,同比上升22.41%。非小细胞肺癌为1月份最热研发领域。
热门领域分布
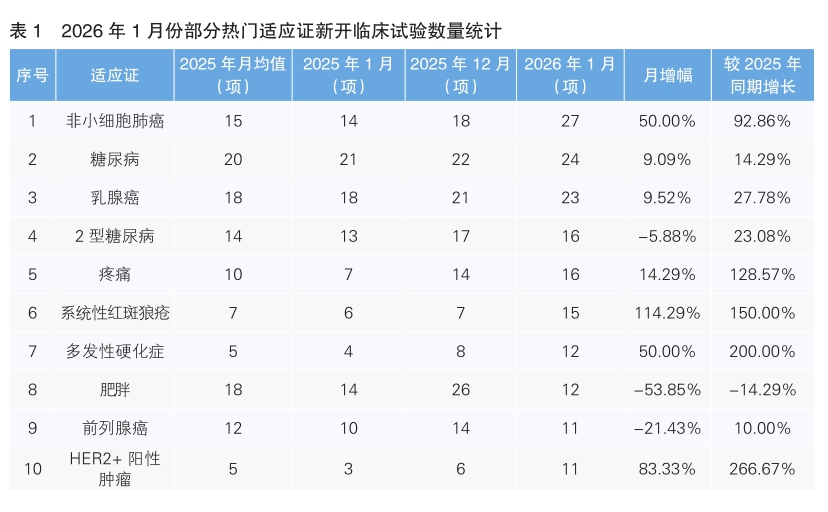
从1月份新开临床试验热门适应证来看,非小细胞肺癌为最热门的研发领域,新开临床试验27项,环比上升50%,同比上涨92.86%。其次为糖尿病,新开临床试验数量为24项,环比上升9.09%,同比上涨14.29%。值得注意的是,1月份新开临床试验数量上升幅度最大的热门适应证为系统性红斑狼疮,由去年12月份的7项上升至15项,上升幅度为114.29%;新开临床试验数量下降幅度最大的热门适应证为肥胖,由去年12月份的26项下降到12项,下降幅度为53.85%。(详见表1)
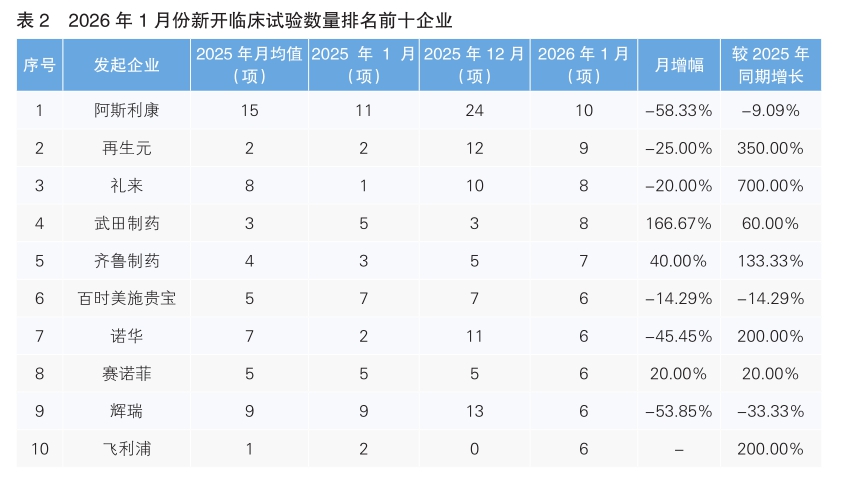
对新开临床试验的发起单位进行统计后发现,1月份发起临床试验最多的企业是阿斯利康,新开临床试验10项,环比下降了58.33%。其次为再生元,新开临床试验9项,环比下降了25%。新开临床试验数量上升幅度最大的企业为武田制药,环比上升了166.67%。值得注意的是,1月份我国药企齐鲁制药进入新开临床试验数量排名前十榜单,新开临床试验7项,环比增长40.00%,同比增长133.33%。(详见表2)
对临床试验的申请国家和地区进行统计后发现,1月份美国仍为临床试验开展最为主要的国家,新开临床试验260项,环比下降了3.35%。其次是中国,新开临床试验数量为118项,环比下降了30.99%。
头部企业表现
阿斯利康1月份新开的10项临床试验中,仅有1项Ⅲ期临床试验,适应证为重症哮喘(NCT07363642),试验药物为Tezepelumab。该药是阿斯利康与安进联合开发的全人源单克隆抗体,作用靶点为胸腺基质淋巴细胞生成素(TSLP)。
再生元1月份新开的9项临床试验中,包含4项Ⅲ期临床试验,其中2项在美国开展,2项在韩国开展。在美国开展的2项Ⅲ期临床试验适应证分别为变应性结膜炎(NCT07309432)和嗜酸性食管癌(NCT07112378)。其中,变应性结膜炎的试验药物为REGN5713,是再生元自主研发的一款人源化单克隆抗体,主要用于白桦树花粉过敏的预防和治疗;嗜酸性食管癌的试验药物为Dupilumab,该药也是一款全人源单克隆抗体,靶向IL-4Rα,可同时阻断IL-4与IL-13两条过敏及炎症核心通路,已获批适应证较为广泛。在韩国开展的2项Ⅲ期临床试验适应证分别为阵发性睡眠性血红蛋白尿症(NCT07154745)和难治性多发性骨髓瘤(NCT07222761)。其中,阵发性睡眠性血红蛋白尿症的试验药物为Pozelimab,该药是一款全人源IgG4P单克隆抗体,也是全球首个获批用于治疗CHAPLE病的药物;难治性多发性骨髓瘤的试验药物为Linvoseltamab,这是一款BCMA/CD3双特异性T细胞接合抗体。
礼来1月份新开的8项临床试验中,有3项为Ⅲ期临床试验,其中2项在英国启动,1项在加拿大开展。在英国开展的2项Ⅲ期临床试验适应证分别为肥胖(NCT07321886)和1型糖尿病(NCT07222137),试验药物分别为Eloralintide和Baricitinib。其中,Eloralintide是礼来研发的长效、选择性胰淀素1受体(AMY1R)激动剂,是GLP-1类别以外的新一代减重药物;Baricitinib是礼来和因赛特合作开发的口服选择性JAK1/JAK2抑制剂。在加拿大开展的Ⅲ期临床试验适应证为肥胖,试验药物为Retatrutide。该药是礼来研发的全球首个每周1次皮下注射的三重激素受体激动剂(GLP-1R/ GIPR/GCGR),主要用于肥胖/超重与2型糖尿病的治疗。
武田制药1月份新开的8项临床试验中,包括3项Ⅲ期临床试验。其中1项Ⅲ期临床试验的适应证为嗜睡症(NCT07363720),试验药物为TAK-861。该药是武田制药研发的全球首个口服、高选择性食欲素受体2(OX2R)激动剂,主要用于治疗1型发作性睡病(NT1)。其余2项Ⅲ期临床试验的适应证分别为多发性骨髓瘤(NCT06980480)和登革热(NCT06579755),试验药物分别为10%免疫球蛋白(IVIG)和四价登革热疫苗。
齐鲁制药1月份新开的7项临床试验中,仅1项推进至Ⅲ期临床试验,其适应证为重型再生障碍性贫血(NCT07345000),试验药物为Romiplostim N01(注射用罗普司亭N01)。该药是齐鲁制药研发的第二代长效血小板生成素受体激动剂(TPORA),此前已于2024年4月在我国获批上市,用于成人慢性免疫性血小板减少症(ITP)。
百时美施贵宝1月份新开的6项临床试验中,仅1项为Ⅲ期临床试验,适应证为神经分裂症(NCT07288567),试验药物为KarXT。该药是全球首个非多巴胺/5-羟色胺机制的口服抗精神病复方药物,通过中枢M1/M4毒蕈碱受体激动起效。
辉瑞1月份新开的6项临床试验中,包含2项Ⅲ期临床试验,适应证分别为中重度慢性阻塞性肺疾病(NCT07363694)和晚期非小细胞肺癌(NCT07222566)。慢性阻塞性肺疾病的试验药物为PF-07275315,该药是2型炎症领域的突破性多靶点生物药,可同时阻断IL-4、IL-13、TSLP,有望为特应性皮炎、哮喘、慢性阻塞性肺疾病等提供更全面的治疗选择。晚期非小细胞肺癌的试验药物为PF-08634404(SSGJ-707),该药是辉瑞自我国药企三生制药引进的PD-1/VEGF双特异性抗体,为肿瘤免疫治疗领域的新一代双靶点药物。
赛诺菲1月份新开的6项临床试验中,包含5项Ⅲ期临床试验,涉及药物包括Duvakitug、PCV21疫苗和Frexalimab。其中,Duvakitug的适应证分别为溃疡性结肠炎(NCT07185009)和克罗恩氏病(NCT07184944),该药是赛诺菲和梯瓦联合开发的全球首款靶向TL1A(TNFSF15)的人源单克隆抗体。PCV21为21价肺炎球菌结合疫苗,本次Ⅲ期临床试验的涉及人群分别为2月龄婴儿(NCT07348692)和镰刀型贫血症患者(NCT07247188)。Frexalimab的适应证为多发性硬化症(NCT07325292),该药是全球首个进入Ⅲ期临床试验的第二代抗CD40L单克隆抗体,解决了第一代药物的血栓相关缺陷,同时实现高效抗炎与低感染风险的平衡。
(数据来源于美国Clinicaltrial数据库,统计时间为2月11日)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐