出海门槛抬高 行业洗牌加速 ——2025年我国医疗器械在美准入认证情况分析
- 2026-04-02 09:22
- 作者:郭绮 林晓娟 许佳锐
- 来源:中国医药报
近年来,我国医疗器械获美国食品药品管理局(FDA)认证数量呈现企稳回升趋势。新型生物材料与高端医疗器械广东研究院数据中心根据FDA数据整理发现,2025年,我国医疗器械获FDA认证数量达534件,较上年增长4.7%;2025年参与FDA认证的企业数量为341家,连续三年下滑,行业出清加速。在获得FDA认证的医疗器械产品中,Ⅱ类医疗器械以超94%的占比占据主导地位;广东省与上海联影分别在地域和企业维度领跑获证产品数量榜单。总体来看,2025年,我国医疗器械获FDA认证情况呈现“总量稳、结构优、头部聚、集群强”的特征。
获证总数温和回升 三大领域产品数量领跑
2022年至2025年,我国医疗器械获FDA认证的总数分别为617件、510件、510件、534件。2025年获证数量在连续两年下滑后小幅回升。
这一趋势背后,一方面是企业从盲目扩张到理性布局的策略转变,另一方面是海外市场竞争加剧等原因让企业更加谨慎地评估投入产出比。此外,FDA对供应链合规、临床试验数据真实性的审查趋严,也抬高了医疗器械企业的申报门槛。
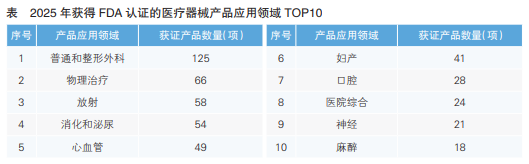
从产品应用领域来看,2025年产品获证数量排在前三的分别是普通和整形外科(125件)、物理治疗(66件)和放射(58件),眼科(1件)、微生物(4件)等领域获证数量较少(详见表)。这一获证格局既体现了我国企业在整形耗材、康复设备、影像配套部件等成熟赛道的规模化出口优势,也暴露了在高端高附加值赛道(如眼科高端植入物、分子诊断试剂)的核心技术短板。
Ⅱ类产品为获证主力 认证周期进一步压缩
按获证产品的风险等级来看,Ⅱ类医疗器械占比超94%,是2025年我国医疗器械出海美国的主力。
我国和美国在医疗器械风险分类上存在一定差异。在我国,医疗器械按照风险程度由低到高,管理类别依次为第一类、第二类和第三类。医疗器械的分类判定需要综合考虑医疗器械的预期目的、结构特征、使用形式、使用状态以及是否接触人体等多方面因素。而FDA将医疗器械按照产品的预期用途和使用适应证等,分为ClassⅠ(Ⅰ类)、Class Ⅱ(Ⅱ类)、Class Ⅲ(Ⅲ类)。其中,Ⅰ类产品风险等级最低,Ⅲ类产品风险等级最高。
在2025年我国获得FDA认证的医疗器械中,Ⅰ类、Ⅱ类、未分类医疗器械获批数量分别为19件、504件、11件,其中Ⅱ类产品占比高达94.4%。
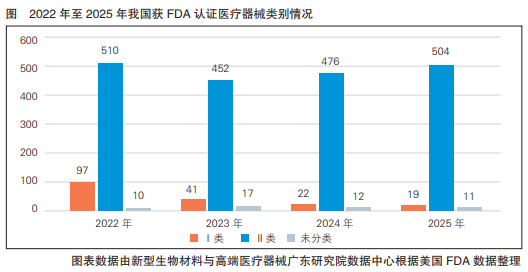
结合2022年至2025年我国医疗器械获FDA认证情况来看,Ⅱ类医疗器械凭借适中的技术门槛与稳定的市场需求,连续多年稳居主导地位,其在获证产品总数中的占比呈逐年增长态势,已然成为我国企业开拓海外市场的“基本盘”(详见图)。Ⅰ类医疗器械因利润空间受限,企业主动投入的意愿逐渐降低;而Ⅲ类医疗器械(如植入式设备、创新体外诊断试剂)受制于高技术壁垒、漫长的认证周期及海外临床数据积累要求,短期内难以实现突破性进展。
从认证效率来看,2025年,我国医疗器械产品获FDA认证总平均周期为144.76天,其中Ⅰ类医疗器械为159.21天,Ⅱ类医疗器械为143.48天。Ⅱ类医疗器械周期更短的核心原因在于:企业申报经验丰富,资料准备精准度提升;FDA对常规Ⅱ类产品优化审查流程,部分纳入“绿色通道”;头部企业通过提前布局合规体系、引入第三方专业机构等,进一步压缩认证周期。
头部梯队稳固 产业集群效应显著
从获证产品的企业数量来看,2022年至2025年参与FDA认证的国产医疗器械企业数量从410家缩减至341家,行业参与主体持续精简。
从2025年企业获证产品数量来看,头部梯队格局稳固。其中,上海联影以17件产品获证排在第一,深圳开颜医疗器械(11件)、深圳童品荟科技(11件)、迈瑞医疗(10件)等区域龙头紧随其后。头部企业凭借深厚的技术积累、充足的资金支撑及成熟的海外合规体系,持续占据主导地位。腰部企业获证产品数量大多为5~8件。尽管腰部企业依托细分赛道的差异化优势不断寻求突破,但受限于技术迭代速度与合规运营成本的双重制约,其与头部企业的差距正逐步拉大。
结合头部梯队的稳固表现与参与FDA认证的企业数量下滑趋势可以看出,我国中小型医疗器械企业因面临市场竞争与合规成本的双重压力,正逐步退出海外认证领域,行业洗牌持续深化。我国医疗器械出海正迈入深水区。
从地域分布来看,2025年获证产品所属企业的地域分布呈现显著集群化特征。广东省以156家企业的数量位居第一,占比45.7%;江苏省以42家的数量排在第二,与浙江省(37家)、上海市(17家)共同构成第二梯队;其他省份企业数量偏少,产业分布不均衡。广东省和长三角地区企业数量占据领先地位,缘于这些地区完善的产业链、活跃的政企协同创新生态。同时,地方出海扶持政策的精准赋能也有效降低了企业合规与研发成本,形成“企业集聚—资源聚合—效率提升”的正向循环。
2025年我国医疗器械产品获得FDA认证情况,清晰地勾勒出产业出海的阶段性特征与转型轨迹,既是我国医疗器械企业出海成果的“成绩单”,更是行业向高质量发展迈进的“风向标”。在全球贸易格局重构、FDA审查趋严的大背景下,我国医疗器械产业的出海之路,已从“拼数量、铺赛道”转向“强技术、守合规、聚生态”的新阶段。未来,唯有以技术创新突破高端瓶颈,以合规体系筑牢出海根基,依托产业集群整合资源优势,才能在全球市场竞争中突破格局限制,实现从“跟跑”到“领跑”的跨越,推动我国医疗器械产业真正走向全球化高质量发展。
(作者单位:新型生物材料与高端医疗器械广东研究院数据中心)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:张可欣)
分享至
右键点击另存二维码!
-
为你推荐
互联网新闻信息服务许可证10120170033
网络出版服务许可证(京)字082号
©京公网安备 11010802023089号 京ICP备17013160号-1
《中国医药报》社有限公司 中国食品药品网版权所有











