每周医药看点(5.31~6.7)
- 2020-06-08 10:37
- 作者:李硕
- 来源:中国食品药品网
点击收听音频↓↓↓
中国食品药品网讯 中央应对新冠肺炎疫情工作领导小组会议要求进一步加强疫苗药物和检测试剂研发工作,国家药监局发布6个指导原则,《医药代表备案管理办法(试行)》征求意见,1类创新药泽布替尼胶囊上市,严重危害正常医疗秩序的人员拟纳入失信人员名单……5月31日~6月7日,医药行业需要关注这些大事。
行业政策动态
1.李克强主持召开中央应对新冠肺炎疫情工作领导小组会议,要求提升能力精准做好常态化防控,进一步加强疫苗药物和检测试剂研发工作。
2.国家市场监督管理总局等九部门联合发布《关于印发2020年纠正医药购销领域和医疗服务中不正之风工作要点的通知》,包括20个要点,将加大打击欺诈骗取医保基金处罚力度,推动各地开展非过评药品带量采购和高值医用耗材带量采购试点。
3.国家药品监督管理局就《医药代表备案管理办法(试行)》征求意见,在医药代表学历限定、备案主体责任、违反禁止事项后处理方式,以及备案平台建设维护等多个方面做出了重大修改。
4.国家药监局印发《医疗器械生产质量管理规范独立软件现场检查指导原则》《肌腱韧带固定系统注册技术审查指导原则》《3D打印髋臼杯产品注册技术审查指导原则》《3D打印人工椎体注册技术审查指导原则》《整形用面部植入假体注册技术审查指导原则》《全膝关节假体系统产品注册技术审查指导原则》等6个指导原则;发布5月进口第一类医疗器械产品备案信息;注销北京甘甘科技有限公司一次性胰岛素笔用针头医疗器械注册证书。
5.国家医保局就《医药价格和招采信用评价的操作规范》和《关于建立医药价格和招采信用评价制度的指导意见》征求意见,拟建立医药价格和招采失信事项目录清单,医药企业的商业贿赂、滥用市场支配地位、操纵市场价格等6种行为将纳入"黑名单"。
6.国家医保局公示第二批医用耗材信息。经公示无异议后,第二批医用耗材信息将纳入国家医保医用耗材分类与代码数据库,供各地医疗保障部门使用。
7.CDE就《化学药品创新药I期临床试验申请药学共性问题相关技术要求》《化学药品Ⅰ期临床试验申请药学研究信息汇总表》《化学药品注射剂包装系统密封性研究技术指南》《化学药品注射剂生产所用的塑料组件系统相容性研究技术指南》、ICH《Q12:药品生命周期管理的技术和监管考虑》及附件中文翻译稿公开征求意见。
8.中检院发布2020年第六期国家药品标准物质供应新情况,包括21个即将上市的新品种,26个即将换批品种的预计上市时间和26个即将失效品种的有效使用期限,对于有效使用期限外的标准物质以及未规定有效使用期限的非最新批次标准物质,中检院将不再对其进行质量监测。
9.国家药典委公示如意珍宝丸等14个药品的国家药品标准修订草案。
10.国家药品不良反应监测中心发布《药物警戒委托协议撰写指导原则(试行)》,明确和规范药物警戒委托工作中持有人和受托方义务和责任。
11.国家药监局食品药品审核查验中心就《药物非临床安全性评价研究机构和药物临床试验机构药品安全信用档案管理制度》征求意见,共包括信用档案的形式和安全要求等十九条内容。
12.《北京市医院安全秩序管理规定》经北京市十五届人大常委会第二十二次会议表决通过,将于今年7月1日施行。规定北京市医院将建立安检制度,对扬言暴力、多次无理缠闹等高风险人员就诊可安排治安保卫人员陪诊。
13.天津市卫生健康委联合27个部门起草的《关于对严重危害正常医疗秩序的失信行为责任人开展联合惩戒的实施方案》公开征求意见,拟将严重危害正常医疗秩序的人员纳入失信人员名单,并实施15项联合惩戒措施。
产品研发/上市
1.国家药监局通过优先审评审批程序附条件批准百济神州(苏州)生物科技有限公司1类创新药泽布替尼胶囊上市,通过优先审评审批程序批准Genzyme(健赞)公司的注射用拉罗尼酶浓溶液上市。
2.CDE网站新增35条药物临床试验登记公示信息(截至6月5日),其中生物制品5个,化学药物28个,中药/天然药物2个,涉及德谷胰岛素注射液、缬沙坦片、益经颗粒等。
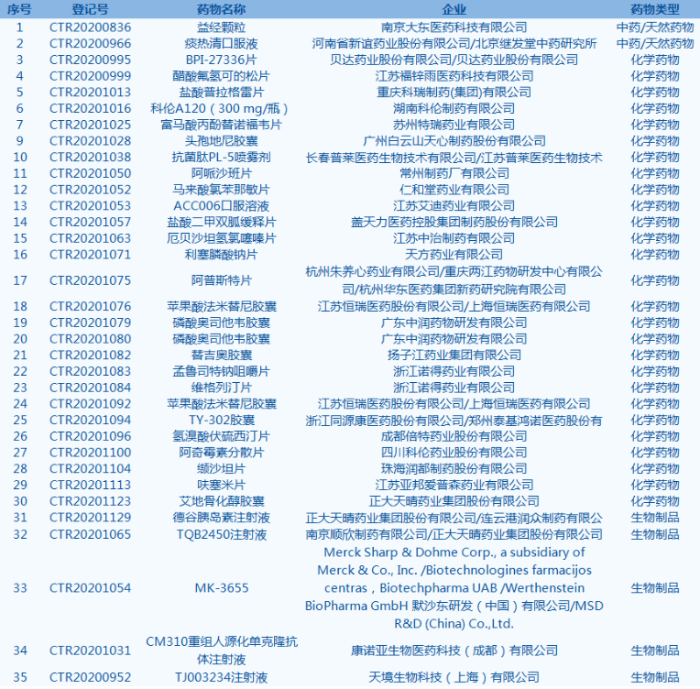
3. CDE网站新增5条仿制药一致性评价任务公示信息(截至6月5日),涉及氯雷他定片等药品。
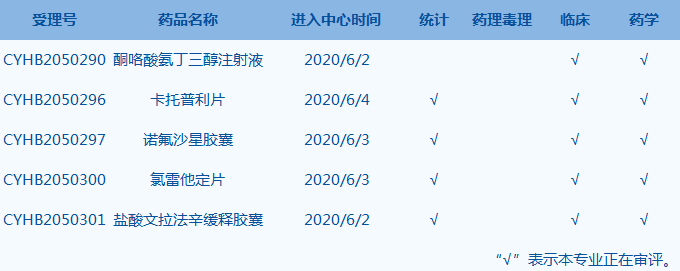
4.恒瑞医药发布公告称,收到国家药监局核准签发的《药品注册批件》,批准公司吉非替尼片注册,发给药品批准文号。
5.齐鲁制药奥沙利铂注射液和恩替卡韦片2款仿制药获批上市,均视同通过一致性评价。对于3类仿制药奥沙利铂注射液,齐鲁制药为国内首家通过该药一致性评价的企业。
6.礼来宣布FDA批准Cyramza(雷莫芦单抗)与厄洛替尼联用一线治疗EGFR 19外显子缺失或21外显子L858R突变的转移性非小细胞肺癌(NSCLC)。至此,Cyramza在特定类型肺癌、肝癌、胃癌和已经获得了FDA的6项批准。
医药企业观察
1.步长制药发布公告,表示其控股子公司浙江天元与兰州百灵签订《产品研发合作协议》及相关补充协议,进一步共同设计和研发四价流感病毒裂解疫苗产品。
2.中国证监会发布公告称,已核发甘李药业IPO批文,标志着甘李药业这家聚焦糖尿病、血液病等多领域药物研发生产的公司即将正式登陆二级资本市场。
3.艾伯维和北京加科思公司宣布达成全球战略合作,共同开发和商业化作用于癌细胞和免疫细胞关键靶点的蛋白酪氨酸磷酸酶(SHP2)抑制剂。根据协议,艾伯维获得SHP2产品组合的独家许可权。
4.江苏柯菲平医药股份有限公司、上海之江生物科技股份有限公司和山西锦波生物医药股份有限公司申请科创板上市申请书均获受理。募资金额分别为15.96亿元、13.56亿元、11.96亿元人民币。
5.嘉和生物药业有限公司宣布完成1.6亿美元的B轮融资,将用于嘉和生物现有产品管线的临床项目推进、早期创新药研发、全球范围内潜在的战略合作,以及为目前处于研发后期的产品商业化做准备。
6.艾伯维、和铂医药、荷兰乌得勒支大学及伊拉斯姆斯大学医学中心联合宣布就一项创新型单克隆抗体的共同开发达成战略合作关系,该抗体将用于预防和治疗新型冠状呼吸道疾病。
7.全球性临床阶段生物制药公司传奇生物正式在美国上市,首日股价暴涨60%,市值近50亿美元。
药品集中采购
1.江苏省医保局发布的《关于进一步落实国家组织集中采购和使用药品医保支付标准配套措施的通知》明确,《全国药品集中采购(江苏)中选品种表》中属于医保目录内的31个中选品种,中选价格即为医保支付标准。
2.宁夏通过仿制药质量和疗效一致性评价药品网上申报工作已开始,2020年3月6日前已公示、公布通过一致性评价资质审核结果的药品和已在宁夏医药采购平台中标(挂网)的药品无需重复申报。
3.黑龙江省医保局发布全省医保特殊药品购药清单,共收录313家医保定点医药机构,可有效保障全省70种医保特殊药品的供应。
4.辽宁印发关于执行多替拉韦钠片等3个药品主动降价结果的通知,同意北京科园信海医药经营有限公司、 正大天睛药业集团股份有限公司、杭州中美华东制药有限公司等3个药品企业生产的3个药品在辽宁省主动降价的申请,6月3日起,对上述药品在全省所有卫生机构执行新的挂网采购价格。
5.青海省药品采购中心发布公告称,对一次性使用留置针开展带量采购,首年约定采购量按全省各级公立医疗机构上报2020年总采购量的70%确定,采购周期原则上不少于2年,具体包括密闭型静脉留置针、开放型静脉留置针、动脉留置针。
6.广西医保局印发通知,自6月1日起将44个中成药和148个西药调出省内医保目录,原广西医保药品支付范围内按规定调增的药品在3年内逐步消化,部分药品被要求按照2019版药品目录执行限定支付范围,缩小了临床适应证的使用,删除了少量药品部分报销的剂型。(中国食品药品网综合整理/李硕)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:李硕)
分享至
右键点击另存二维码!
-
为你推荐














