快来看看,8月上市了哪些新药
- 2020-09-04 10:45
- 作者:陈倩
- 来源:中国食品药品网
美国:7款新药上市
2020年8月美国批准了7款新药,其中包括部分全球首次批准的新药。
2020年8月美国批准上市的新药
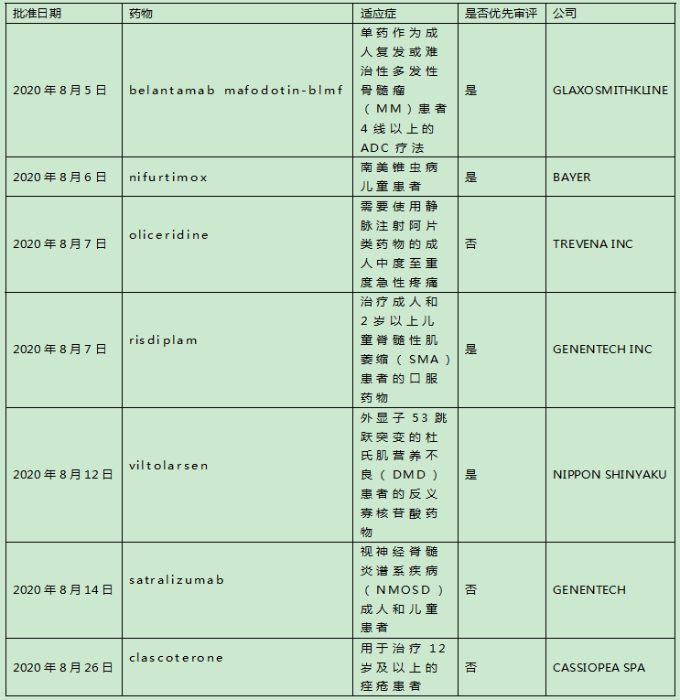
来源:Pharmadigger数据库
目前,抗体偶联药物ADC的研发已经成为制药企业的热点,在过去的十年间,有6款ADC药物获批上市。尤其是在2019年,美国FDA在一年之内批准了3款ADC药物上市。在继2020年4月批准Trodelvy(sacituzumab govitecan-hziy)上市成为首个治疗三阴乳腺癌的ADC药物后,GSK公司的Blenrep(belantamab mafodotin-blmf) 成为今年批准的第二个ADC,这是FDA批准上市的第九个ADC,也是全球首个获批的抗BCMA(B细胞成熟抗原)疗法。BCMA因在MM肿瘤细胞中的特异表达而成为多发骨髓瘤热门靶点,除了ADC,抗BCMA的研发方向还主要集中在CAR-T和双特异性抗体疗法。
罗氏的risdiplam是首个获批上市的口服脊髓性肌肉萎缩症(SMA)药物。诺华的SMA基因疗法Zolgensma (通用名onasemnogene abeparvovec-xioi)在2019年上市后,210万美元的单价让很多患者望而却步,Risdiplam的口服用药优势也许可以给更多患者带来新的治疗选择。该药物已经在中国提交上市申请并被纳入了优先审评。
2018年恩华药业以550万美元、额外注册和商业化里程碑付款以及中国市场10%的版权费付款,从Trevena获得了oliceridine在中国开发和商业化权益。Oliceridine于8月7日在美国成功获批用于住院患者的急性疼痛。
随着机制研究的深入,也有更多的制药企业愿意在自身免疫疾病方面投入更多研发。视神经脊髓炎谱系疾病是一种自身免疫疾病,目前认为IL-6信号通路转导是调节中枢神经系统内外的炎症反应的重要调节通路,这是罗氏IL-6R单抗satralizumab成功获批的关键。目前该药也在中国提交了上市申请。
欧盟:2个生物类似药、3个新药
8月欧盟批准了2个生物类似药和3个新药,其中BCMA-ADC药物同月先在美国FDA获得了上市批准。
2020年8月欧盟批准上市的新药
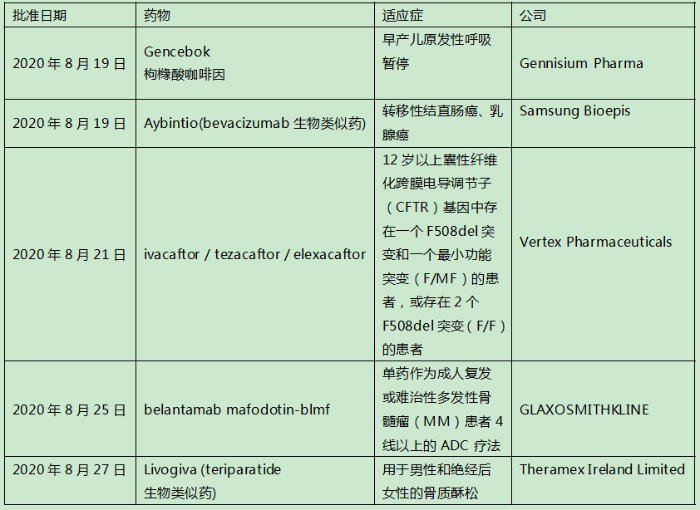
来源:Pharmadigger数据库
欧盟在生物类似药的研发方面一直保持更为开放的态度,8月批准的2款分别是贝伐珠单抗和Teriparatide的生物类似药,都是重量炸弹级别的。其中bevacizumab原研安维汀2018年销售额达到70亿美元;Teriparatide是甲状旁腺素类药物,是第一个被批准的能促合成的治疗骨质疏松药物,原研为礼来公司Forteo,在2018年时销售峰值达到了1749亿美元。
中国:首款曲妥珠单抗生物类似药获批
2020年8月中国批准上市的新药大多来自国外制药企业。
2020年8月中国批准上市的新药
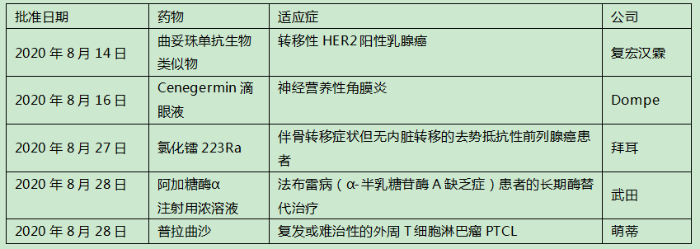
复宏汉霖的第二款生物类似药、中国第一款曲妥珠单抗生物类似药获批上市。在此一个月前,该药就已经在欧盟率先获批上市。目前国内还有7家曲妥珠单抗处于III期临床阶段,包括上海生物制品研究所、嘉和生物、正大天晴、华兰基因、海正药业、安科生物和三星生物。
神经营养性角膜炎是一种罕见的眼科疾病,Cenegermin滴眼液被纳入第一批临床急需境外用药。类似的,阿加糖酶α注射用浓溶液针对法布雷病罕见病,进入第二批临床急需境外新药名单,通过加速审评审批进入中国。
多菲戈®氯化镭(223Ra)注射液是全球首个α例子辐射放射性治疗药物,继2013年首次在美国获批后,至今已经在全球40多个国家(地区)获批,根据Pharmadigger数据库,2018年其全球销售额约为3.89亿美元。
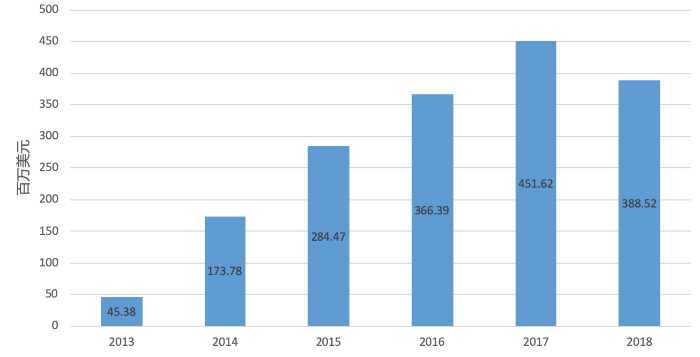
多菲戈®全球销售额
本文仅代表作者观点,不代表本站立场。
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:李硕)
分享至
右键点击另存二维码!
-
为你推荐