2020盘点:FDA批准的53个新药(二)
- 2020-12-29 11:04
- 作者:魏利军
- 来源:中国食品药品网
14.Pemazyre(pemigatinib)
4月17日,FDA加速批准了Incyte公司的成纤维生长因子(FGF)受体2抑制剂pemigatinib,用于携带FGFR2基因融合/重排、既往接受过治疗且不可手术切除或局部晚期的胆管癌成人患者治疗。胆管癌是一种非常罕见的癌症,美国每年新确诊患者约8000人,其中仅有15%的患者属于FGFR2基因突变。EVP预测该产品在2026年的销售额为3.35亿美元。
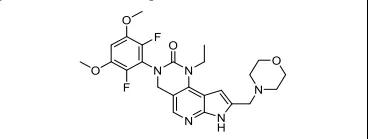
15.Trodelvy(sacituzumab govitecan-hziy)
4月22日,FDA加速批准了Immunomedics公司的抗体药物偶联物(ADC)sacituzumab govitecan,用于治疗既往已接受至少2种疗法的转移性三阴性乳腺癌成人患者。转移性三阴乳腺癌约占侵袭性乳腺癌的15%,目前治疗手段仍以化疗为主,但一般化疗效果较差,应答率一般仅为10%-15%,PFS则只有2-3个月。Sacituzumab是一种靶向于TROP-2(人滋养层细胞表面抗原2)的人源化IgG1抗体,而govitecan是拓扑异构酶抑制剂伊立替康的代谢活性产物。除了三阴乳腺癌,本品开发的适应证还包括直肠癌、前列腺癌、胃癌等多种实体瘤,是2020年最值得关注的药物之一。EVP预测该产品在2026年的销售额可达21.51亿美元。
16.Ongentys(opicapone)
4月24日,FDA批准了Neurocrine公司的新一代儿茶酚-氧位-甲基转移酶(COMT)抑制剂opicapone,与甲基多巴和左旋多巴联用,以改善帕金森病(PD)患者“关”时间。开关现象是PD患者长期应用左旋多巴出现的疗效波动,而“关”主要表现为突然出现肢体僵直,运动不能,此前获批用于改善开关现象治疗的COMT抑制剂有托卡朋和恩他卡朋,但托卡朋因为肝毒性已经很少用。市场方面,本品早在2016年就获得EMA批准上市,但市场表现平平。EVP预测该产品在2026年的销售额为3.44亿美元。
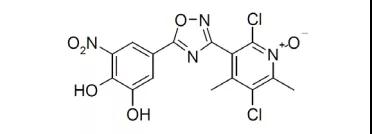
17.Tabrecta(capmatinib)
5月6日,FDA加速批准诺华公司的capmatinib上市,用于治疗MET(上皮-间质细胞转化)外显子14跳跃突变的转移性非小细胞肺癌(NSCLC)成人患者。携带MET外显子14跳跃突变的NSCLC占肺癌患者总量的3%-4%,本品是首个获FDA批准的针对性药物。除了NSCLC,诺华还在开发乳腺癌、淋巴瘤和肾细胞癌等适应证。EVP预测该产品在2026年的销售额可达3.55亿美元。
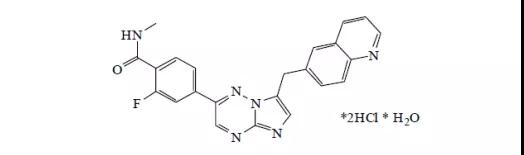
18.Retevmo(selpercatinib)
5月8日,FDA加速批准了Loxooncology公司的selpercatinib,用于治疗RET(转染重排基因)融合阳性的转移性非小细胞肺癌和甲状腺癌,以及RET基因突变的髓样甲状腺癌成人患者。Selpercatinib是首个获得FDA批准用于RET基因改变的药物。EVP预测本品在2026年的销售额可达11.72亿美元。
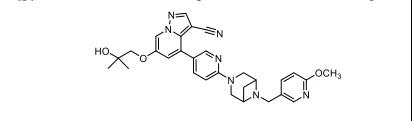
19.Qinlock(ripretinib)
5月15日,FDA批准Deciphera制药的ripretinib上市,用于转移性胃肠间质瘤四线治疗。Ripretinib是一种广谱KIT原癌基因受体酪氨酸激酶抑制剂和PDGFR(血小板衍生生长因子受体)α激酶抑制剂,基因检测数据显示,超过85%的胃肠间质瘤和系统性肥大细胞增多症病例检测到KIT或PDGFRA激酶,另外急性髓细胞白血病(AML)、黑色素瘤、生殖细胞肿瘤、肺癌和成胶质细胞瘤也存在一定比例的KIT或PDGFRA激酶,因此本品应用前景较广,EVP预测本品在2026年的销售额可达13.11亿美元。
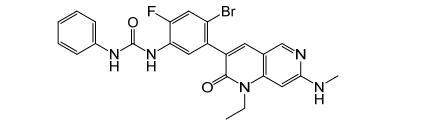
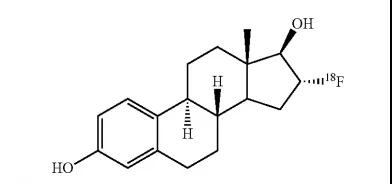
20.Cerianna(fluoroestradiol F18)
5月20日,FDA批准了Zionexa公司的含氟正电子发射型计算机断层显像(PET)剂,用于雌激素受体(ER)阳性病变检测,作为复发或转移性乳腺癌患者活检的辅助手段。本品是一种F-18标记的F取代雌二醇,与雌激素受体有很强的亲和力,而F-18是正电子放射性核素,可核变产生的正电子与周围的负电子发生堙灭现象,产生湮没辐射而成相。
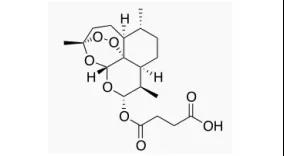
21.Artesunate(青蒿琥酯)
5月26日,FDA批准Amivas公司的青蒿琥酯用于成人或儿童严重疟疾患者初始治疗。疟疾是对人类影响最大的传染病之一,全世界有3亿~5亿人感染过疟原虫,每年有150万~270万人死于该病,其中90%以上病患在非洲。美国疾病控制与预防中心(CDC)数据显示,美国每年仅有约2000个疟疾确诊病例,其中仅300例为重症患者。
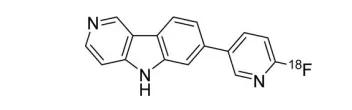
22.Tauvid(flortaucipir F18)
5月28日,FDA批准Avid Radiopharm的Tauvid上市,用于τ蛋白神经纤维纠结的密度和分布成像,为阿尔茨海默病(AD)诊断提供评估依据。Flortaucipir F18可与聚集的τ蛋白结合,靶向分布在病变区域。使用PET技术对病理性τ成像,将有助于AD早期诊断和疾病进展情况监测,在提倡AD疾病早期干预的时代背景下,τ蛋白和β-淀粉样蛋白示踪剂都具有巨大的发展潜力,是国外诊断巨头们争相布局的领域之一。
23.Uplizna(inebilizumab-cdon)
6月11日,FDA批准了Viela生物的inebilizumab,用于水通道蛋白4(AQP4)抗体阳性的视神经脊髓炎谱系疾病(NMOSD)治疗。NMOSD是一种非常罕见的疾病,患者的免疫系统会错误地攻击体内的健康细胞和蛋白质,大约50%的患者会发展成永久性视力障碍和瘫痪。流行病学数据显示,约有1.6万-1.7万美国人罹患此病。除了NMOSD,本品还在开发肾移植、重症肌无力等多种自免疫疾病。EVP预测该产品在2026年的销售额可达5.18亿美元。
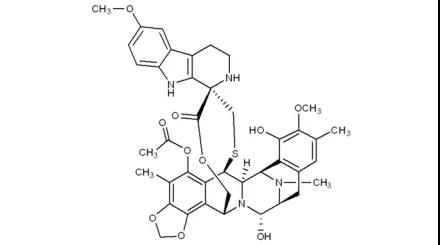
24.Zepzelca(lurbinectedin)
6月22日,FDA加速批准Jazz制药的lurbinectedin上市,用于铂类化疗中进展或化疗后进展的晚期小细胞肺癌(SCLC)治疗。小细胞肺癌约占肺癌总数的13%-15%,目前治疗仍以化疗为主。市场潜力方面,EVP预测本品在2026年的销售额可达3.97亿美元。
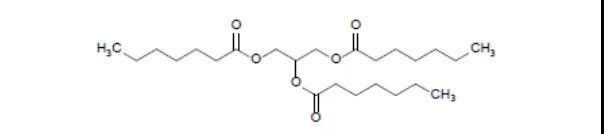
25.Dojolvi(三庚酸甘油酯)
6月30日,FDA批准了Ultragenyx公司的三庚酸甘油酯作为能量和脂肪酸的来源,用于长链脂肪酸氧化紊乱(LC-FAOD)患者治疗。LC-FAOD是一种非常罕见且危及生命的常染色体隐性遗传病,美国每年约有100名新生儿被确诊为该病。该病患者因无法将长链脂肪酸转化为能量而导致线粒体能量生成不足,临床表现为心肌病、运动不耐受、频繁肌痛,反复横纹肌溶解和低血糖等。除了LC-FAOD,本品还在开展多项代谢失调的适应证研究。EVP预测其在2026年的销售额为2.68亿美元。(药事纵横 魏利军)
本文的销售额预测数据均来自Evaluate Pharma网站公开文章。本文已征得作者同意刊发,未经许可不得转载。
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
为你推荐