天津市药监局第五监管办组织药品制剂生产企业对“原辅包”供应商开展联合检查
- 2022-06-27 15:43
- 作者:杨菲
- 来源:中国食品药品网
中国食品药品网讯 近期,天津市药监局第五药品监督管理办公室(以下简称第五监管办)积极探索有益经验多次组织辖区药品制剂生产企业对“原辅包”供应商(以下简称供应商)开展联合检查,进一步深化药品审评审批制度改革工作成果,确保药品上市许可持有人制度和“原辅包”(即化学原料药、药用辅料、直接接触药品的包装材料和容器)关联审评审批制度的有效实施。
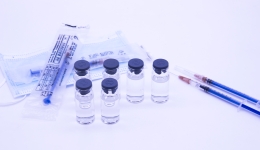
图为现场检查。
摸清底数、拟定方案。在检查工作开展前,第五监管办预先对辖区内药品上市许可持有人、药品生产企业合格供应商信息进行系统梳理并建档成册,充分掌握供需双方合作关系。将“原辅包”日常监管与药品制剂生产企业对其供应商的现场审计相结合,与辖区制剂生产企业组成联合检查组,在明确人员组成、检查重点和任务分工的基础上开展联合检查。
联合检查、共同发力。联合检查组对供应商生产车间、原料及成品库房、检验室、留样室等场所开展现场检查,同时仔细查阅相关企业资质、各类验证方案及报告、“原辅包”生产及检验记录。联合检查组分别从日常监管和现场审计两个角度对供应商存在的问题进行指导,做到相辅相成、互为补充,共同筑牢产品质量安全防线。
研讨交流、持续改进。检查工作结束后,联合检查组与供应商负责人以座谈会的形式,对现场检查情况进行深入分析沟通,对供应商提出的问题予以现场解答。在座谈过程中,第五监管办监管人员也注意听取制剂生产企业和供应商对于质量管理工作的意见和建议,为后续创新“原辅包”监管措施提供来自一线的科学参考。(杨菲)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:张可欣)
分享至
×
右键点击另存二维码!
网民评论
欢迎
登录
-
为你推荐