近期医药看点(1月3日—1月14日)
- 2024-01-16 13:53
- 作者:刘思慧
- 来源:中国食品药品网
中国食品药品网讯 10部门联合发布《关于推进儿童医疗卫生服务高质量发展的意见》;《执业药师继续教育暂行规定》发布……1月3日—1月14日,医药行业的这些动态值得关注。
行业政策动态
1.国家卫生健康委联合国家药监局等10部门发布《关于推进儿童医疗卫生服务高质量发展的意见》,要求补齐儿童用药短板,推动儿童药重点品种原料药与制剂一体化发展,探索医工、医技、医信、医护、医药结合,推动儿童用药、医疗器械等方面“产学研用一体化”,打造一批攻关儿科“卡脖子”关键核心技术的科技领军人才和创新团队等。《意见》在构建高质量儿童医疗卫生服务体系、提供优质化儿童医疗卫生服务、加强现代化儿科人才队伍建设、完善儿童医疗卫生服务高质量发展配套政策等方面提出具体目标。主要目标是:到2025年,完善功能明确、布局合理、规模适当、富有效率的国家、区域、省、市、县级儿童医疗卫生服务体系。儿科医疗资源配置和服务均衡性逐步提高,每千名儿童拥有儿科执业(助理)医师数达到0.87人、床位数达到2.50张,儿童医疗卫生服务能力不断提升。到2035年,基本形成城乡均衡、协同高效的儿童医疗卫生服务体系,更好满足儿童医疗卫生服务需求。
2.国家药监局、人力资源社会保障部印发《执业药师继续教育暂行规定》,以规范执业药师继续教育工作,保障执业药师参加继续教育的合法权益。《规定》共有6章30条,阐明了执业药师继续教育工作的基本要求和执业药师继续教育工作遵循的基本原则,明确了执业药师继续教育管理体制、职责分工,继续教育内容、方式以及机构和学时管理等内容。
3.国家药监局综合司印发《药品网络交易第三方平台检查指南(试行)》,适用于指导药品监管部门对提供第三方平台服务的企业开展监督检查工作。有关检查组织实施、检查机构和人员、检查程序、常规检查、有因检查、检查与稽查的衔接、跨区域检查协作、检查结果的处理等工作,按照《药品检查管理办法(试行)》等有关要求执行。
4.国家医保局办公室发布《关于加强医药集中带量采购中选产品供应保障工作的通知》,要求从及时组织签订采购协议、畅通医疗机构反馈问题渠道、积极协调应对短时间激增需求、做好中选产品供应情况监测、探索建立供应情况评价机制、加强供应情况评分结果运用六方面加强工作。
5.国家医保局办公室发布《关于促进同通用名同厂牌药品省际间价格公平诚信、透明均衡的通知》。通知指出,国家医保局将针对“四同药品”(即通用名、剂型、规格、厂家均相同的药品)进行全面的梳理挂网监测排查。到2024年3月底前,基本消除“四同药品”省际间的不公平高价、歧视性高价,促进省际间价格更加透明,维护患者合法权益。
6.国家药监局药品审评中心(CDE)发布《基于药代动力学方法支持用于肿瘤治疗的抗PD-1/PD-L1抗体可选给药方案的技术指导原则》,进一步指导企业优化抗PD-1/PD-L1抗体的临床用药剂量,提高患者依从性及总体生活质量,并提供可参考的技术规范。《指导原则》主要阐述基于药代动力学建模和模拟的方法,支持抗 PD-1/PD-L1 抗体在上市前和/或上市后给药方案之间的相互转换。该方法适用于PD-1/PD-L1单药治疗方案,或联合治疗方案中仅改变PD-1/PD-L1给药剂量和/或给药间隔的情况。
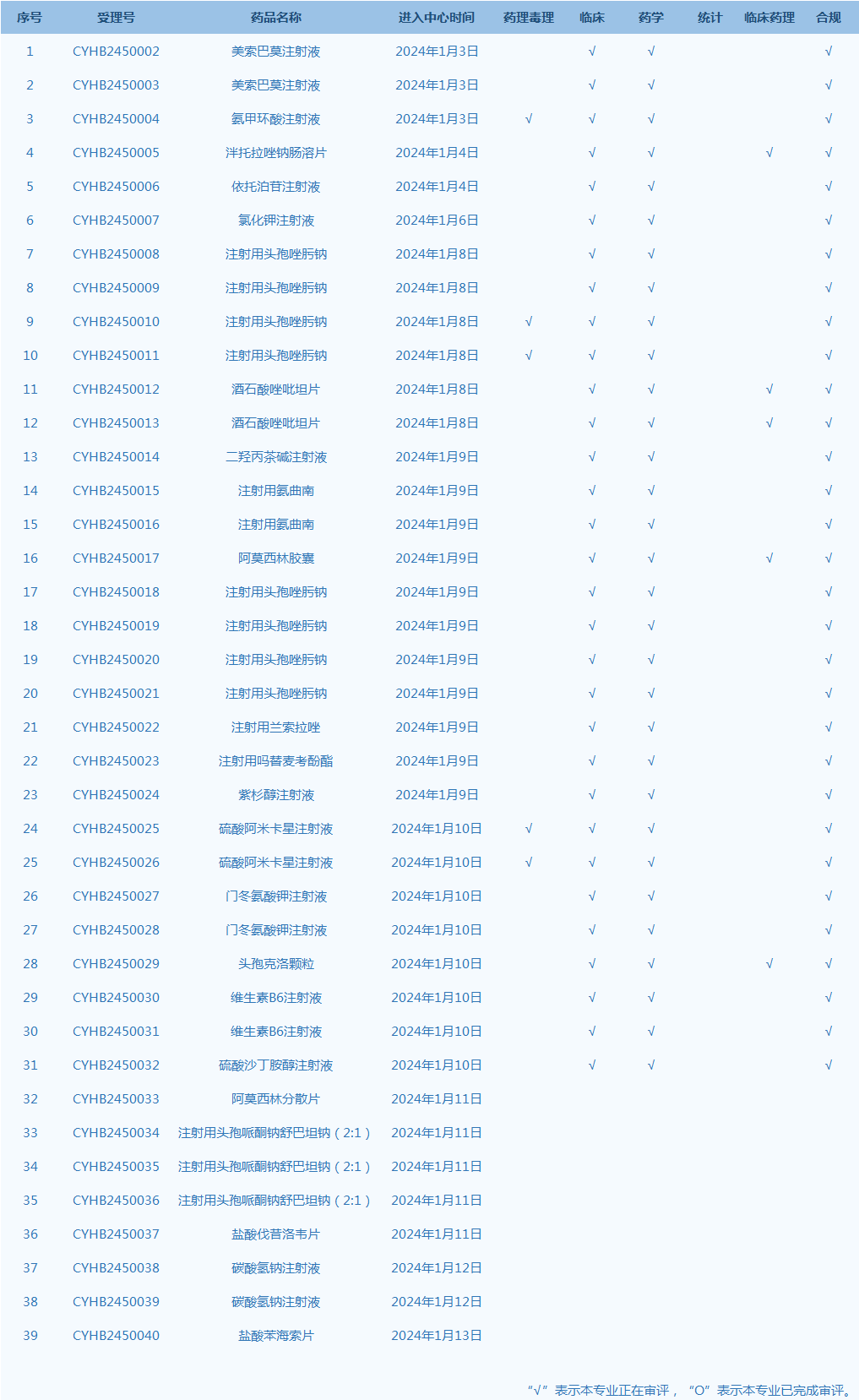
7.CDE网站公示39个仿制药一致性评价任务,涉及美索巴莫注射液等品种(截至1月14日)。
产品研发上市信息
1.国家药监局通过优先审评审批程序批准Eisai Inc.申报的仑卡奈单抗注射液(商品名:乐意保/Leqembi)上市。用于治疗由阿尔茨海默病引起的轻度认知障碍和阿尔茨海默病轻度痴呆。
2.国家药监局批准湖北齐进药业有限公司申报的中药1.1类创新药儿茶上清丸上市。该药品清热退火、解毒敛疮、止痛,用于轻型复发性阿弗他溃疡上焦实热证。
3.国家药监局发布6期药品批准证明文件送达信息,共包括362个受理号,涉及四川科伦药业股份有限公司等企业(截至1月14日)。
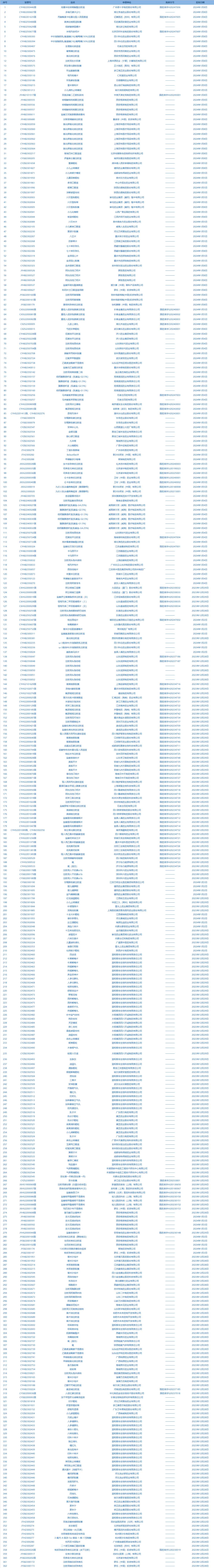
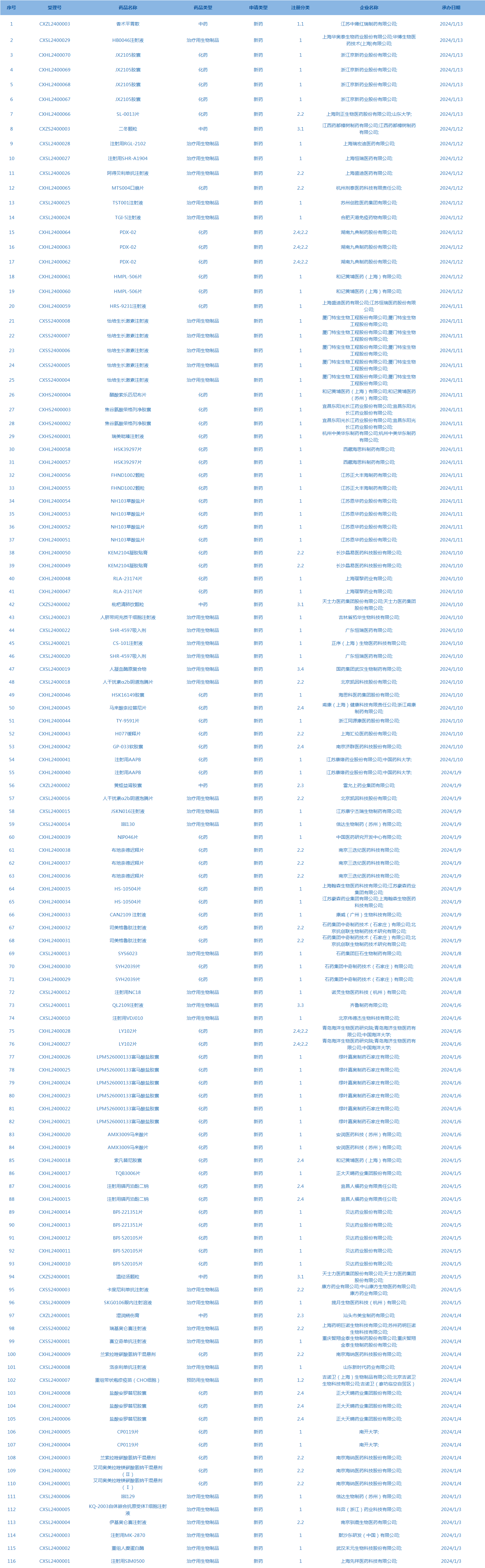
4.CDE承办受理116个新药上市申请,包括HB0046注射液等药品(截至1月14日)。
5.普利制药发布公告称,收到美国食品药品管理局(FDA)签发的伏立康唑干混悬剂和阿昔洛韦钠注射液上市许可;收到加拿大卫生部签发的注射用伏立康唑200mg的上市许可。
6.双成药业发布公告称,收到巴基斯坦药监局核准签发的注射用胸腺法新(基泰)注册批件。
7.和誉医药宣布,其在研的新一代CSF-1R抑制剂Pimicotinib(ABSK021)获得欧洲药品管理局(EMA)授予的孤儿药资格认定,用于治疗不可手术的腱鞘巨细胞瘤(TGCT)。
8.华海药业发布公告称,公司向美国FDA申报的帕罗西汀缓释片的新药简略申请(ANDA)已获得批准。
9.普方生物宣布,公司申报的rinatabart sesutecan (Rina-S,PRO1184)获得美国FDA授予快速通道资格,用于治疗表达叶酸受体α(FRα)的高级别浆液性或子宫内膜样铂耐药的卵巢癌患者。
医药企业观察
1.药明巨诺宣布与2seventy bio签订一项独家合作协议,双方将在大中华区围绕针对自身免疫疾病的嵌合抗原受体(CAR)T细胞治疗产品进行共同开发、制造和商业化,项目名为自身免疫性疾病项目(AID项目)。
2.安锐生物宣布与阿斯利康达成独家选择权和全球许可协议,开发并商业化一款针对表皮生长因子受体(EGFR)L858R突变的新型变构抑制剂,作为治疗晚期EGFR突变的非小细胞肺癌(NSCLC)的潜在新疗法。根据协议条款,安锐生物将获得高达4000万美元的预付款和近期付款,此外基于合作项目取得的研发里程碑和商业化里程碑,安锐生物有权获得超过5亿美元额外付款以及全球净销售额的分级特许权使用费。
3.美纳里尼集团及其全资子公司Stemline Therapeutics和英矽智能达成一项授权许可协议。美纳里尼将获得ISM5043的全球独家开发和商业化权益,这是由英矽智能人工智能平台辅助设计和开发的一种靶向KAT6的新型小分子抑制剂,有望被用于ER+/HER2-乳腺癌和其他癌症的治疗。根据协议条款,该合作交易总额逾5亿美元,包括1200万美元的首付款,以及后续开发、监管和商业里程碑。此外,英矽智能还有望获得潜在可达两位数的特许权使用费率。
4.复宏汉霖宣布与Sermonix Pharmaceuticals达成战略合作和独占许可协议,以在中国开发、生产和商业化Sermonix公司的核心在研产品lasofoxifene。根据协议条款,复宏汉霖将获得lasofoxifene在合作区域内用于至少两项ER+/HER2-乳腺癌适应证的独占权利和分许可权;Sermonix公司将从本次合作中获得首付款及可达5800万美元的里程碑付款,并享有在复宏汉霖合作区域的销售分成。
5.元羿生物宣布与Praxis Precision Medicines达成独家合作和许可协议,元羿生物将在大中华地区开发并商业化治疗原发性震颤的ulixacaltamide。Praxis公司将获得1500万美元的首付款,其中包括500万美元现金和1000万美元的普通股投资。此外,Praxis公司预计将获得2.64亿美元的开发、监管和商业化里程碑付款,以及大中华地区净销售额的分级特许权使用费。
6.舶望制药宣布,已与诺华签订两项独家许可和合作协议,舶望制药将从诺华获得1.85亿美元的首付款,并有资格获得潜在的期权和里程碑付款以及商业销售的分级版税。两项交易潜在总额高达41.65亿美元。根据第一项协议,舶望制药授予诺华公司开发和商业化一项针对心血管疾病的1期项目全球开发和商业化权益独家许可;诺华还将获得针对心血管疾病的最多2个额外靶点的化合物潜在许可选择。根据第二项协议,舶望制药授予诺华公司一项心血管疾病治疗的Ⅰ/Ⅱa期临床试验阶段项目在大中华区以外开发和商业化权益独家许可。
7.安锐生物宣布与美国Avenzo Therapeutics达成转让协议,后者将获得安锐生物自主研发的一款细胞周期蛋白依赖性激酶2(CDK2)选择性抑制剂ARTS-021全球(除大中华区)开发和商业化权益,以及一个将于2025年初提交IND的临床前项目的独家选择权。根据协议条款,安锐生物将获得4000万美元的首付款、额外研发里程碑和商业化里程碑的付款,以及销售额的分级特许权使用费,两个项目的潜在付款总额将会超过10亿美元。
8.诺华宣布就收购信瑞诺医药达成协议,为其加强在肾脏疾病领域的布局迈出坚实一步。信瑞诺医药是一家专注于肾脏疾病及相关治疗领域的临床阶段中国生物技术公司,成立于2021年,是Chinook Therapeutics与数家生命科学投资者共同设立的一家合资公司。诺华于2023年8月收购了Chinook公司,而持有该合资公司的部分股权,此次诺华将收购信瑞诺医药的其余股份。
药品集中采购
1.安徽省医药价格和集中采购中心发布《关于公布安徽省2023年度部分化学药品及生物制剂集采中选结果的通知》,正式公布安徽第五批药品集采中选结果,但未对外公布价格信息。本次共产生107个中选产品,涉及50家企业,对比采购目录,8个品种流标。
2.广东省药品交易中心发布《关于查看广东联盟阿莫西林等药品集中带量采购报名产品相关信息的通知》,相关企业可查看3项集采信息:符合申报条件报名产品及申报品规等信息;同品种同组药品联盟地区医疗机构2022年度采购量表;符合申报条件报名产品价格等信息(用CA证书登录交易系统查看)。(刘思慧整理)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐