每周医药看点(12月1日—7日)
- 2025-12-08 15:42
- 作者:
- 来源:中国食品药品网
国家医保局、人力资源社会保障部印发《国家基本医疗保险、生育保险和工伤保险药品目录(2025年)》和《商业健康保险创新药品目录(2025年)》;国家药监局发布《仿制药参比制剂目录(第九十九批)》,其中包括奥德昔巴特胶囊等品种。……12月1日—7日医药行业的这些动态值得关注。
行业·政策动态
1.国家医保局、人力资源社会保障部印发《国家基本医疗保险、生育保险和工伤保险药品目录(2025年)》。目录调整新增114种药品,其中50种1类创新药;调出了29种临床没有供应或可被其他药物更好替代的药品。一同发布的还有《商业健康保险创新药品目录(2025年)》,共纳入19种药品,包含CAR-T细胞治疗产品和多款罕见病治疗药物。
2.国家药监局发布《仿制药参比制剂目录(第九十九批)》,包括奥德昔巴特胶囊等品种。同时,国家药监局还发布《调出参比制剂目录品种清单(第三批)》,为药用炭胶囊。
3.国家医保局发布《关于开展药品价格登记查询服务的公告》。公告显示,国家医保局与北京市人民政府加强相关合作,认可北京相关国资企业开展药品价格登记查询服务;医药企业可自主申报登记创新药价格,登记范围逐步扩展至有价格登记意愿的其他药品。
4.国家药监局药品审评中心(CDE)发布通知,将江苏威凯尔医药科技股份有限公司的安瑞替尼胶囊纳入儿童抗肿瘤药物研发鼓励试点计划(星光计划)。该试点项目拟开发的儿童适应证为携带神经营养酪氨酸受体激酶(NTRK)融合基因的实体瘤。
5.CDE发布《疫苗临床试验不良事件分级标准指导原则(修订版)》,旨在通过对不良事件的严重程度进行合理分析和判定,规范不良事件分级,提高疫苗安全性评估的科学性。该指导原则自发布之日起施行。
6.12月3日,CDE分别就《化学仿制药药学研究重大缺陷(试行)(征求意见稿)》和《化学仿制药生物等效性研究重大缺陷(试行)(征求意见稿)》面向社会公开征求意见,旨在促进化学仿制药质量提升,指导企业研发,严格仿制药技术审评,提高审评效率。征求意见时限均为自发布之日起1个月。
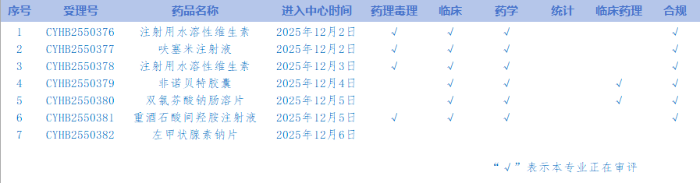
7.CDE网站公示7个仿制药一致性评价任务(详见表),涉及注射用水溶性维生素等品种。
产品研发·上市信息
1.国家药监局发布3期药品批准证明文件送达信息,共包括38个受理号,涉及昆明源瑞制药有限公司等企业。
2.CDE承办受理71个新药上市申请,包括清金化痰颗粒等。
3.和其瑞医药宣布,公司的靶向催乳素受体的单克隆抗体HMI-115已获得美国食品药品管理局(FDA)授予快速通道资格认定。HMI-115拟用于治疗子宫内膜异位症相关的中重度疼痛。
4.石药集团宣布,集团开发的GLP-1/GIP受体双偏向性激动多肽注射液SYH2069注射液的临床试验申请已获得FDA批准。SYH2069注射液拟用于肥胖或超重合并至少一种体重相关合并症人群的体重管理。
5.正大天晴药业集团宣布,集团的1类新药TQF3250胶囊的临床试验申请已获得FDA批准。TQF3250胶囊拟用于减重适应证。
医药企业观察
1.科伦博泰宣布,与Crescent Biopharma,Inc.达成合作。此次合作涉及科伦博泰的抗体偶联药物SKB105,以及Crescent的双特异性抗体CR-001。两款候选药物均用于治疗实体瘤。根据合作条款,科伦博泰授予Crescent Biopharma,Inc.在美国、欧洲等国家及地区的研究、开发、生产和商业化SKB105的独家权利;Crescent Biopharma,Inc.授予科伦博泰在中国研究、开发、生产和商业化CR-001的独家权利。
2.先声药业宣布,与苏州旺山旺水生物医药股份有限公司订立许可协议。根据协议,先声药业将获得氢溴酸氘瑞米德韦干混悬剂在中国用于抗呼吸道合胞病毒感染以及抗人偏肺病毒感染适应证的独家许可权益。
3.华东医药宣布,全资子公司华东医药(杭州)有限公司与贵州生诺生物科技有限公司及该公司全资子公司上海生诺医药科技有限公司、江苏太瑞生诺生物医药科技有限公司(以下简称生诺医药)达成独家商业化合作协议。根据协议,生诺医药作为药品上市许可持有人,负责利那拉生酯的研发、注册、生产和供应;华东医药将负责利那拉生酯在中国的商业化推广工作。
药品集中采购
1.上海市医药集中招标采购事务管理所发布公告,公布2025年9月部分短缺药的全国平均价。公布的药品品种包括重酒石酸去甲肾上腺素注射液等。同时,公告要求,医疗机构根据市场供需情况,在保供稳价的基础上,采购质量可靠、价格适宜的药品。
2.根据上海市医药集中招标采购事务管理所发布的通知,因未按要求调整药品价格,自2025年11月28日起暂停上海信谊金朱药业有限公司生产的甲硫酸新斯的明注射液(规格:2ml:1mg*1支/支,中硼硅玻璃安瓿装)的采购资格。
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐