2月份中美欧批准上市新药盘点 我国自主研发的三款新药在全球范围内首次获批上市
- 2026-04-03 09:59
- 作者:陈倩
- 来源:中国医药报
2月份,中美欧批准上市的新药中,中国批准的新药数量最多,为5款;美国批准4款;欧盟批准3款新药上市。
中国批准5款新药上市
2月份,我国共批准5款新药上市(详见表1)。根据Pharmadigger数据库,安沐奇塔单抗注射液、罗伐昔替尼片和硫酸索西美雷塞片为我国企业自主研发的全球范围内首次获批上市的新药。
精氨酸艾曲莫德片(商品名:维适平)是一款高选择性鞘氨醇-1-磷酸受体(S1PR)调节剂,可选择性作用于S1PR1、S1PR4和S1PR5靶点。该药最初由美国Arena Pharmaceuticals开发,2017年12月,云顶新耀以总交易额2.24亿美元获得其在大中华区和韩国的独家开发、生产及商业化权益。2021年12月,辉瑞完成对Arena的收购,进而取得该产品的全球剩余权益。该药本次获批的适应证为:对传统治疗或生物制剂应答不充分、失应答或不耐受的成人中度至重度活动性溃疡性结肠炎。其亚洲多中心Ⅲ期临床研究数据显示,经40周维持治疗后,艾曲莫德组在主要终点及全部关键次要终点上,均较安慰剂组实现具有临床意义与统计学意义的改善。该药最早于2023年10月在美国获批上市。
米吉珠单抗注射液[商品名:安妥来(皮下注射);安妥来利(静脉输注)]由礼来研发,是一款选择性靶向白细胞介素-23(IL-23)p19亚基的单克隆抗体。该药通过阻断IL-23与受体结合,抑制促炎细胞因子和趋化因子释放,从而发挥抗炎作用。该药本次获批用于治疗成人中重度活动性克罗恩病及溃疡性结肠炎。其中,克罗恩病适应证的获批主要依据其VIVI D-1全球Ⅲ期临床研究。研究结果显示,米吉珠单抗组较安慰剂组在联合主要终点及全部关键次要终点上均实现具有临床意义的改善。溃疡性结肠炎适应证的获批则基于LUCENT系列全球Ⅲ期临床研究结果:米吉珠单抗组64%的患者获得临床应答,24%的患者达到临床缓解,数据均显著优于安慰剂组。该药此前已于2023年3月在日本获批上市。
安沐奇塔单抗注射液(商品名:益赛拓)由三生国健自主研发,为抗白细胞介素17A(IL-17A)单克隆抗体,用于治疗适合系统治疗或光疗的中度至重度斑块状银屑病成人患者。该药也是目前国内已获批上市产品中,少数可在维持期实现每8周1次给药的IL-17A抑制剂之一。在作用机制方面,安沐奇塔单抗拥有独特的抗原结合表位,对IL-17A表现出较高亲和力、较强抑制活性和较好稳定性,同时免疫原性较低。该药本次获批主要基于其Ⅲ期临床研究结果:约三分之二的患者在第52周时可实现皮损完全清除。
罗伐昔替尼片(商品名:安煦)是正大天晴自主研发的新型口服JAK/ROCK双靶点抑制剂,适用于中危-2或高危的原发性骨髓纤维化、真性红细胞增多症后骨髓纤维化或原发性血小板增多症后骨髓纤维化成人患者的一线治疗,主要改善疾病相关脾肿大或疾病相关症状。作用机制方面,罗伐昔替尼既可抑制JAK家族激酶活性、阻断JAK/STAT通路异常持续激活,又可抑制ROCK2、降低STAT3磷酸化水平,进而在一定程度上重建免疫平衡。该药本次获批主要基于其一项关键注册研究结果:经独立评审委员会评估,治疗第24周时,罗伐昔替尼组脾脏体积缩小≥35%的患者比例为58.33%,显著高于对照组的22.86%。今年3月4日,正大天晴宣布将罗伐昔替尼在全球范围内开发、生产和商业化的独家许可授权给赛诺菲。根据公开信息,正大天晴母公司中国生物制药可获得最高15.3亿美元交易总金额,其中包括1.35亿美元的首付款,以及后续开发、注册与销售相关里程碑付款,并可基于罗伐昔替尼年度净销售额获得最高双位数阶梯式特许权使用费。
硫酸索西美雷塞片(商品名:济乐美)是杭煜制药自主研发的KRAS G12C抑制剂,适用于至少接受过一种系统性治疗的鼠类肉瘤病毒癌基因G12C突变型晚期非小细胞肺癌成人患者。其临床前研究显示,与同靶点药物相比,该药物具有更强的脑通透性,且无明显心脏毒性及药物相互作用风险。该药本次获批基于其Ⅱ期临床试验数据,结果显示,约半数患者达到客观缓解,中位缓解时间为1.4个月。
美国批准4款新药上市
2月份,美国批准4款新药上市(详见表2)。根据Pharmadigger数据库,Milsaperidone为全球范围内首次获批。
Difamilast(商品名:Adquey)由大塚制药研发,是一款非甾体、高选择性外用磷酸二酯酶4(PDE4)抑制剂,用于2岁及以上儿童与成人轻中度特应性皮炎的局部治疗。其作用机制为精准抑制与炎症密切相关的PDE4B亚型,阻断IL-4、IL-13、TNF-α等促炎细胞因子释放,从源头控制炎症与瘙痒。该药本次获批基于其关键全球Ⅲ期临床研究。研究结果显示,患者接受1% Difamilast治疗后,从研究者整体评估(IGA)看,其治疗成功率显著优于安慰剂组,且差异具有统计学意义。该药最早于2021年9月在日本获批上市。
Milsaperidone(商品名:Bysanti)由Vanda公司研发,为伊洛哌酮的前体药物,口服后可迅速转化为伊洛哌酮并发挥药理作用。该药本次获批用于治疗成人精神分裂症,以及成人双相I型障碍伴发躁狂或混合发作急性期治疗。其核心机制为拮抗中枢多巴胺D2受体与5-羟色胺2A(5-HT2A)受体。其中,对D2受体的拮抗有助于调节中脑边缘通路的多巴胺能神经传递,是控制精神分裂症阳性症状及躁狂期精神运动性兴奋的重要基础;对5-HT2A受体的拮抗,则有助于改善阴性症状和部分认知功能,同时降低单纯D2拮抗所致锥体外系不良反应风险。该药本次获批主要基于一项为期4周的多中心、随机、双盲、安慰剂对照试验。试验结果显示,Milsaperidone 12mg每日两次给药组在精神症状和体征量表改善方面显著优于安慰剂组。
Pegzilarginase-nbln(商品名:Loargys)由Immedica公司研发,是经PEG修饰的重组人精氨酸酶1,通过金属离子优化提升酶活性与体内半衰期,用于治疗精氨酸酶1缺乏症(ARG1-D)相关高精氨酸血症。ARG1-D是一种极为罕见的常染色体隐性遗传代谢病,是尿素循环障碍中最少见的亚型之一。该药本次获批基于一项Ⅲ期临床试验。试验结果显示,在2至29岁ARG1-D患者中,经Pegzilarginase-nbln治疗24周后,约90.5%的患者血精氨酸水平降至正常范围或指南目标值以下,显著优于安慰剂组。该药此前已于2023年12月在欧盟获批上市。
Navepegritide(商品名:Yuviwel)由Ascendis公司基于TransCon技术平台研发,是一款C型利钠肽(CNP)前药,采用每周一次皮下注射给药。该药通过持续释放活性CNP,拮抗软骨发育不全患者体内过度激活的FGFR3信号通路,从而促进线性生长。其关键研究结果表明,Navepegritide可显著提高2岁及以上、骨骺未闭合的软骨发育不全儿童的年化生长速度,达到预设主要疗效终点。
欧盟批准3款新药上市
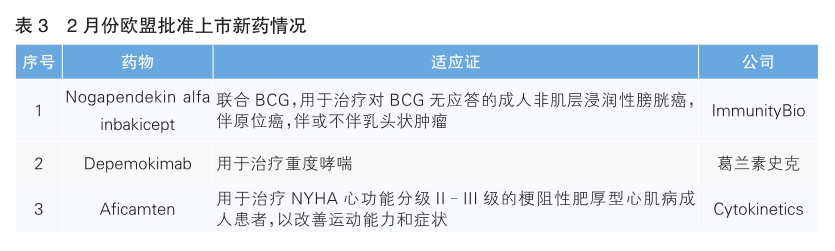
2月份,欧盟批准3款新药上市(详见表3)。根据Pharmadigger数据库,均非全球首次批准上市的新药。
Nogapendekin alfa inbakicept(商品名:Anktiva)是ImmunityBio公司研发的IL-15受体激动剂。该药可联合卡介苗(BCG),用于治疗对BCG无应答的成人非肌层浸润性膀胱癌,伴原位癌,伴或不伴乳头状肿瘤。该药此前已于2024年4月在美国获批上市。
Depemokimab(商品名:Exdensur)是葛兰素史克研发的新一代抗IL-5单克隆抗体,用于治疗重度哮喘。该药具有半衰期长、结合亲和力高、药效强的特点,仅需每半年注射一次。该药此前已于2025年12月在美国获批上市。
Aficamten(商品名:Myqorzo)是Cytokinetics公司研发的选择性小分子心肌肌球蛋白抑制剂,用于治疗NYHA(纽约心脏协会)心功能分级Ⅱ-Ⅲ级的梗阻性肥厚型心肌病成人患者,以改善运动能力与临床症状。该药通过化学结构优化提升治疗指数与药代动力学特征,减少每个心动周期中活性肌球蛋白产力横桥的数量,从而抑制肥厚型心肌病相关的心肌过度收缩。该药此前已于2025年12月在美国获批上市。
(注:本文中的新药分别按中国、美国、欧盟三地新分子实体或生物药首次NDA/BLA来统计,一些药物首先在美国上市后首次在中国或欧盟上市时也会纳入统计)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐