9月份美国Clinicaltrial数据库临床试验数据显示—— 乳腺癌药物研发最为活跃
- 2025-10-23 13:53
- 作者:陈宇哲
- 来源:中国医药报
根据美国Clinicaltrial数据库数据,今年9月份,全球新开由企业资本主导的临床试验总数为826项,数量较8月份上升18.51%;单月新开临床试验数量高于去年同期水平,同比上升28.46%。
热门领域分布
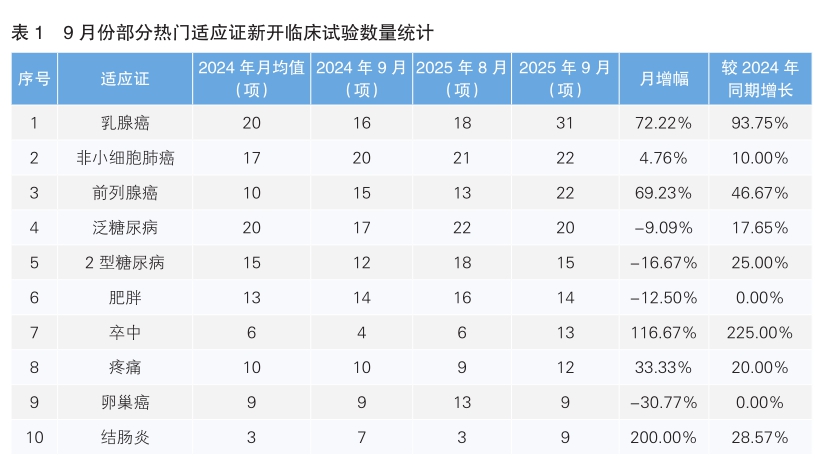
从9月份新开临床试验热门适应证来看,乳腺癌为最主要的热门研发领域,新开临床试验31项,环比上涨72.22%,同比上涨93.75%。其次为非小细胞肺癌,新开临床试验22项,与去年同期相比上涨10.00%。值得注意的是,9月份新开临床试验数量上升幅度最大的热门适应证为结肠炎,由8月份的3项上升至9项,上升幅度为200.00%;数量下降幅度最大的适应证为卵巢癌,由8月份的13项下降到9项,下降幅度为30.77%。(详见表1)
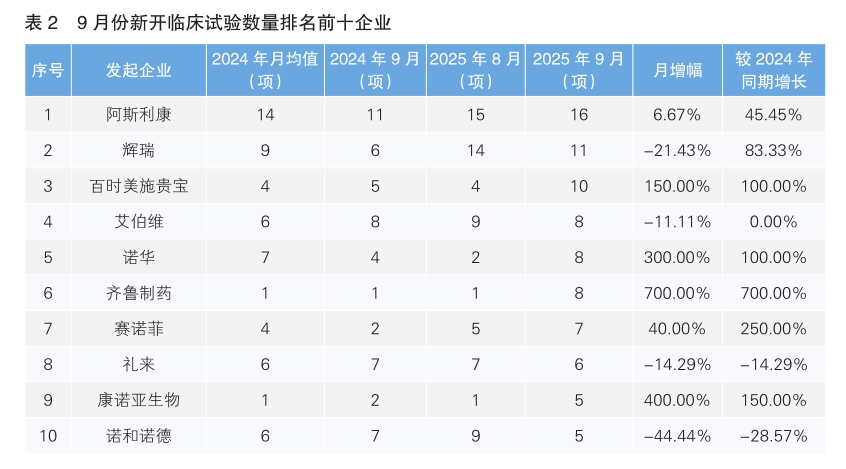
对新开临床试验的发起企业进行统计后发现,9月份发起临床试验最多的企业为阿斯利康,新开临床试验16项,环比上升6.67%,同比上升45.45%。其次为辉瑞,新开临床试验11项,环比下降21.42%,同比增长83.33%。值得注意的是,9月份我国药企齐鲁制药和康诺亚生物进入新开临床试验数量排名前十榜单,分别新开8项和5项临床试验。其中,齐鲁制药为新开临床试验数量上升幅度最大的企业,与8月份相比上升了7倍。(详见表2)
对临床试验的申请国家和地区进行统计后发现,9月份美国仍为临床试验开展最为主要的国家,新开临床试验227项,相较8月份上涨了1.79%。其次是中国,新开临床试验数量为113项,与8月份相比下降了21.53%。
头部企业表现
9月份新开临床试验数量排名前三的企业分别为阿斯利康、辉瑞和百时美施贵宝,数量分别为16项、11项、10项。
阿斯利康9月份新开的16项临床试验中,有两项为Ⅲ期临床试验,适应证均为肿瘤。其中一项的适应证为尿路上皮癌(NCT07205822),试验药物为Dato-DXd(德达博妥单抗)。该药是一种靶向TROP2的抗体偶联药物(ADC),主要用于治疗乳腺癌和非小细胞肺癌。另一款进入Ⅲ期临床试验的药物为Durvalumab,适应证为硬纤维瘤(NCT06992609)。Durvalumab是一种人源化的抗PD-L1蛋白单克隆抗体,可阻断PD-L1与PD-1和CD80结合的能力。
辉瑞9月份新开的11项临床试验中,有3项为Ⅲ期临床试验,其中两项的适应证均为肿瘤,分别为泛晚期肿瘤(NCT06103734)和广泛性小细胞肺癌(NCT07028853)。其中,泛晚期肿瘤的试验药物为Zavegepant,该药属于第三代高选择性降钙素基因相关肽(CGRP)受体拮抗剂,通过阻断CGRP信号通路发挥治疗作用;广泛性小细胞肺癌的试验药物为Mevrometostat,是一款选择性EZH2抑制剂。另一项Ⅲ期临床试验的适应证为体外膜氧合并发症(NCT07029828),试验药物为Ritlecitinib,该药是一种口服选择性JAK3抑制剂。
百时美施贵宝9月份新开的10项临床试验中,有3项为Ⅲ期临床试验,适应证分别为多发性硬化症(NCT07140913)、肾结石(NCT07116967)和克罗恩病(NCT06979453)。以多发性硬化症为适应证的试验药物为Xanomeline/Trospium Chloride,这是一款复方药物。其中,Xanomeline通过激活中枢神经系统的M1/M4受体,改善精神分裂症的阳性(如幻觉)、阴性(如情感淡漠)及认知症状;Trospium Chloride作为外周拮抗剂,抑制Xanomeline对胃肠道的副作用(如恶心、呕吐),提高机体耐受性。以肾结石和克罗恩病为适应证的试验药物均为Deucravacitinib,该药是一种选择性酪氨酸激酶2(TYK2)变构抑制剂,通过选择性结合TYK2假激酶结构域,抑制IL-12/23和Ⅰ型干扰素信号通路,从而调节免疫反应。
齐鲁制药9月份新开8项临床试验,其中3项为Ⅲ期临床试验,适应证分别为周围神经病变(NCT07162883)、胰腺癌(NCT07079228)和特应性皮炎(NCT06732323)。以周围神经病变为适应证的试验药物为QL2107,这是一款PD-1抑制剂生物类似药。以胰腺癌为适应证的试验药物为QLS31905,该药是齐鲁制药自主研发的靶向Claudin18.2(CLDN18.2)和CD3的双特异性T细胞衔接器(BiTE),通过结合肿瘤细胞表面的CLDN18.2和T细胞表面的CD3,激活T细胞,从而杀伤肿瘤细胞。以特应性皮炎为适应证的试验药物为ESG401,该药是一款靶向 CLDN18.2的单克隆抗体,主要用于治疗CLDN18.2阳性实体瘤。
康诺亚生物9月份新开的5项临床试验中,包括两项Ⅲ期临床试验,适应证分别为多发性硬化症(NCT07181239)和特应性皮炎(NCT07106372)。多发性硬化症的试验药物为CM336,该药是康诺亚生物自主研发的一款靶向BCMA和CD3的双特异性抗体,通过同时结合靶细胞上的BCMA和T细胞上的CD3,激活T细胞介导的细胞毒性(TDCC)作用,从而清除靶细胞。以特应性皮炎为适应证的试验药物为Stapokibatrt,该药是一款靶向I L-4Rα的单克隆抗体,主要用于治疗2型炎症性疾病。
(数据来源于美国Clinicaltrial数据库,统计时间为10月9日)
《中国医药报》社版权所有,未经许可不得转载使用。
(责任编辑:刘思慧)
分享至
右键点击另存二维码!
-
相关阅读
-
为你推荐